黑龙江省大庆市东风中学2020-2021学年高一上学期第一次阶段考试化学试题
黑龙江
高一
阶段练习
2020-10-20
254次
整体难度:
较易
考查范围:
认识化学科学、物质结构与性质、初中衔接知识点、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.野火烧不尽,春风吹又生 | B.粉身碎骨浑不怕,要留清白在人间 |
| C.春蚕到死丝方尽,蜡炬成灰泪始干 | D.爆竹声中一岁除,春风送暖入屠苏 |
| A.酸、碱、盐可能都不含金属元素 |
| B.含氧元素的化合物一定是氧化物 |
| C.单质不一定只含一种元素 |
| D.酸、碱中一定含氢,盐一定不含氢 |
| A.Cl2→Cl- | B.I-→I2 | C.SO2→SO32- | D.CuO→Cu |
【知识点】 氧化还原反应的几组概念解读
| A.纯净物与混合物:是否仅含有一种元素 |
| B.溶液与胶体:本质区别是能否发生丁达尔现象 |
| C.电解质与非电解质:水溶液是否能导电 |
| D.氧化还原反应的本质:有电子转移 |
| A.O4是一种化合物 |
| B.O4是由O2组成的混合物 |
| C.O4 和 O2互为同素异形体 |
| D.一个 O4 分子由 2个O2分子构成 |
| A.F2、K、HCl | B.Cl2、Al、H2 |
| C.NO2、Na、Br2 | D.O2、SO2、H2O |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的规律解读
 +2M3++4H2O=
+2M3++4H2O=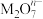 +Cl-+8H+,
+Cl-+8H+, 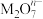 中M的化合价是
中M的化合价是 | A.+4 | B.+5 | C.+6 | D.+7 |
【知识点】 氧化还原反应基本概念 氧化还原反应方程式的书写与配平解读
C
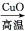 CO2
CO2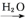 H2CO3
H2CO3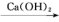 CaCO3
CaCO3 CO2
CO2| A.化合反应、置换反应、分解反应、复分解反应 |
| B.置换反应、复分解反应、化合反应、分解反应 |
| C.置换反应、化合反应、分解反应、复分解反应 |
| D.置换反应、化合反应、复分解反应、分解反应 |
① 有色玻璃 ② 淀粉溶液 ③ 碘酒 ④云、雾 ⑤ Fe(OH)3悬浊液
| A.①③ | B.②④⑤ | C.①③⑤ | D.③⑤ |
A.2Fe3++2H2O+SO2=2Fe2++SO +4H+ +4H+ |
| B.2Fe2++Cl2=2Fe3++2Cl- |
C.I2+SO2+2H2O=4H++SO +2I- +2I- |
| D.H2O2+H2SO4=SO2↑+O2↑+2H2O |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
A.在无色透明溶液中:Fe2+、K+、NO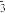 、Cl- 、Cl- |
B.在SO 存在的溶液中:Na+、Mg2+、Ca2+、I- 存在的溶液中:Na+、Mg2+、Ca2+、I- |
C.在pH=1的溶液中:K+、Ba2+、HC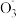 、Br- 、Br- |
D.在滴加酚酞试液显红色的溶液中:Na+、S2-、C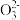 、K+ 、K+ |
【知识点】 限定条件下的离子共存解读
| A.盐酸中逐滴加入食盐溶液 | B.硫酸中逐滴加入氢氧化钠溶液 |
| C.硫酸中逐滴加入氢氧化钡溶液 | D.醋酸中逐滴加入氨水 |
A. 在熔融状态下的电离方程式为 在熔融状态下的电离方程式为 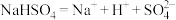 |
| B.纯水几乎不导电,但水是电解质 |
C. 和 和  溶于水后能导电,故 溶于水后能导电,故 和 和  为电解质 为电解质 |
D. 在水溶液中的电离方程式: NaHCO3 = Na+ +H+ + CO 在水溶液中的电离方程式: NaHCO3 = Na+ +H+ + CO |
【知识点】 电解质的电离 非电解质、电解质物质类别判断解读 电离方程式解读
| A.一元酸 | B.二元酸 | C.三元酸 | D.不能确定 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
| A.HCl+NaHCO3=NaCl+H2O+CO2↑ |
| B.2HCl+BaCO3=BaCl2+H2O+CO2↑ |
| C.H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ |
| D.2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读
| A.KOH和CH3COONH4与Ba(OH)2与NH4Cl |
| B.AgNO3和HCl与Ag2CO3和HCl |
| C.BaCl2和Na2SO4与Ba(OH)2与H2SO4 |
| D.CH3COOH和Na2CO3与CH3COOH和NaHCO3 |
【知识点】 离子反应的发生及书写
①2BrO
 +Cl2=Br2+2ClO
+Cl2=Br2+2ClO ;
;②5Cl2+I2+6H2O=2HIO3+10HCl;
③ClO
 +5Cl-+6H+=3Cl2↑+3H2O。
+5Cl-+6H+=3Cl2↑+3H2O。下列微粒氧化性强弱顺序正确的是
A.ClO >BrO >BrO >HIO3>Cl2 >HIO3>Cl2 | B.BrO >Cl2>ClO >Cl2>ClO >HIO3 >HIO3 |
C.BrO >ClO >ClO >Cl2>HIO3 >Cl2>HIO3 | D.Cl2>BrO >ClO >ClO >HIO3 >HIO3 |
| A.氧化镁与稀硫酸混合:MgO+2H+=Mg2++H2O |
| B.稀硫酸滴在铜片上:Cu+2H+=H2↑+Cu2+ |
| C.向稀盐酸溶液中加铁:3Fe+6H+=3Fe3++3H2↑ |
D.澄清石灰水中滴加少量NaHCO3溶液:Ca2++2OH-+2HCO =CaCO3↓+2H2O+CO =CaCO3↓+2H2O+CO |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
①SiO2(石英砂)+2C(焦炭)
 Si(粗硅)+2CO↑
Si(粗硅)+2CO↑②Si(粗硅)+2Cl2
 SiCl4
SiCl4③SiCl4+2H2
 Si(纯硅)+4HCl
Si(纯硅)+4HCl下列对上述三个反应的叙述中,不正确的是
| A.①③为置换反应 |
| B.①②③均为氧化还原反应 |
| C.②为化合反应 |
| D.三个反应的反应物中硅元素均被还原 |
 N2+6NH4Cl,被氧化的NH3与被还原的Cl2的物质的量之比为
N2+6NH4Cl,被氧化的NH3与被还原的Cl2的物质的量之比为| A.2∶3 | B.8∶3 | C.6∶3 | D.3∶2 |
【知识点】 与氧化剂、还原剂有关的计算解读
二、填空题 添加题型下试题
(1)2019年12月27日“胖五”在文昌航天发射场顺利升空。“胖五”的燃料系统大部分是以-183℃的液氧①为氧化剂、-253℃的液氢②为燃料——这已经接近低温的极限,所以又称为“冰箭”。“胖五”的动力心脏——大推力氢氧发动机和液氧煤油③发动机都是全新研制的。
(2)2019年3月10日我国长征三号乙运载火箭在西昌卫星发射中心完成第300次发射。长征三号乙运载火箭的一子级上部是装有液体四氧化二氮(N2O4)④的氧化剂箱,下部是装有液体偏二甲肼[(CH3)2NNH2]的燃料箱。
(3)2019年1月3日嫦娥四号探测器成功着陆在月球背面,嫦娥四号探测器主体部分使用的是钛合金⑤等新材料,太空舱中利用NiFeO4⑥和其他物质转化呼出的二氧化碳⑦等废气。
上述短文标有序号的物质中,属于混合物的是
 固体;⑤稀硫酸;⑥
固体;⑤稀硫酸;⑥  ;⑦
;⑦  固体;⑧乙醇;⑨
固体;⑧乙醇;⑨  固体;⑩熔融的
固体;⑩熔融的 。
。(1)能导电的是
(2)属于非电解质的是
(3)既不属于电解质也不属于非电解质的是
(4)写出上述物质中②和⑤反应的离子方程式
(5)请补充完整并配平物质 ①和 ③ 的稀溶液反应的离子方程式:
 +
+(1)常用澄清石灰水检验 CO2 气体,反应的离子方程式是
(2)请配平反应
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
① 用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
② 如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
(4)Fe(OH)3胶体的制备:向沸水中逐滴加入几滴
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
(1)氯气跟水反应生成的次氯酸(
 )具有杀菌作用,常用于自来水的消毒,在次氯酸(HClO)中,氯元素的化合价为
)具有杀菌作用,常用于自来水的消毒,在次氯酸(HClO)中,氯元素的化合价为(2)苹果汁是人们喜爱的饮料,由于此饮料中含有 Fe2+。现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素 C,可有效防止这种现象发生。以上现象说明维生素C具有
(3)自然界中存在的元素大多以化合态存在,而我们在生产和生活中需要许多单质如金属镁、单质溴等。把某元素由化合态变成游离态,则它
A. 被氧化
B. 被还原
C. 可能被氧化,也可能被还原
D. 由高价态变成零价
(4)实验室可用浓盐酸与高锰酸钾反应来制取少量氯气,反应的化学方程式为2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
① 反应中氧化剂与还原剂的个数比为
② 浓盐酸在此反应中所具有的性质是
③用双线桥标出电子转移的方向和数目
2KMnO4 + 16HCl(浓)= 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 氧化还原反应定义、本质及特征 氧化还原反应在生活、生产中的应用 | |
| 2 | 0.94 | 单一分类法 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 3 | 0.85 | 氧化还原反应的几组概念 | |
| 4 | 0.85 | 分类方法的应用 分散系概念及其分类 电解质、非电解质概念 氧化还原反应定义、本质及特征 | |
| 5 | 0.85 | 无机物质的分类 几组常见同素异形体 物质构成的奥秘 | |
| 6 | 0.85 | 氧化还原反应的几组概念 氧化还原反应的规律 | |
| 7 | 0.65 | 氧化还原反应基本概念 氧化还原反应方程式的书写与配平 | |
| 8 | 0.94 | 四种基本反应类型 | |
| 9 | 0.94 | 胶体的定义及分类 胶体的性质和应用 | |
| 10 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 11 | 0.85 | 限定条件下的离子共存 | |
| 12 | 0.85 | 电解质的电离 物质水溶液的导电性 离子反应的实际应用 | |
| 13 | 0.85 | 电解质的电离 非电解质、电解质物质类别判断 电离方程式 | |
| 14 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 15 | 0.85 | 离子反应的发生及书写 离子方程式的书写 | |
| 16 | 0.65 | 离子反应的发生及书写 | |
| 17 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 18 | 0.65 | 离子方程式的书写 离子方程式的正误判断 | |
| 19 | 0.85 | 四种基本反应类型 氧化还原反应的几组概念 硅的制备 | |
| 20 | 0.65 | 与氧化剂、还原剂有关的计算 | |
| 二、填空题 | |||
| 21 | 0.65 | 无机物与有机物 单质和化合物 酸、碱、盐、氧化物的概念及其相互联系 | |
| 22 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 电离方程式 氧化还原反应方程式的配平 | |
| 23 | 0.65 | 离子方程式的书写 氧化还原反应方程式的配平 碳酸氢钠与酸反应 氢氧化铝与强酸反应 | |
| 24 | 0.85 | 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 物质含量的测定 综合实验设计与评价 | |
| 25 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化还原反应的规律 | |



