江苏省南京市第二十九中学2020-2021学年高一上学期期中考试化学试题
江苏
高一
期中
2020-11-19
537次
整体难度:
较易
考查范围:
认识化学科学、化学与STSE、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.云、烟、雾均属于气溶胶 |
| B.可用渗析的方法除去胶体中存在的离子 |
| C.胶体是混合物,可用丁达尔效应来鉴别胶体和溶液 |
| D.PM2.5是对空气中直径小于或等于2.5μm(2.5×10-6m)的固体颗粒或液滴的总称,其分散在空气中一定形成气溶胶 |
【知识点】 分散系概念 胶体 化学科学对人类文明发展的意义解读
| A.水银—Ag | B.胆矾—CuO |
| C.烧碱—NaOH | D.明矾—Al2(SO4)3 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 化学用语综合判断 明矾
| A.还原剂 | B.氧化剂 |
| C.既是氧化剂又是还原剂 | D.以上均不是 |
| A.Cu2(OH)2CO3 是混合物,所以为非电解质 |
| B.该反应中氧、碳元素化合价发生变化,所以是氧化还原反应 |
| C.该反应中 Cu 得电子,O2 失电子,所以是氧化还原反应 |
| D.该反应是氧化还原反应,化合价发生改变的只有两种元素 |
 ∶Fe3+∶K+∶M=2∶3∶1∶3∶1,(不考虑水的电离),则M为
∶Fe3+∶K+∶M=2∶3∶1∶3∶1,(不考虑水的电离),则M为A. | B.Mg2+ | C.Na+ | D.Ba2+ |
【知识点】 离子共存 离子反应的实际应用 限定条件下的离子共存解读
| A.钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| B.钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+ |
| C.钠与盐酸反应:2Na+2H+=2Na++H2↑ |
| D.钠跟氯化钾溶液反应:2Na+2H2O=2Na++2OH-+H2↑ |

| A.装置①中,用手捂住试管,烧杯中出现气泡,放开手后,导管中形成一段稳定的水柱 |
| B.装置②中,向长颈漏斗中加入一定量水,形成水柱,随后水柱下降至与瓶中液面相平的位置 |
| C.装置③中,双手捂住烧瓶,导管中形成一段稳定的水柱,双手放开后,水柱慢慢回落 |
| D.装置④中,将a管向上提至一段高度,a、b两管之间水面形成稳定的高度差 |
| A.“日照澄洲江雾开”,指日光加热使雾的颗粒聚沉 |
| B.过滤和蒸发操作均用到玻璃棒,但玻璃棒的作用不相同 |
C.加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有 CO |
D.先加入稀 HCl 无现象,再加入 BaCl2 溶液产生白色沉淀,证明含大量的 SO |
 Hg+SO2,下列叙述不正确的是( )
Hg+SO2,下列叙述不正确的是( )| A.该反应是置换反应 |
| B.该反应转移 4e-时产生 1 分子 SO2 |
| C.Hg 是还原产物 |
| D.HgS 既是还原剂又是氧化剂 |
【知识点】 四种基本反应类型解读 氧化还原反应的几组概念解读 电子转移计算
| A.Na2O2→Na2CO3 | B.FeCl3→Fe(OH)3 |
| C.BaCl2→Ba(OH)2 | D.CaCO3→CaCl2 |
【知识点】 物质的转化 过氧化钠和二氧化碳反应解读
| A.非金属氧化物都是酸性氧化物 |
| B.碱性氧化物都是金属氧化物 |
| C.酸性氧化物都能与水反应生成酸 |
| D.酸性氧化物都是电解质 |
| A.都比较稳定,密封放置不产生沉淀 | B.都有丁达尔效应 |
| C.加入少量NaOH溶液都可产生沉淀 | D.分散质微粒均可透过滤纸 |
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 澄清石灰水 | 硫酸 | 干冰 |
| B | 冰水混合物 | 酒精溶液 | 硫酸钡 | 二氧化碳 |
| C | 氨水 | 盐酸 | 铜 | 硫酸钡 |
| D | 胆矾 | 食盐水 | 氯化铜 | 氯气 |
| A.A | B.B |
| C.C | D.D |
A. 、 、 、 、 、 、 |
B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 |
D. 、 、 、 、 、 、 |
【知识点】 离子反应的发生条件解读 离子共存 无附加条件的离子共存解读
| A.KMnO4→MnO2 | B.H2O2→O2 | C.SO2→H2S | D.C→CO2 |
| A.2.3g | B.3.1g | C.4.6g | D.5.3g |
| 实验Ⅰ | 实验Ⅱ | |
| 操作 | 将点燃的金属钠伸到盛有CO2的集气瓶中 | 将实验Ⅰ的集气瓶用水冲洗,过滤。取黑色滤渣灼烧;取滤液分别滴加酚酞和氯化钡溶液 |
| 现象 | ①火焰呈黄色 ②底部有黑色固体,瓶壁上附有白色固体 | ①黑色滤渣可燃 ②滤液能使酚酞溶液变红,滴加氯化钡溶液有白色沉淀生成 |
| A.生成的黑色固体中含有C |
| B.白色固体是Na2O |
| C.实验说明CO2具有氧化性 |
| D.金属Na着火不能用CO2灭火 |
| A.2Na+2H2O=2NaOH+H2↑ | B.Cl2+H2O=HCl+HClO |
| C.2F2+2H2O=4HF+O2 | D.SO2+H2O=H2SO3 |
【知识点】 氧化还原反应的几组概念解读 常见氧化剂与还原剂解读
| A.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
| B.碳酸镁溶于硝酸中:2H++CO32-=CO2↑+H2O |
| C.在澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
| D.硫酸氢钠溶液中加入碳酸氢钠溶液:H++HCO3-=CO2↑+H2O |
【知识点】 离子方程式的正误判断解读
| A.含最高价元素的化合物,一定具有强氧化性 |
| B.氧化剂在同一反应中既可以是反应物,也可以是生成物 |
| C.失电子多的还原剂,还原性就强 |
| D.化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
| A.Li2NH中N的化合价为-1价 |
| B.该反应中H2既是氧化剂又是还原剂 |
| C.Li2NH是氧化剂 |
| D.此法储氢和钢瓶储氢的原理相同 |
A | B | C | D |
|
|
|
|
氧化物分类 | 物质分类 | 地壳中元素含量 | 金属的化学性质 |
| A.A | B.B | C.C | D.D |
| A.Ca(OH)2+CO2=CaCO3↓+H2O |
| B.CO2+2Mg=C+2MgO |
| C.2Fe2O3+3C=4Fe+3CO2↑ |
D.C+2H2O 2H2+CO2 2H2+CO2 |
| A.该反应的氧化产物为N2 |
| B.Cl2+H2O=HCl+HClO |
| C.该反应的氧化剂与还原剂微粒个数之比为3:8 |
| D.通过该反应可说明Cl2的氧化性强于N2 |
| A.2.8 g | B.3.0 g | C.7.2 g | D.无法确定 |
二、填空题 添加题型下试题
(1)首先在四支试管中分别滴入
(2)在剩余三支试管中分别滴入
(3)在剩余两支试管中分别滴入
①反应中
②用单线桥标出电子转移方向和数目
③反应产物中,所得氧化产物与还原产物物质的量之比为
三、解答题 添加题型下试题
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a.该反应有氧气生成,且质量为
b.
(2)某探究小组取相同质量过氧化钠粉末,拟用如图所示装置进行实验,以证明上述结论。
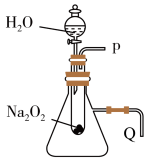
①该反应的离子方程式
②用以验证结论a的实验操作方法及现象是
③用以验证结论b的实验
④向反应后试管中滴加酚酞试液并振荡,现象
(3)经小组讨论认为Na2O2和H2O反应可生成H2O2。
①推测该反应类型为
②请设计简单易行的实验证明Na2O2和足量的H2O充分反应后的溶液中有H2O2存在
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 分散系概念 胶体 化学科学对人类文明发展的意义 | |
| 2 | 0.94 | 酸、碱、盐、氧化物的概念及其相互联系 化学用语综合判断 明矾 | |
| 3 | 0.85 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 | |
| 4 | 0.85 | 物理变化与化学变化 | |
| 5 | 0.85 | 氧化还原反应基本概念 氧化还原反应的定义及实质 氧化还原反应定义、本质及特征 铜绿 | |
| 6 | 0.85 | 离子共存 离子反应的实际应用 限定条件下的离子共存 | |
| 7 | 0.65 | 离子方程式的正误判断 钠与水反应原理 钠与盐溶液的反应 | |
| 8 | 0.65 | 化学实验基础操作 | |
| 9 | 0.85 | 胶体的性质和应用 硫酸根离子的检验 物质分离、提纯的常见物理方法 常见阴离子的检验 | |
| 10 | 0.85 | 四种基本反应类型 氧化还原反应的几组概念 电子转移计算 | |
| 11 | 0.85 | 物质的转化 过氧化钠和二氧化碳反应 | |
| 12 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 | |
| 13 | 0.85 | 分散系概念及其分类 胶体的性质和应用 | |
| 14 | 0.85 | 分类方法的应用 无机物质的分类 电解质与非电解质 非电解质、电解质物质类别判断 | |
| 15 | 0.94 | 离子反应的发生条件 离子共存 无附加条件的离子共存 | |
| 16 | 0.85 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 常见氧化剂与还原剂 | |
| 17 | 0.65 | 钠与水反应原理 氧化钠 | |
| 18 | 0.65 | 钠的化学性质 碱金属发生火灾的处理方法 物质性质实验方案的设计 | |
| 19 | 0.65 | 氧化还原反应的几组概念 常见氧化剂与还原剂 | |
| 20 | 0.85 | 离子方程式的正误判断 | |
| 21 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化性、还原性强弱的比较 | |
| 22 | 0.85 | 氧化还原反应的几组概念 常见氧化剂与还原剂 氧化还原反应在生活、生产中的应用 | |
| 23 | 0.85 | 物质的转化 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 金属元素的存在及分布 | |
| 24 | 0.85 | 氧化还原反应的定义及实质 氧化还原反应的几组概念 常见氧化剂与还原剂 | |
| 25 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 26 | 0.85 | 过氧化钠与水的反应 过氧化钠和二氧化碳反应 过氧化钠的相关计算 | |
| 二、填空题 | |||
| 27 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 物质的检验 物质检验和鉴别的实验方案设计 | |
| 28 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 | |
| 三、解答题 | |||
| 29 | 0.65 | 四种基本反应类型 化学方程式计算中物质的量的运用 过氧化钠与水的反应 物质性质实验方案的设计 | 实验探究题 |







