河北省衡水市武邑武罗学校2020-2021学年高一上学期期中考试化学试题
河北
高一
期中
2021-03-12
326次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础
一、单选题 添加题型下试题
| A.溶液 | B.悬浊液 | C.乳浊液 | D.胶体 |
【知识点】 胶体

A. |
B.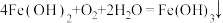 |
C.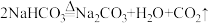 |
D.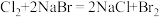 |
【知识点】 四种基本反应类型与氧化还原反应的关系解读
| A.钠溶解,有铁析出并有气体产生 | B.只有气体产生 |
| C.既有气体产生,又有红褐色沉淀产生 | D.只有沉淀产生 |
① 根据碳酸钠溶于水呈碱性,碳酸钠既属于盐,又属于碱。
② 根据反应前后是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液
④ 根据反应中的热效应将化学反应分为放热反应和吸热反应
| A.①③ | B.②④ | C.①④ | D.③④ |
 NaCl+N2↑+2H2O,关于该反应的说法正确的是
NaCl+N2↑+2H2O,关于该反应的说法正确的是| A.NaNO2是氧化剂 | B.生成1个N2时转移的电子为6个 |
| C.NH4Cl中的N元素被还原 | D.N2既是氧化剂又是还原剂 |
【知识点】 氧化还原反应的几组概念解读
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、CO 、CO |
C.Na+、H+、NO 、SO 、SO | D.Fe3+、Na+、Cl-、SO |
【知识点】 离子共存 限定条件下的离子共存解读
①溶液中有气泡产生
②溶液一直呈现红色
③开始时,溶液出现红色,最后红色褪去
④自始至终都未见红色出现
| A.①② | B.②③ | C.③④ | D.②④ |
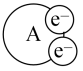 是
是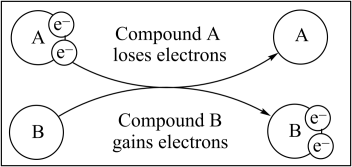
| A.还原剂 | B.氧化剂 | C.氧化产物 | D.还原产物 |
【知识点】 氧化还原反应的几组概念解读

| A.氯化镁固体是非电解质 |
| B.氯化镁溶液是电解质 |
| C.氯化镁在水溶液中电离产生自由移动的离子 |
| D.氯化镁只有在溶液中才能导电 |
①将BaSO4放入水中不能导电,所以BaSO4不是电解质
②氨气溶于水得到的氨水能导电,所以氨水是电解质
③固态共价化合物不导电,熔融态的共价化合物可以导电
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
| A.①④ | B.①④⑤ | C.①②③④⑤ | D.①②③④ |
①
 、
、 、
、 ②
② 、
、 、
、 ③
③ 、
、 、
、 ④
④ 、
、 、
、
| A.②③④ | B.②①④ | C.②③① | D.②①③ |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 电离方程式解读
| A.单质钠与水的反应:Na+H2O=Na++OH-+H2↑ |
B.过量NaHSO4溶液与少量Ba(OH)2溶液反应:H++SO +Ba2++OH-= BaSO4↓+H2O +Ba2++OH-= BaSO4↓+H2O |
C.含等个数的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH +HCO +HCO =BaCO3↓+NH3·H2O+H2O =BaCO3↓+NH3·H2O+H2O |
| D.氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
 +6M,关于该反应的说法正确的组合是
+6M,关于该反应的说法正确的组合是①氧化剂是H3AsO3 ②还原性:Cl->As ③M为OH- ④SnCl
 是氧化产物
是氧化产物| A.①③ | B.①④ | C.①②③ | D.①②④ |
二、多选题 添加题型下试题
| A.Ba(OH)2和盐酸; Ba(OH)2和HNO3 |
| B.BaCl2和Na2SO4; Ba(OH)2和(NH4)2SO4 |
| C.NaHCO3和H2SO4; Ca(HCO3)2和HNO3 |
| D.Ba(OH)2和HNO3; Cu(OH)2和H2SO4 |

| A.甲为Na2CO3,乙为NaHCO3 |
| B.要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球 |
| C.整个实验过程中A烧杯中的澄清石灰水无明显变化 |
| D.加热不久就能看到A烧杯中的澄清石灰水变浑浊 |
【知识点】 碳酸钠与碳酸氢钠性质的比较解读
三、单选题 添加题型下试题
 与S2-在酸性溶液中能发生反应: Mn2O
与S2-在酸性溶液中能发生反应: Mn2O +3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O
+3S2-+14H+=2Mn3++3S↓+7H2O,则Mn2O 中锰元素的化合价是
中锰元素的化合价是| A.+2 | B.+4 | C.+3 | D.+6 |
【知识点】 氧化还原反应方程式的配平解读 氧化还原反应的规律解读
①(m+0.8)g ②(m+1.0)g ③(m+1.2)g ④(m+1.6)g ⑤(m+1.4)g
| A.仅①④ | B.仅①⑤ | C.仅③④ | D.①②③④⑤ |
【知识点】 化学方程式计算中物质的量的运用解读 钠
四、填空题 添加题型下试题

(1)两种物质都是电解质的是
(2)分类标准代号A表示
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:
【知识点】 非电解质、电解质物质类别判断解读 离子方程式的书写解读
五、解答题 添加题型下试题

(1)淡黄色的粉末是
(2)X的名称是
(3)反应I的化学方程式是
(4)反应II的离子方程式是
【知识点】 无机综合推断 过氧化钠和二氧化碳反应解读

(1)在A试管内发生反应的化学方程式是
(2)B装置的作用是
(3)在双球干燥管内发生反应的化学方程式为
(4)双球干燥管内观察到的实验现象是
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是:
六、填空题 添加题型下试题
(1)写出反应的离子方程式
(2)下列三种情况下,离子方程式与题干中相同的是
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至
 恰好完全沉淀
恰好完全沉淀C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流I表示)可近似地用图中的
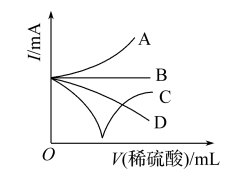
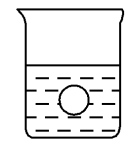
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示。向该烧杯中缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将
(1)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2=2Ag2S+2H2O。还原剂是
(2)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
①上述反应的离子方程式为
②氧化剂与还原剂的个数之比为
(3)已知反应KClO3+6HCl=KCl+3Cl2↑+3H2O
①该反应的离子方程式为
②反应中HCl的作用为
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的应用
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 胶体 | |
| 2 | 0.65 | 四种基本反应类型与氧化还原反应的关系 | |
| 3 | 0.85 | 化学物质的分类方法 无机物质的分类 | |
| 4 | 0.94 | 钠与水反应原理 钠与盐溶液的反应 | |
| 5 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 分散系概念及其分类 氧化还原反应定义、本质及特征 吸热反应和放热反应 | |
| 6 | 0.85 | 氧化还原反应的几组概念 | |
| 7 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 8 | 0.85 | 过氧化钠与水的反应 | |
| 9 | 0.94 | 氧化还原反应的几组概念 | |
| 10 | 0.85 | 电解质与非电解质 | |
| 11 | 0.65 | 电解质与非电解质 电解质的电离 物质水溶液的导电性 综合实验设计与评价 | |
| 12 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 13 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 电离方程式 | |
| 14 | 0.85 | 氧化还原反应的几组概念 常见氧化剂与还原剂 氧化性、还原性强弱的比较 | |
| 15 | 0.65 | 离子方程式的书写 | |
| 16 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应的应用 氧化还原反应的规律 | |
| 19 | 0.85 | 氧化还原反应方程式的配平 氧化还原反应的规律 | |
| 20 | 0.65 | 化学方程式计算中物质的量的运用 钠 | |
| 二、多选题 | |||
| 17 | 0.85 | 离子方程式的书写 | |
| 18 | 0.85 | 碳酸钠与碳酸氢钠性质的比较 | |
| 三、填空题 | |||
| 21 | 0.65 | 非电解质、电解质物质类别判断 离子方程式的书写 | |
| 24 | 0.65 | 物质水溶液的导电性 离子方程式的书写 离子反应的实际应用 | |
| 25 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的应用 | |
| 四、解答题 | |||
| 22 | 0.85 | 无机综合推断 过氧化钠和二氧化碳反应 | 无机推断题 |
| 23 | 0.65 | 过氧化钠和二氧化碳反应 碳酸氢钠的不稳定性 化学实验方案的设计与评价 物质性质实验方案的设计 | 实验探究题 |







