青海省西宁市湟源县第一中学2020-2021学年高一上学期期中考试化学试题
青海
高一
期中
2022-09-22
93次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.铜 | B.食盐水 | C.烧碱 | D.蔗糖 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
| A.0.3mol/L | B.0.04mol/L | C.0.03mol/L | D.0.05mol/L |
【知识点】 物质的量浓度的计算 物质的量浓度与溶液稀释的计算解读
| A.Na2O | B.O2 | C.NaClO | D.FeSO4 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
| A.能电离出H+ 的化合物叫做酸 |
| B.实验测得1mol某气体体积为22.4 L,测定条件一定是标准状况 |
| C.摩尔是七个基本物理量之一 |
| D.化合物分为酸、碱、盐和氧化物是用树状分类法分类的 |
| A.H2S | B.HCl | C.NH3 | D.Cl2 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.KOH | B.H2SO4 | C.BaCl2 | D.Na2CO3 |
【知识点】 离子反应的实际应用
 的物质的量浓度相等的是
的物质的量浓度相等的是| A.10 mL 0.5 mol·L-1 硝酸铜溶液 | B.5 mL 0.8 mol·L-1 硝酸铝溶液 |
| C.10 mL 2 mol·L-1 硝酸银溶液 | D.10 mL 1 mol·L-1 硝酸镁溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.NaOH + HCl = NaCl + H2O |
| B.Zn + 2HCl =ZnCl2 + H2↑ |
C.MnO2 + 4HCl(浓) MnCl2 + 2H2O + Cl2↑ MnCl2 + 2H2O + Cl2↑ |
| D.CuO + 2HCl = CuCl2 + H2O |
【知识点】 氧化还原反应基本概念
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、CO 、CO |
C.Na+、H+、NO 、SO 、SO | D.Fe3+、Na+、Cl-、SO |
【知识点】 离子共存 限定条件下的离子共存解读
| A.1L溶液中含有0.6NA个钾离子 |
| B.1L溶液中含有钾离子和硫酸根离子总数为0.9NA |
| C.2L溶液中钾离子浓度为1.2mol/L |
| D.2L溶液中含有硫酸根离子0.6NA个 |
| A.该反应属于置换反应 | B.氧化性:I2>KClO3 |
| C.还原性:KClO3>I2 | D.还原剂为KIO3,氧化剂为I2 |
| A.稀硫酸滴铜片上:Cu + 2H+ = Cu2+ + H2↑ | B.氧化镁与稀盐酸:MgO + 2H+ = Mg2++ H2O |
| C.铜片与硝酸银溶液:Cu + Ag+ = Cu2+ + Ag | D.铁与稀硫酸 2 Fe + 6H+ = 2Fe3+ + 3H2↑ |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
| A.7.5 mol/L | B.5 mol/L | C.10 mol/L | D.2.5 mol/L |
| A.在氧化还原反应中一定所有元素的化合价都发生变化 |
| B.只有得氧或失氧的化学反应才是氧化还原反应 |
| C.化合反应和分解反应不可能是氧化还原反应 |
| D.氧化还原反应中,被氧化和被还原的可以是同一物质 |
四、未知 添加题型下试题
五、单选题 添加题型下试题
| A.PCl3→PCl5 | B.MnO →Mn2+ →Mn2+ | C.SO3→SO | D.CO2→H2CO3 |
【知识点】 氧化还原反应基本概念
| A.胶体一定是混合物 |
| B.胶体与溶液的本质区别是有丁达尔效应 |
| C.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D.胶体不属于介稳体系 |
| A.2FeCl3+Cu=2FeCl2+CuCl2 |
| B.Cl2+H2O=HCl+HClO |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.CaCO3+2HCl=CaCl2+H2O+CO2↑ |
【知识点】 氧化还原反应基本概念
| A.分子中一定含有氧元素 | B.反应后化合价升高 |
| C.氧化性:氧化剂<氧化产物 | D.在反应中易结合电子的物质 |
【知识点】 氧化还原反应定义、本质及特征解读
| A.3.01×1023 | B.6.02×1023 | C.0.5 | D.1 |
【知识点】 根据n=N/NA的相关计算解读
| A.所用NaOH已经潮解 | B.向容量瓶中加水未到刻度线 |
| C.有少量NaOH溶液残留在烧杯里 | D.定容时仰视刻度线 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
六、填空题 添加题型下试题
【知识点】 酸的通性解读 物质分离、提纯的常见化学方法解读
(1)碳酸钙和盐酸(写出离子方程式)
(2)氢氧化钡溶液和稀硫酸(写出离子方程式)
(3)Fe2(SO4)3(写出电离方程式)
(4)H++OH-=H2O(写出对应的化学方程式)
(5)2Na+2H2O=2NaOH+H2↑(标出双线桥)
【知识点】 离子反应的发生及书写 单线桥、双线桥分析氧化还原反应解读
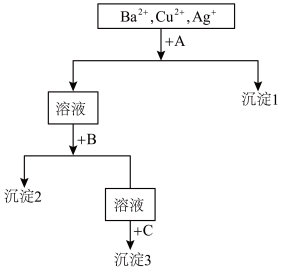
(1)沉淀的化学式:沉淀1
(2)写出混合液+A的离子方程式
【知识点】 离子反应在混合物分离、除杂中的应用解读
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 2 | 0.85 | 物质的量浓度的计算 物质的量浓度与溶液稀释的计算 | |
| 3 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 4 | 0.85 | 离子方程式的书写 | |
| 5 | 0.85 | 树状分类法 物质的量及单位——摩尔 22.4L/mol适用条件 | |
| 6 | 0.94 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 7 | 0.65 | 无机物质的分类 单质和化合物 | |
| 8 | 0.65 | 离子反应的实际应用 | |
| 9 | 0.65 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 11 | 0.94 | 氧化还原反应基本概念 | |
| 12 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 13 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 物质的量浓度计算-与溶质成分有关的计算 | |
| 14 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 15 | 0.85 | 离子方程式的书写 离子方程式的正误判断 | |
| 16 | 0.85 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 17 | 0.85 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 | |
| 19 | 0.65 | 氧化还原反应基本概念 | |
| 20 | 0.65 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 21 | 0.85 | 氧化还原反应基本概念 | |
| 22 | 0.94 | 氧化还原反应定义、本质及特征 | |
| 23 | 0.85 | 根据n=N/NA的相关计算 | |
| 24 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 二、未知 | |||
| 10 | 0.85 | 分散系概念 胶体 分散系概念及其分类 | 未知 |
| 18 | 0.85 | 物质的量浓度的计算 | 未知 |
| 三、填空题 | |||
| 25 | 0.65 | 氧化还原反应的几组概念 | |
| 26 | 0.85 | 根据n=N/NA进行相关计算 结合物质结构基础知识与NA相关推算 | |
| 27 | 0.85 | 物质的量浓度的计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 28 | 0.85 | 酸的通性 物质分离、提纯的常见化学方法 | |
| 29 | 0.65 | 离子反应的发生及书写 单线桥、双线桥分析氧化还原反应 | |
| 30 | 0.85 | 离子反应在混合物分离、除杂中的应用 | |

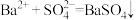 来表示的是
来表示的是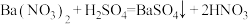
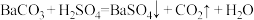
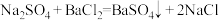
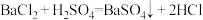
 3Fe+4CO2中,
3Fe+4CO2中,

