2015-2016学年河北省隆化县存瑞中学高一上学期第二次月考化学试卷
河北
高一
阶段练习
2017-07-27
303次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学与STSE、化学反应原理、化学实验基础
一、单选题 添加题型下试题
| A.胶体是纯净物。 |
| B.胶体与溶液的本质区别是有丁达尔效应。 |
| C.Al(OH)3胶体具有很强的吸附能力,能凝聚水中的悬浮物,也能吸附色素,可做净水剂。 |
| D.胶体粒子可以透过半透膜。 |
【知识点】 物质的分类
| A.醋酸 | B.食盐水 | C.烧碱 | D.蔗糖 |
【知识点】 电解质
| A.难溶于水的BaCO3是弱电解质。 |
| B.0.1 mol/L的CH3COOH溶液中H+浓度为0.1 mol/L 。 |
| C.强电解质水溶液的导电能力一定比弱电解质的强。 |
| D.电解质溶液导电的原因是溶液中有自由移动的阴、阳离子。 |
【知识点】 物质的分类
| A.它们相差一个电子层 |
| B.它们的化学性质相似 |
| C.钠原子,钠离子均为同一元素 |
| D.灼烧时,它们的焰色反应都呈黄色 |
| A.KOH | B.H2SO4 | C.BaCl2 | D.Na2CO3 |
【知识点】 离子反应的实际应用
 的物质的量浓度相等的是
的物质的量浓度相等的是| A.10 mL 0.5 mol·L-1 硝酸铜溶液 | B.5 mL 0.8 mol·L-1 硝酸铝溶液 |
| C.10 mL 2 mol·L-1 硝酸银溶液 | D.10 mL 1 mol·L-1 硝酸镁溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
| A.②④⑤③①⑥ | B.③②④①⑤⑥ |
| C.③④②⑤①⑥ | D.②④③⑤①⑥ |
| A.都是白色固体 | B.都是碱性氧化物 |
| C.都能与水反应生成强碱溶液 | D.都是强氧化剂 |
【知识点】 氧化钠 过氧化钠 过氧化钠的物理性质、组成、结构及用途解读
A.2NaCl(熔融) 2Na + Cl2↑ 2Na + Cl2↑ | B.Al2O3 + 3H2 2Al + 3H2O 2Al + 3H2O |
C.Fe2O3+ 3CO  2 Fe + 3CO2 2 Fe + 3CO2 | D.MgCl2 Mg + Cl2↑ Mg + Cl2↑ |
| A.Fe → FeSO4 | B.AgNO3 → Ag | C.S →SO2 | D.CO32-- →CO2 |
【知识点】 氧化还原反应
| A.一定被氧化 | B.一定被还原 |
| C.既可能被氧化又可能被还原 | D.化合价一定升为零价 |
【知识点】 氧化还原反应基本概念
 的化学反应(未配平):
的化学反应(未配平):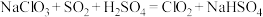 ,下列说法正确的是
,下列说法正确的是A. 在反应中被还原 在反应中被还原 | B. 在反应中失去电子 在反应中失去电子 |
C. 在反应中作氧化剂 在反应中作氧化剂 | D. 氧化剂在反应中得到 氧化剂在反应中得到 电子 电子 |
| A.0.03mol/L | B.0.3mol/L | C.0.05mol/L | D.0.04mol/L |
A. | B. | C. | D. |
| A.稀硫酸滴铜片上:Cu + 2H+ = Cu2+ + H2↑ | B.氧化镁与稀盐酸:MgO + 2H+ = Mg2++ H2O |
| C.铜片与硝酸银溶液:Cu + Ag+ = Cu2+ + Ag | D.铁与稀硫酸 2 Fe + 6H+ = 2Fe3+ + 3H2↑ |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
| A.K+、NO3-、OH-、Cl- | B.Cu2+、SO42-、H+、Na+ |
| C.H+、Ba2+、Mg2+、NO3- | D.NH4+、MnO4-、H+、K+ |
【知识点】 离子共存 限定条件下的离子共存解读
| A.热稳定性:Na2CO3<NaHCO3 |
| B.常温时在水中的溶解度:Na2CO3<NaHCO3 |
| C.等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多 |
| D.等质量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的量:Na2CO3<NaHCO3 |
【知识点】 碳酸钠与碳酸氢钠性质的比较解读
| A.3 mol/L HCl | B.4 mol/L HNO3 | C.8 mol/L NaOH | D.浓H2SO4 |
A.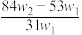 | B.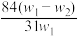 | C. | D.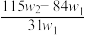 |
【知识点】 碳酸钠、碳酸氢钠混合物的有关求算解读
| A.1:3 | B.3:1 | C.1:2 | D.1:1 |
A. | B.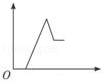 | C. | D. |
| A.200mL | B.250mL | C.500mL | D.无法计算 |
| A.1︰3 | B.9︰8 | C.3︰4 | D.4︰3 |
二、填空题 添加题型下试题
(1)Fe2(SO4)3(写出电离方程式)
(2)向稀硫酸溶液中滴加氢氧化钡溶液至中性(写出离子方程式)
(3)写出实验室制取二氧化碳反应的离子方程式)
(4)鉴别KCl溶液和K2CO3溶液的试剂是
(5)除去Na2CO3粉末中混入的NaHCO3杂质用
【知识点】 弱电解质的电离
三、解答题 添加题型下试题
① A+NaOH=D+H2O ② B=A+H2O ③C+NaOH(适量)="B+NaCl" ④C+D+H2O=B+NaCl
则A是
(2)实验室用加热二氧化锰和浓盐酸制氯气,离子方程式
若生成标况下2.24 L Cl2,则被氧化的HCl的物质的量为
四、填空题 添加题型下试题

(1)图中C点表示当加入
(2)图中线段OA和AB两段NaOH的物质的量之比为
【知识点】 沉淀溶解平衡
五、解答题 添加题型下试题
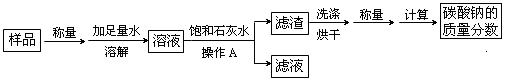
请回答下列问题:
(1)操作A用到的玻璃仪器除烧杯外还必需有
(2)在实验过程中加入饱和石灰水后发生反应的离子方程式是
(3)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现无气泡产生,说明滤液中一定不含
(4)在(3)探究中,滴加盐酸前滤液中的溶质除氯化钠外,一定还含有的溶质是
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 物质的分类 | |
| 2 | 0.64 | 电解质 | |
| 3 | 0.85 | 物质的分类 | |
| 4 | 0.85 | 焰色试验 物质结构与性质综合考查 原子核外电子的排布 核素 | |
| 5 | 0.65 | 离子反应的实际应用 | |
| 6 | 0.65 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 7 | 0.85 | 海水资源综合利用 海水提取镁 | |
| 8 | 0.94 | 氧化钠 过氧化钠 过氧化钠的物理性质、组成、结构及用途 | |
| 9 | 0.65 | 常见金属的冶炼 | |
| 10 | 0.85 | 氧化还原反应 | |
| 11 | 0.64 | 氧化还原反应基本概念 | |
| 12 | 0.85 | 氧化还原反应基本概念 氧化还原反应定义、本质及特征 氧化还原反应的规律 电子转移计算 | |
| 13 | 0.85 | 碳酸钠 碳酸氢钠 | |
| 14 | 0.94 | 物质的量浓度的计算 物质的量浓度的基础计算 物质的量浓度与溶液稀释的计算 | |
| 15 | 0.85 | 离子方程式的书写 | |
| 16 | 0.85 | 铝与强碱溶液反应 氢氧化铝与强碱反应 | |
| 17 | 0.85 | 离子方程式的书写 离子方程式的正误判断 | |
| 18 | 0.85 | 离子共存 限定条件下的离子共存 | |
| 19 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 | |
| 20 | 0.65 | 铝与酸溶液反应 铝与强碱溶液反应 | |
| 21 | 0.65 | 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 22 | 0.85 | 化学方程式计算中物质的量的运用 铝与酸溶液反应 铝与强碱溶液反应 | |
| 23 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 铝盐与强碱溶液反应 | |
| 24 | 0.65 | 镁的结构与化学性质 铝与酸溶液反应 铝盐与强碱溶液反应 | |
| 25 | 0.65 | 化学方程式计算中物质的量的运用 铝与强碱溶液反应 铝热反应 | |
| 二、填空题 | |||
| 26 | 0.85 | 弱电解质的电离 | |
| 28 | 0.85 | 沉淀溶解平衡 | |
| 三、解答题 | |||
| 27 | 0.65 | 氯气 氧化铝 | 无机推断题 |
| 29 | 0.65 | 离子方程式的书写 碳酸钠与盐酸的反应 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 综合实验设计与评价 | 实验探究题 |

 固体中少量
固体中少量 的最佳方法是
的最佳方法是
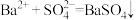 来表示的是
来表示的是