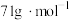河南省汤阴县五一中学2019-2020学年高一下学期期中考试化学试题
河南
高一
期中
2021-03-31
561次
整体难度:
较易
考查范围:
化学实验基础、认识化学科学、化学与STSE
一、单选题 添加题型下试题
| A.摩尔是国际科学界建议采用的一种物理量 |
| B.摩尔是物质的量的单位,简称摩,符号为mol |
| C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来 |
| D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩 |
【知识点】 物质的量及单位——摩尔
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时应将溶液蒸干 |
| D.称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
 及泥砂,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )
及泥砂,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ |
| C.②④⑤①③ | D.⑤②④①③ |
| A.l0g H2和l0g O2 | B.9g H2O和0.5mol Br2 |
| C.224mL H2(标准状况)和0.1mol N2 | D.5.6L N2(标准状况)和22g CO2 |
| A.O2 | B.CH4 | C.CO2 | D.SO2 |
【知识点】 阿伏加德罗定律 根据n=m/M的相关计算解读
| A.质量 | B.原子总数 | C.密度 | D.分子数 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.标准状况下,22.4L H2O含有的分子数为1NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,1NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
| A.所用NaOH已经潮解 |
| B.向容量瓶中加水未到刻度线 |
| C.有少量NaOH溶液残留在烧杯里 |
| D.用带游码的托盘天平称2.4g NaOH时误用了“左码右物”方法 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
| A.自来水 | B.0.5mol·L-1盐酸 |
| C.0.5mol·L-1硫酸 | D.0.5mol·L-1硝酸 |
| A.BaCl2 | B.Ba(OH)2 | C.Na2CO3 | D.KOH |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
A.K+、Na+、NO 、MnO 、MnO | B.Mg2+、Na+、Cl-、SO |
| C.K+、Na+、Br-、Cu2+ | D.Na+、Ba2+、OH-、SO |
【知识点】 限定条件下的离子共存解读
| A.稀硫酸滴在铜片上:Cu + 2H+ = Cu2+ + H2↑ |
| B.氧化镁和稀盐酸混合:MgO +2H+ = Mg2+ + H2O |
| C.铜片插入硝酸银溶液中:Cu + Ag+ = Cu2+ + Ag |
| D.稀盐酸滴在石灰石上:CO32- + 2H+ = H2O + CO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.是否有元素的化合价的变化 |
| B.是否有元素的电子转移 |
| C.是否有氧元素的参加 |
| D.是否有原子的重新组合 |
【知识点】 氧化还原反应基本概念 氧化还原反应定义、本质及特征解读
| A.Fe | B.Br | C.Fe和Br | D.Cl |
【知识点】 氧化还原反应的几组概念解读
① 2H2S + SO2 = 3S↓+ 2H2O
② 2KI + Cl2 = 2KCl + I2
③ 2FeCl2 + Cl2 = 2FeCl3
④ 2FeCl3 + 2HI =2FeCl2 + I2 + 2HCl
⑤ I2 + SO2 + 2H2O = H2SO4+ 2HI
下列有关物质的氧化性的强弱排列顺序中正确的是( )
| A.Cl2 >Fe3+ >I2 >SO2 | B.Cl2 >I2 >Fe3+>SO2 |
| C.Cl2 >Fe3+ >SO2 >I2 | D.Fe3+ >I2 >Cl2 >SO2 |
【知识点】 氧化性、还原性强弱的比较解读
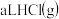 溶于
溶于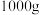 水中,得到的盐酸密度为
水中,得到的盐酸密度为 ,则该盐酸的物质的量浓度(mol/L)是
,则该盐酸的物质的量浓度(mol/L)是
A. | B.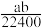 | C.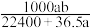 | D. |
二、填空题 添加题型下试题
①用托盘天平称出1.00g氢氧化钠:将天平调好零点,再在两盘上各取一张同样质量的纸,把游码调到1.00g的位置上,于左盘放粒状氢氧化钠至天平平衡,取下称好的氢氧化钠,并撤掉两盘上的纸。
②把称好的氢氧化钠放入一只100mL的烧杯中,加入约10mL水,搅拌使之溶解,溶解后立即用玻璃棒引流将溶液移至一只100mL的容量瓶内,加水至离刻度线约2cm处,用滴管加水至刻度线。
③写出一个标有配制日期的“0.25mol·L-1NaOH溶液”的标签,贴在容量瓶上密闭保存。指出上述操作中的7处错误:
(1)
(3)
(5)
(7)
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用
(2)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用
(3)除去乙醇中溶解的微量食盐可采用
(4)粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。对粗盐中的这些杂质可采用
(5)除去氧化钙中的碳酸钙可用
(1)用稀硫酸清洗铁锈(Fe2O3)
(2)碳酸钠溶液与盐酸混合
(3)硫酸铜溶液和氢氧化钡溶液混合
(4)向足量澄清石灰水中通入二氧化碳
把下列离子方程式改写成化学方程式
(5)CO
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O(6)Ag++Cl-=AgCl↓
(7)Cu2++2OH-=Cu(OH)2↓
(8)SO2十2OH-=SO
 +H2O
+H2O【知识点】 离子反应的发生及书写 离子方程式的书写解读
【知识点】 氧化还原反应的应用
三、计算题 添加题型下试题
(1)用“双线桥法”标出电子转移情况
MnO2 + 4HCl(浓)
 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O(2)理论上需要参加反应的二氧化锰多少
(3)被氧化的HCl的质量为多少
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 仪器使用与实验安全 实验安全 | |
| 2 | 0.85 | 物质的量及单位——摩尔 | |
| 3 | 0.85 | 化学实验基础操作 蒸发与结晶 蒸馏与分馏 萃取和分液 | |
| 4 | 0.85 | 胶体 分散系概念及其分类 | |
| 5 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 海水中盐的开发及利用 | |
| 6 | 0.85 | 萃取和分液 | |
| 7 | 0.65 | 22.4L/mol适用条件 根据n=N/NA进行相关计算 | |
| 8 | 0.85 | 阿伏加德罗定律 根据n=m/M的相关计算 | |
| 9 | 0.85 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 10 | 0.85 | 摩尔质量的概念 气体摩尔体积概念 | |
| 11 | 0.85 | 阿伏加德罗常数的应用 22.4L/mol适用条件 气体物质与NA相关的推算 | |
| 12 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 13 | 0.65 | 物质的量浓度 物质的量浓度的计算 | |
| 14 | 0.65 | 无机物质的分类 单质和化合物 | |
| 15 | 0.94 | 胶体的定义及分类 | |
| 16 | 0.85 | 电解质与非电解质 物质水溶液的导电性 | |
| 17 | 0.85 | 物质水溶液的导电性 | |
| 18 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 19 | 0.85 | 限定条件下的离子共存 | |
| 20 | 0.94 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 21 | 0.85 | 电离方程式 | |
| 22 | 0.85 | 氧化还原反应基本概念 氧化还原反应定义、本质及特征 | |
| 23 | 0.85 | 氧化还原反应的几组概念 | |
| 24 | 0.85 | 氧化性、还原性强弱的比较 | |
| 25 | 0.85 | 22.4L/mol适用条件 依据物质的量浓度公式的基础计算 | |
| 二、填空题 | |||
| 26 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 | |
| 27 | 0.65 | 物质的分离、提纯 物质分离、提纯的常见物理方法 物质分离、提纯综合应用 | |
| 28 | 0.85 | 离子反应的发生及书写 离子方程式的书写 | |
| 29 | 0.85 | 氧化还原反应的应用 | |
| 三、计算题 | |||
| 30 | 0.85 | 单线桥、双线桥分析氧化还原反应 与氧化剂、还原剂有关的计算 | |