安徽省安庆市桐城中学2019-2020学年高一上学期第一次月考化学试题
安徽
高一
阶段练习
2019-10-21
233次
整体难度:
适中
考查范围:
常见无机物及其应用、化学实验基础、认识化学科学、物质结构与性质
一、单选题 添加题型下试题
| A.当有大量毒气泄漏时,人应沿顺风方向疏散 |
| B.实验室里电线失火,首先要断开电源 |
| C.当少量浓硫酸沾在皮肤上,应立即用氢氧化钠溶液冲洗 |
| D.酒精失火用水浇灭 |

| A.蒸馏、蒸发、萃取、过滤 | B.萃取、过滤、蒸馏、蒸发 |
| C.蒸馏、过滤、萃取、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
| 选项 | 异常情况 | 可能原因分析 |
| A | 蒸发结晶:蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到热的蒸发皿底部 |
| B | 分液:分液漏斗中的液体难以滴下 | 没有打开分液漏斗活塞或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
| C | 萃取:液体静置不分层 | 加入萃取剂的量较多 |
| D | 蒸馏:冷凝管破裂 | 冷凝管没有通水或先加热后通水 |
| A.A | B.B | C.C | D.D |
| A.标准状况下,22.4 L氢气完全燃烧,生成H2O分子数为NA |
| B.18 g水中含有的电子数为10 NA |
| C.46 g二氧化氮和46 g四氧化二氮含有的原子数均为3 NA |
| D.在1L 2 mol/L的硝酸镁溶液中含有的离子数为4 NA |
| A.偏二甲肼的摩尔质量为60g |
| B.6.02×1023个偏二甲肼分子的质量约为60g |
| C.1mol偏二甲肼的质量为60g·mol-1 |
| D.6g偏二甲肼含有NA个偏二甲肼分子 |
①该硫原子的相对原子质量为
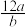 ②mg该硫原子的物质的量为
②mg该硫原子的物质的量为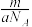 mol
mol③该硫原子的摩尔质量是aNA g ④ag该硫原子所含的电子数为16NA
| A.①③ | B.②④ | C.①② | D.②③ |
【知识点】 阿伏加德罗常数 摩尔质量 物质的量有关计算 几种“相对原子质量”的计算解读
| A.C2H4、CH4 | B.CO2、Cl2 | C.SO2、CO2 | D.CH4、Cl2 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.32 | B.65 | C.140 | D.150 |
【知识点】 物质的量有关计算
| A.2:4:5 | B.1:2:3 | C.1:1:1 | D.2:2:3 |
【知识点】 物质的量有关计算 根据n=m/M的相关计算解读
| A.Ca(OH)2的溶解度 |
| B.溶液中Ca2+的数目 |
| C.溶液中溶质的质量分数 |
| D.溶剂的质量 |
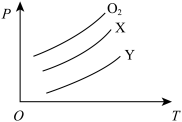
| A.p(H2)=p(O2)=p(N2) | B.p(H2)> p(N2)>p(O2) |
| C.p(O2)> p(N2) > p(H2) | D.p(O2)>p(H2)>p(N2) |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.H2S | B.HCl | C.NH3 | D.Cl2 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.配制盐酸溶液用量筒量取盐酸时量筒必须先润洗 |
| B.配制盐酸溶液时,容量瓶中少量的水不影响最终的浓度 |
| C.定容时观察液面俯视会造成所配溶液浓度偏低 |
| D.浓H2SO4稀释后即可注入容量瓶配制 |
| A.配制500mL该溶液,可将0.1mol BaCl2溶于500mL水中 |
| B.Ba2+和Cl-的物质的量浓度都是0.2mol∙L-1 |
| C.将该瓶溶液稀释一倍,则所得溶液的c(Cl-)为0.2mol∙L-1 |
| D.从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.1mol∙L-1 |
| A.1∶4 | B.1∶5 | C.2∶1 | D.2∶3 |
| A.2w1=w2 | B.w1=2w2 | C.2w1<w2 | D.w1<w2<2w1 |
二、解答题 添加题型下试题
(2)除去KCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式)
(3)下列物质的分离和提纯方法操作为
①粗盐中的泥沙
②油水混合物
③四氯化碳与碘的混合物(回收四氯化碳)
④碘水中的I2
⑤KNO3溶液得到KNO3固体
三、计算题 添加题型下试题
(2)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(3)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(4)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性.实验室可将氧气通过高压放电管来制取臭氧:


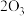
① 若在上述反应中有30 %的氧气转化为臭氧,所得混合气的平均摩尔质量为
 (保留一位小数)
(保留一位小数)②将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为
③实验室将氧气和臭氧的混合气体0.896L (标准状况)通入盛有20.0g铜粉的反应器中,充分加热后(气态全部参加反应),粉末的质量变为21.6g,则原混合气中臭氧的体积分数为
四、解答题 添加题型下试题

供选试剂:Na2SO4溶液、K2SO4溶液、K2CO3溶液、盐酸
(1)操作①的名称是
(2)试剂a是
(3)加入试剂b所发生的化学反应方程式为:
(4)该方案能否达到实验目的:
(5)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是
【知识点】 离子反应的发生及书写 物质的分离、提纯 化学实验基础操作解读 物质含量的测定
(1)应选用的容量瓶规格为:
(2)配制时,在下面的操作中,正确的操作顺序是(用字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
B.准确称量所需的NaCl的质量于烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使固体溶解
C.将冷却后的NaCl溶液注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面最低点恰好与刻度线水平相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(3)配制过程中加蒸馏水不慎超过了刻度,则溶液浓度将
【知识点】 配制一定物质的量浓度溶液的综合考查解读
(1)该“84消毒液”的物质的量浓度为
(2)该同学取100 mL“威露士”牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)一瓶“威露士”牌“84消毒液”能吸收空气中
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480mL含25%NaClO的消毒液。下列说法正确的是

A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143g
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 硫酸物理性质 化学实验基础操作 实验安全 | |
| 2 | 0.94 | 常用仪器及使用 蒸发与结晶 蒸馏与分馏 萃取和分液 | |
| 3 | 0.65 | 仪器使用与实验安全 化学实验基础操作 蒸馏与分馏 萃取和分液 | |
| 4 | 0.65 | 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 5 | 0.65 | 摩尔质量与相对原子质量区别与联系 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 | |
| 6 | 0.85 | 阿伏加德罗常数 摩尔质量 物质的量有关计算 几种“相对原子质量”的计算 | |
| 7 | 0.85 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 8 | 0.65 | 物质的量有关计算 | |
| 9 | 0.65 | 物质的量有关计算 根据n=m/M的相关计算 | |
| 10 | 0.65 | 溶液的含义和组成 溶解度、饱和溶液的概念 结合物质结构基础知识与NA相关推算 | |
| 11 | 0.65 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 12 | 0.94 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 13 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度溶液的综合考查 | |
| 14 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-溶液配制有关计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 15 | 0.65 | 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液配制有关计算 配制一定物质的量浓度溶液的综合考查 | |
| 16 | 0.65 | 物质的量浓度的基础计算 物质的量浓度与溶液混合的计算 基于氨水密度比水小的相关计算及比较 | |
| 二、解答题 | |||
| 17 | 0.65 | 物质的分离、提纯 常用仪器及使用 化学实验基础操作 | 实验探究题 |
| 19 | 0.65 | 离子反应的发生及书写 物质的分离、提纯 化学实验基础操作 物质含量的测定 | 实验探究题 |
| 20 | 0.85 | 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 21 | 0.65 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |
| 三、计算题 | |||
| 18 | 0.65 | 物质的量有关计算 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 | |



