【校级联考】江苏省江阴四校2018-2019学年高一上学期期中考试化学试题
江苏
高一
期中
2018-11-26
328次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、物质结构与性质、常见无机物及其应用、化学与STSE、化学反应原理
一、单选题 添加题型下试题
| A.水和CCl4 | B.碘和酒精 | C.酒精和水 | D.硝酸钾和氯化钾溶液 |
【知识点】 物质分离、提纯的常见物理方法 萃取和分液解读
| A.H2的摩尔质量是2g |
B.氟原子的结构示意图: |
| C.32He和42He互为同位素 |
| D.碳酸钠的电离方程式:Na2CO3═Na2++CO32﹣ |
A.CuO+H2 Cu+H2O Cu+H2O | B.Na2CO3+CO2+H2O=2NaHCO3 |
C.3Fe+2O2 Fe3O4 Fe3O4 | D.NH4HS NH3↑+H2S↑ NH3↑+H2S↑ |

| A.钠在水层中反应并四处游动 |
| B.钠停留在煤油层中不发生反应 |
| C.钠在煤油的液面上反应并四处游动 |
| D.钠在水与煤油的界面处反应并上下跳动 |
 Bi和
Bi和 Bi的说法正确的是( )
Bi的说法正确的是( )A. Bi和 Bi和 Bi都含有83个中子 Bi都含有83个中子 | B. Bi和 Bi和 Bi互为同位素 Bi互为同位素 |
C. Bi和 Bi和 Bi的核外电子数不同 Bi的核外电子数不同 | D. Bi和 Bi和 Bi分别含有126和127个质子 Bi分别含有126和127个质子 |
| A.氨水 | B.二氧化碳气体 | C.铜丝 | D.氢氧化钠固体 |
| A.1mol NH3所含有的原子数为NA |
| B.常温常压下,22.4L氧气所含的原子数为2NA |
| C.常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| D.1 L 0.1mol/LNaCl溶液中所含的Na+ 为NA |
| A.容量瓶使用前必须检查是否漏液 |
| B.蒸发结晶时应将溶液蒸干 |
| C.用一根洁净的铂丝蘸取碳酸钠溶液,置于酒精灯火焰上灼烧可以检验钠离子 |
| D.用洁净的玻璃棒蘸取溶液滴在pH试纸上,跟标准比色卡对照可测定溶液的pH |
| A.CaO+H2O=Ca(OH)2 | B.Cl2+H2O=HCl+HClO |
| C.2Na+2H2O=2NaOH+H2↑ | D.2F2+2H2O=4HF+O2 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读
| A.海水中含有镁元素,只需经过物理变化就可以得到镁单质 |
| B.目前工业上直接由海水提取I2 |
| C.海水蒸发制海盐的过程中只发生了化学变化 |
| D.从海水中可以得到NaCl,电解熔融NaCl可制备Na |
【知识点】 海水资源综合利用 海水中盐的开发及利用解读 海水提取镁解读
A. 溶液 溶液 :加过量 :加过量 溶液,过滤,再加适量盐酸并加热 溶液,过滤,再加适量盐酸并加热 |
B. 溶液 溶液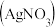 :加过量KCl溶液,过滤 :加过量KCl溶液,过滤 |
C. 溶液 溶液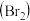 :加 :加 萃取分液 萃取分液 |
D. 溶液 溶液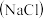 :加热蒸发得浓溶液后,降温,过滤 :加热蒸发得浓溶液后,降温,过滤 |
【知识点】 物质的分离、提纯 物质分离、提纯的常见化学方法解读
| A.① | B.①② | C.②③ | D.①②③ |
【知识点】 以N=m·NA/M为中心的有关基本粒子的推算解读
| A.加入 AgNO3 溶液有大量白色沉淀 |
| B.加入盐酸有无色无味的气体产生 |
| C.加入BaCl2 溶液时有白色沉淀产生,再加入稀盐酸沉淀全部溶解,且产生可以使澄清石灰水变浑浊的无色无味气体 |
| D.加入Ba(OH)2 溶液有白色沉淀产生,再加稀盐酸,沉淀全部溶解,且产生可以使澄清石灰水变浑浊的无色无味气体。 |
【知识点】 离子的检验
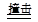 K2O+5Na2O+16N2↑,有关该反应说法正确的是
K2O+5Na2O+16N2↑,有关该反应说法正确的是| A.属于复分解反应 | B.KNO3发生氧化反应 |
| C.NaN3是还原剂 | D.NaN3和KNO3中氮元素化合价均降低 |
| A.150 mL 1 mol•L﹣1的NaCl | B.150 mL 3 mol•L﹣1的KCl |
| C.75 mL 2 mol•L﹣1的NH4Cl | D.75 mL 2 mol•L﹣1的CaCl2 |
| A.分子数 | B.密度 | C.质量 | D.质子数 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.2:1 | B.1:2 | C.3:1 | D.1:3 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算
 ,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是
,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④③① | D.⑤②④①③ |
【知识点】 卤素在自然界的存在解读 物质分离、提纯的常见化学方法解读
 MnCl2+ Cl2↑+2H2O,下列说法不正确的是
MnCl2+ Cl2↑+2H2O,下列说法不正确的是| A.还原剂是HCl,氧化剂是MnO2 |
| B.每有2molHCl被氧化,转移电子的物质的量为2mol |
| C.每消耗1mol MnO2,起还原剂作用的HCl消耗4mol |
| D.转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L |
二、填空题 添加题型下试题
(1)需称量纯碱的质量为
(2)配制溶液时下列仪器中:
A.锥形瓶 B. 托盘天平 C.烧杯 D.胶头滴管 E.药匙
不需要用到的是
(3)人们常将配制过程简述为以下各步骤:
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移 H.装瓶。
其正确的操作顺序应是
①B E A G C G D F H ②B E G A C G F D H
③B E F G C G D H A ④B E A G C G D H F
(4)在此配制过程中,下列情况会使配制结果偏高的是
①纯碱晶体部分失水 ②容量瓶使用时未干燥
③移液时未洗涤烧杯和玻璃棒 ④定容时俯视刻度线观察液面
⑤定容时仰视刻度线观察液面
⑥摇匀后静置,发现液面低于刻度线,再加蒸馏水补至刻度线
【知识点】 一定物质的量浓度的溶液的配制
三、解答题 添加题型下试题

填写下列空白:
(1)写出化学式:A
(2)写出反应⑤的化学反应方程式:
(3)写出反应⑥的化学反应方程式:
四、计算题 添加题型下试题
(1)请写出电解饱和食盐水的化学方程式,若为氧化还原反应则用单线桥标出电子转移的方向和数目
(2)若电解饱和食盐水时消耗NaCl 58.5g,试计算理论上最多可得到氯气的体积(标准状况)为多少
(3)若将1mol氯气通入石灰乳中,理论上可得到Ca(ClO)2的质量是多少
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 无机物与有机物 无机物质的分类 | |
| 2 | 0.85 | 物质分离、提纯的常见物理方法 萃取和分液 | |
| 3 | 0.65 | 化学用语综合判断 原子结构示意图、离子结构示意图 摩尔质量 元素、核素、同位素 | |
| 4 | 0.65 | 氧化还原反应基本概念 四种基本反应类型与氧化还原反应的关系 | |
| 5 | 0.85 | 钠 钠的化学性质 钠单质的保存与用途 钠与水反应原理 | |
| 6 | 0.65 | 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 7 | 0.65 | 电解质与非电解质 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 8 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 某溶液与物质的量浓度相关的物理量的判断 根据n=m/M进行相关计算 | |
| 9 | 0.85 | 焰色试验 仪器使用与实验安全 化学实验基础操作 配制一定物质的量浓度的溶液实验的仪器 | |
| 10 | 0.85 | 电解质的电离 离子反应的实际应用 | |
| 11 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 | |
| 12 | 0.85 | 海水资源综合利用 海水中盐的开发及利用 海水提取镁 | |
| 13 | 0.85 | 电离方程式 | |
| 14 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见化学方法 | |
| 15 | 0.85 | 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 16 | 0.85 | 焰色试验 | |
| 17 | 0.85 | 离子的检验 | |
| 18 | 0.65 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 | |
| 19 | 0.65 | 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度计算-与溶质成分有关的计算 | |
| 20 | 0.65 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 21 | 0.65 | 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 22 | 0.65 | 卤素在自然界的存在 物质分离、提纯的常见化学方法 | |
| 23 | 0.65 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 二、填空题 | |||
| 24 | 0.65 | 一定物质的量浓度的溶液的配制 | |
| 三、解答题 | |||
| 25 | 0.65 | 无机综合推断 钠的化学性质 过氧化钠 碳酸氢钠的不稳定性 | 无机推断题 |
| 四、计算题 | |||
| 26 | 0.65 | 化学方程式计算中物质的量的运用 单线桥、双线桥分析氧化还原反应 氧化还原反应方程式的配平 氯碱工业 | |

 、
、 、
、 、
、 四种离子,已知前三种离子的个数比为3:2:1,则溶液中
四种离子,已知前三种离子的个数比为3:2:1,则溶液中

