辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题
辽宁
高一
期中
2020-12-14
482次
整体难度:
较易
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础、物质结构与性质
辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题
辽宁
高一
期中
2020-12-14
482次
整体难度:
较易
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
容易(0.94)
1. 体检的化验单中,葡萄糖为5.9 mmol/L。表示该体检指标的物理量是
| A.溶解度(S) | B.物质的量浓度(c) | C.物质的量(n) | D.摩尔质量(M) |
【知识点】 物质的量浓度概念、含义解读
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
2. 下列实验操作或事故处理方法正确的是( )
| A.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| B.用水湿润的PH试纸测量某溶液的PH |
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的 ,液体也不能蒸干 ,液体也不能蒸干 |
| D.金属钠着火时,用湿毛巾灭火 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
3. 具备基本化学实验技能是进行科学探究活动的基础和保证。下列试验中所选装置不合理 的是( )
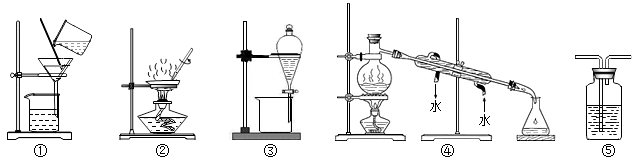

| A.分离Na2CO3溶液和CCl4,选④ | B.分离花生油和水,选③ |
| C.用NaOH溶液吸收除去N2中的少量CO2,选⑤ | D.粗盐提纯,选①和② |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
4. 下列有关胶体的叙述正确的是( )
| A.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| B.“血液透析”利用了胶体的性质 |
| C.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-7~10-5 m之间 |
| D.常温下,将氯化铁稀溶液滴加到蒸馏水中就可制得氢氧化铁胶体 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
5. 若NA表示阿伏加德罗常数,下列说法中,正确的是
| A.1 mol Cl2作为氧化剂得到的电子数为NA |
| B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C.25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3 NA |
| D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4 |
您最近一年使用:0次
2016-12-09更新
|
156次组卷
|
5卷引用:2015-2016学年内蒙古包头九中高一上12月月考化学试卷
单选题
|
较易(0.85)
解题方法
6. 下列表示对应化学反应的离子方程式正确的是
| A.稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| B.氢氧化钡与盐酸:Ba(OH)2+2H+=Ba2++2H2O |
C.硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-=Cu(OH)2↓+ |
D.碳酸氢钠溶液与硫酸混合: +H+= H2O+CO2↑ +H+= H2O+CO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
您最近一年使用:0次
单选题
|
较易(0.85)
名校
7. 在同温同压下,容器甲中盛有H2,容器乙盛有NH3,若使它们所含的原子总数相等,则这两个容器的体积之比是( )
| A.2:1 | B.1:2 | C.2:3 | D.1:3 |
【知识点】 阿伏加德罗定律的应用解读
您最近一年使用:0次
2020-04-18更新
|
175次组卷
|
14卷引用:2012-2013学年江西省四校高一零班第一次月考化学试卷
(已下线)2012-2013学年江西省四校高一零班第一次月考化学试卷2014-2015四川省雅安中学高一上学期期末化学试卷河北省鸡泽县第一中学2016-2017学年高二下学期期末考试化学试题云南省腾冲市第八中学2017-2018学年高一上学期期末考试化学试题(已下线)2018年9月9日 《每日一题》人教必修1-每周一测天津市武清区杨村第三中学2018-2019学年高一上学期第一次月考化学试题【全国百强校】辽宁省实验中学2018-2019学年高一上学期期中考试化学试题云南省腾冲市第八中学2018-2019学年高一下学期开学考试化学试题甘肃省靖远县第二中学2018-2019学年高一下学期开学考试化学试题山东省新泰二中2019-2020学年高一上学期第一次月考化学试题(已下线)【南昌新东方】2019 新建一中 高一上 期中黑龙江省牡丹江市海林林业局第一中学2019-2020学年高二下学期第一次月考化学试题(已下线)2.3.2 气体摩尔体积-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题
单选题
|
容易(0.94)
解题方法
8. 下列说法正确的是( )
| A.金属氧化物均是碱性氧化物 |
| B.烧碱、冰醋酸、四氯化碳均是电解质 |
| C.干冰、白磷、碘酒分别属于化合物、单质、混合物 |
| D.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均为离子化合物 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
9. 下列各组离子能在溶液中大量共存的是
A.Ag+、K+、 、Cl- 、Cl- | B.Mg2+、Na+、Cl-、 |
| C.Ca2+、Mg2+、OH-、Cl- | D.H+、Na+、 、 、 |
【知识点】 无附加条件的离子共存解读
您最近一年使用:0次
2020-10-18更新
|
175次组卷
|
7卷引用:安徽省安庆市宜秀区白泽湖中学2020-2021学年高一上学期第一次月考化学试题
单选题
|
容易(0.94)
名校
解题方法
10. 下列离子方程式中,只能表示一个化学反应的是( )
①Fe+Cu2+ = Fe2++Cu
②Ba2++2OH-+2H++ =BaSO4↓+2H2O
=BaSO4↓+2H2O
③Cl2+H2O = H++Cl-+HClO
④CaCO3+2H+ = CO2↑+H2O +Ca2+
⑤H++OH- = H2O
①Fe+Cu2+ = Fe2++Cu
②Ba2++2OH-+2H++
 =BaSO4↓+2H2O
=BaSO4↓+2H2O③Cl2+H2O = H++Cl-+HClO
④CaCO3+2H+ = CO2↑+H2O +Ca2+
⑤H++OH- = H2O
| A.只有③ | B.②③ | C.③⑤ | D.①④ |
【知识点】 离子反应的发生及书写 离子反应的发生条件解读 离子方程式的书写解读
您最近一年使用:0次
2020-12-03更新
|
127次组卷
|
2卷引用:辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题
11. 对于反应O3+I-+H+→I2+O2+H2O(未配平),下列说法正确的是( )
| A.O2和H2O是还原产物 |
| B.该反应能说明O2氧化性大于I2 |
| C.氧化产物与还原产物的物质的量之比是1∶1 |
| D.配平后的化学方程式为:2O3 + 2I-+ 4H+ = I2+ 2O2+ 2H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
12. 用48mL0.1mol/L的FeSO4溶液,恰好还原2.4×10-3mol [RO(OH)2]+,Fe2+被氧化为Fe3+,则R元素的最终价态为( )
| A.+2价 | B.+3价 | C.+4价 | D.+5价 |
【知识点】 基于氧化还原反应守恒规律的计算解读
您最近一年使用:0次
2019-12-13更新
|
225次组卷
|
7卷引用:【校级联考】江西省上饶市铅山县第一中学2019届高三上学期第一次三校联考化学试题
单选题
|
较易(0.85)
解题方法
13. 下列属于电解质并能导电的物质是
| A.熔融的NaCl | B.KNO3溶液 | C.Na | D.酒精 |
您最近一年使用:0次
2016-12-09更新
|
1093次组卷
|
5卷引用:2010年浙江省嘉兴一中高一上学期10月月考化学试题
(已下线)2010年浙江省嘉兴一中高一上学期10月月考化学试题(已下线)2010—2011学年江苏省淮安五校高一上学期期末考试化学试卷2014-2015福建省福州市八中高一上学期期中化学试卷辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题福建省泉州市永春美岭中学2022-2023学年高一上学期第一次月考化学试题
单选题
|
较易(0.85)
解题方法
14. 下列反应中,既是化合反应,又是氧化还原反应的是( )
(1)铁和氯气反应 2Fe+3Cl2=2FeCl3
(2)氯气通入溴化钠溶液Cl2+2NaBr=2NaCl+Br2
(3)氯化钠溶液和浓硫酸混合加热2NaCl+H2SO4(浓)=Na2SO4+2HCl↑
(4)二氧化锰跟浓盐酸在加热条件下反应 MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(5)氢气在氯气中燃烧 H2+Cl2=2HCl
(1)铁和氯气反应 2Fe+3Cl2=2FeCl3
(2)氯气通入溴化钠溶液Cl2+2NaBr=2NaCl+Br2
(3)氯化钠溶液和浓硫酸混合加热2NaCl+H2SO4(浓)=Na2SO4+2HCl↑
(4)二氧化锰跟浓盐酸在加热条件下反应 MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(5)氢气在氯气中燃烧 H2+Cl2=2HCl
| A.(1)(2) | B.(1)(3) | C.(1)(4) | D.(1)(5) |
您最近一年使用:0次
2020-10-31更新
|
93次组卷
|
2卷引用:云南省保山市第九中学2020-2021学年高一上学期10月阶段性测试化学试题
二、未知 添加题型下试题
三、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
您最近一年使用:0次
2021-10-23更新
|
3851次组卷
|
122卷引用:2010年四川省成都九中高一上学期期中考试化学试卷
(已下线)2010年四川省成都九中高一上学期期中考试化学试卷(已下线)2010年江西省德兴市四校联考高一上学期期中考试化学试卷(已下线)2010年浙江省嘉兴一中高一12月月考题化学试卷(已下线)2010年青海省青海师大附中高一上学期期中考试化学试卷(已下线)2010年安徽省泗县双语中学高一上学期第三次月考化学试卷(已下线)2010年江苏省海安县南莫中学高一上学期期中考试化学试卷(已下线)2011-2012年福建省福州市罗源一中高一上学期第一次月考化学试卷(已下线)2011-2012学年黑龙江省哈三中高一上学期期中考试化学试卷(已下线)2011-2012学年安徽师大附中高一第一学期期中考查化学试卷(已下线)2011-2012学年甘肃省兰州市兰炼一中高一上学期期中考试化学试卷(已下线)2011-2012学年江西省上高二中高一上学期第二次月考化学试卷(已下线)2012届湖南省四市九校高三上学期第一次联考化学试卷(已下线)2011-2012学年贵州省凯里一中高一上学期期中考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一上学期期末考试化学试卷(已下线)2011-2012学年北京市师大附中高一上学期期中考试化学试卷(已下线)2011-2012学年山东济南平阴一中高一上学期期末检测化学试卷(已下线)2012-2013学年云南省芒市中学高一上学期期中考试化学试卷(已下线)2012-2013学年江西省赣州市十一县(市)高一上学期期中联考化学试卷(已下线)2013-2014学年海南省三亚市一中高一上学期期中考试化学试卷(A)(已下线)2013-2014学年安徽省宿州市高一上学期期末考试化学试卷(已下线)2013-2014学年河南省驻马店市高一上学期四校联考化学试卷(已下线)2014-2015学年浙江省杭州市西湖高级中学高一10月月考化学试卷(已下线)2014-2015学年甘肃省民乐县第一中学高一上学期第一次月考化学试卷(已下线)2014-2015浙江省宁波市效实中学高一上学期期中化学试卷2014-2015学年辽宁省朝阳县柳城高中高一上学期期中化学试卷2014-2015湖南省边城高级中学高一上学期期中考试化学试卷2015-2016学年湖北省宜昌部分示范高中高一上期中测试化学试卷2015-2016学年河北成安一中、永年二中高一上期中联考化学试卷2015-2016学年吉林省扶余市第一中学高一上学期期中测试化学试卷2015-2016学年陕西省西安第七十中学高一上学期期中测试化学试卷2015-2016学年浙江省台州市书生中学高一上学期第一次月考化学试卷2015-2016学年吉林省吉林一中高一上11月月考化学试卷2015-2016学年吉林省吉林一中高二上11月月考化学试卷12015-2016学年浙江省慈溪市高一上学期期中联考化学试卷2015-2016学年江西省九江一中高一上期末考试化学试卷2015-2016学年湖北省黄冈市高一上学期期末考试化学试卷2017届陕西省安康市石泉中学高三上学期第一次月考化学试卷2016-2017学年福建省霞浦一中高一上学期第一次月考化学试卷2016-2017学年山西省怀仁一中高一上期中化学试卷2016-2017学年天津市红桥区高一上学期期中化学试卷2016-2017学年陕西西藏民族学院附中高一上期中化学卷2016-2017学年河北省冀州中学高一上11月月考化学卷2016-2017学年辽宁省实验中学分校高一上期中化学卷2016-2017学年河北省石家庄市第一中学高一上学期期末考试化学试卷河南省林州市第一中学2017-2018学年高一(火箭班)10月调研化学试题吉林省长春外国语学校2017-2018学年高一上学期期中考试化学试题辽宁省辽河油田第二高级中学2017-2018学年高一上学期第一次月考化学试题新疆生产建设兵团第二中学2017-2018学年高一上学期期中考试化学试题山西省康杰中学2017-2018学年高一上学期期中考试化学试题广东省实验中学2017-2018学年高一上学期期中考试化学试题贵州省遵义航天高级中学2017-2018学年高一上学期第三次月考理综化学试题宁夏银川九中2017-2018学年高一上学期期中考试化学试题湖南省常宁一中2017-2018学年高一下学期期末考试化学试题河南省灵宝三高2017-2018学年高一上学期第三次质量检测化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高一上学期第一次月考化学试题【全国百强校】贵州省铜仁市第一中学2019届高三上学期第二次月考化学试题陕西省西安市远东第一中学2019届高三上学期10月月考化学试题吉林省长白山第二中学2018-2019学年高一上学期期中考试化学试题河北省张家口市2017-2018学年高一上学期期末考试化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高一上学期期中考试化学试题【全国百强校】内蒙古鄂尔多斯市第一中学2018-2019学年高一上学期期中考试化学试题【校级联考】江苏省江阴四校2018-2019学年高一上学期期中考试化学试题广东省广州市中山大学附属中学2018-2019学年高一第一学期期中考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一上学期第二次月考化学试题河北省邢台市第八中学2017-2018学年高一上学期期末考试化学试题山西省应县第一中学校2018-2019学年高二下学期期末考试化学试题江西省南康中学2017-2018学年高一上学期期中考试化学试题内蒙古额市一中2019-2020学年高一第一学期期中化学试题福建省泉州市泉港区第一中学2019-2020学高一上学期第一次月考化学试题云南省昭通市巧家县二中2019-2020学年高一10月月考化学试题广东第二师范学院番禺附属中学2019-2020学年高一上学期中考试化学试题河南省鹤壁市高级中学2019-2020学年高一11月月考化学试题(已下线)【新东方】高中化学5031黑龙江省海林市朝鲜族中学2019-2020学年高一上学期期中考试化学试题黑龙江省哈尔滨市阿城区龙涤中学2019-2020学年高一上学期第一次段考化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高一上学期期中考试化学试题(已下线)广东省深圳市深圳中学2019-2020学年高一上学期期中考试化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题1(已下线)【新东方】2019新中心五地106高中化学吉林省梅河口市博文学校2019-2020学年高一上学期第二次月考化学试题云南省福贡县第一中学2019-2020学年高一上学期期末考试化学试题云南省丽江市华坪县第一中学2019—2020学年高一上学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解中三大守恒的应用(强化练习)贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题陕西省吴起高级中学2019-2020学年高二下学期第一次质量检测化学试题(已下线)【南昌新东方】江西省九江一中2015-2016学年高一上学期期末化学试题甘肃省灵台县第一中学2019-2020学年高一上学期期中考试化学试题(已下线)期中模拟卷(一)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)人教版(2019)高一必修第一册 第一章 物质及其变化 章末综合检测卷黑龙江省双鸭山市第一中学2020-2021学年高一10月月考化学试题黑龙江省绥化市明水县第一中学2020-2021学年高一上学期第一次月考化学试题(已下线)【浙江新东方】1北京市铁路第二中学2020-2021学年高一上学期期中考试化学试题辽宁省大石桥市第三高级中学2020-2021学年高一上学期期中考试化学试题辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP423】【化学】(已下线)【浙江新东方】81.青海省西宁市2020-2021学年高一上学期期末调研测试化学试题福建省福州市闽江口联盟校2020-2021学年高一上学期期中联考化学试题江西省南昌市八一中学、洪都中学等七校2020-2021学年高一上学期期末联考化学试题安徽省滁州市明光中学2020-2021学年高一下学期开学考试化学试题甘肃省天水市一中2020-2021学年高一下学期开学考试化学试题重庆市南坪中学2020-2021学年高一上学期期中考试化学试题安徽省安庆桐城市第八中学2020-2021学年高一上学期第一次段考化学试题江苏省南京市外国语学校2020-2021学年高一上学期化学10月月考化学试卷黑龙江省齐齐哈尔市第二十四中学2021-2022学年高一上学期第一次月考化学试题山西省大同市平城中学校2021-2022学年高一上学期10月月考化学试题内蒙古包头市一机一中2021-2022学年高一上学期10月月考化学试题黑龙江省绥化市望奎县第一中学2021-2022学年高一上学期第一次月考化学试题陕西省咸阳市泾阳县2021-2022学年高一上学期期中考试化学试题广东省中山市第一中学2021-2022学年高一上学期第二次统测化学试题河北省石家庄市第十八中学2021-2022学年高一上学期期中考试化学试题北京市东直门中学2021-2022学年高一上学期期中考试化学试题湖南省常德市鼎城区第一中学2021-2022学年高一上学期12月月考化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题湖南省娄底市第四中学2021-2022学年高一下学期第一次月考化学试题广东省东莞市东华高级中学、东华松山湖高级中学2022-2023学年高一上学期10月联考化学试题江西省丰城市2023-2024学年高三上学期9月月考化学试题天津市滨海新区田家炳中学2023-2024学年高一上学期期中考试化学试题四川省达州外国语学校2023-2024学年高一上学期11月月考化学试题
单选题
|
较易(0.85)
名校
解题方法
17. 由锌、铁、铝、镁4种金属中的两种组成的混合物10g,与足量的盐酸反应,产生的氢气在标准状况下的体积为11.2L,则混合物中一定含有的金属是
| A.锌 | B.铁 | C.铝 | D.镁 |
您最近一年使用:0次
2020-11-18更新
|
1575次组卷
|
61卷引用:江苏省2011届高三化学一轮过关测试(5)
(已下线)江苏省2011届高三化学一轮过关测试(5)(已下线)江苏省2011届高三化学一轮过关测试(12)(已下线)2010年湖北省孝感高中高一上学期期中考试化学试卷(已下线)2010年浙江省绍兴一中高一上学期期中考试化学试题(已下线)2010—2011学年黑龙江省大庆中学高一上学期期末考试化学试卷(已下线)2011-2012学年上海市崇明中学高二上学期期中考试化学试卷(已下线)2011-2012学年上海市吴淞中学高一上学期期中考试化学试卷(已下线)2011-2012学年浙江省瑞安中学高一上学期期中考试化学试卷(已下线)2011-2012学年天津市蓟县一中高一第二次月考化学试卷(已下线)2011-2012学年江西省赣州市信丰县信丰中学高一第二次月考化学试卷(已下线)2014届安徽省马鞍山二中高三上学期期中考试化学试卷(已下线)2014届湖南省长郡中学高三第二次月考化学试卷2014-2015宁夏回族自治区银川一中高一上学期期末考试化学试卷2016届山东省乳山市第一中学高三上学期10月月考化学试卷2015-2016学年河北省唐山一中高一上第一次月考化学试卷2015-2016学年黑龙江省哈尔滨六中高一上期末化学试卷2015-2016学年江西省上高二中高一上学期期末化学试卷2015-2016学年湖南省湘潭一中等四校高一上学期第三次联考化学试卷2016-2017学年甘肃省嘉峪关市酒钢三中高一上学期期末考试化学试卷湖北省华中师范大学第一附属中学2016-2017学年高一下学期期中考试(文)化学试题河北省衡水市安平中学2017-2018学年高一上学期第三次月考化学试题1河北省邢台市第一中学2017-2018学年高一上学期第三次月考化学试题重庆市西北狼联盟2017-2018学年高一上学期第一次联盟考试(12月)化学试题黑龙江省大庆铁人中学2017-2018学年高一上学期阶段性考试化学试题贵州省遵义市第四中学2017-2018学年高一上学期第二次月考化学试题甘肃省武威市第一中学2017-2018学年高一上学期期末考试化学试题(已下线)黄金30题系列 高一化学 小题好拿分【提升版】河南省灵宝三高2017-2018学年高一上学期第三次质量检测化学试题【校级联考】浙江省温州市“十五校联合体”2018-2019学年高一上学期期中联考化学试题【全国百强校】湖北省孝感市高级中学2018-2019学年高一上学期期中考试化学试题【全国百强校】宁夏回族自治区银川一中2018-2019学年高一上学期12月阶段性测试化学试题上海市华东师大二附中2016-2017学年高二(上)月考化学试卷(10月份)吉林省长春市吉林省实验中学2019-2020学年高一上学期期中考试化学试题黑龙江省安达市第七中学2019-2020学年高一上学期月考化学试题吉林省大安市第一中学2020届高三第二次月考化学试题江西省南昌市新建区第一中学2019-2020学年高一上学期第二次月考(共建部)化学试题(已下线)上海市华师大二附中2016-2017学年高二(上)第一次月考化学试卷新疆维吾尔自治区阿勒泰地区2019-2020学年高二下学期期末考试化学试题(B卷)人教版(2019)高一必修第一册 第三章 铁 金属材料 第二节 金属材料 方法帮(已下线)【新东方】【2019】【高一上】【期中考】【JYZ】【化学】河南省漯河市临颍县南街高级中学2020-2021学年高一10月质量检测化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)第三章 金属及其化合物(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)3.1.2 金属与酸和水的反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)黑龙江省肇东市第四中学校2021届高三上学期期中考试化学试题(已下线)【浙江新东方】双师 (16)(已下线)【南昌新东方】9. 2020 高一上 铁路一中 刘惠文 钟欣辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题(已下线)3.2.2 物质的量在化学方程式计算中的应用(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)3.2.2 物质的量在化学方程式计算中的应用(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)上海市奉城高级中学2019-2020学年高二上学期期中考试化学试题江苏省启东中学2020-2021学年高一上学期第二次月考化学试题黑龙江嫩江市高级中学2020-2021学年高一上学期第一次月考化学试题吉林省松原市长岭县第三中学2020-2021学年高一上学期期末考试化学试题吉林省四平市公主岭市范家屯镇第一中学2020-2021学年高一上学期期末联考化学试题(已下线)2.2.3 化学反应的计算(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)湖南省长沙市第一中学2019-2020学年高一上学期第二次阶段性检测(月考)化学试题宁夏银川一中2021-2022学年高一上学期期末考试化学试题上海市曹杨中学2021-2022学年高一上学期期中考试化学试题浙江省东阳市横店高级中学2021-2022学年高一下学期开学考试检测化学试题河南省驻马店市新蔡县第一高级中学2022-2023学年高三上学期11月月考化学试题
单选题
|
较易(0.85)
解题方法
18. 用质量分数为ω的浓盐酸(其密度为ρ1 g﹒cm-3),按浓盐酸与水的体积比为1﹕3配制成稀盐酸(其密度为ρ2 g﹒cm-3),则所配制稀盐酸的物质的量浓度为
A.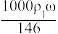 mol/L mol/L | B.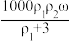 mol/L mol/L |
C.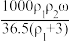 mol/L mol/L | D.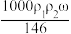 mol/L mol/L |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
19. 下列反应中必须加入还原剂才能进行的是
| A.Fe2+→Fe | B.Zn→Zn2+ | C.H2→H2O | D.CuO→CuCl2 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
20. 某气体的摩尔质量为M g·mol-1,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为x。则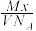 表示的是( )
表示的是( )
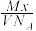 表示的是( )
表示的是( )| A.V L该气体的质量(以g为单位) |
| B.1 L该气体的质量(以g为单位) |
| C.1 mol该气体的体积(以L为单位) |
| D.1 L该气体中所含的分子数 |
您最近一年使用:0次
2016-11-01更新
|
329次组卷
|
19卷引用:2014届湖北省黄冈中学、黄石二中、鄂州高中高三11月联考化学试卷
(已下线)2014届湖北省黄冈中学、黄石二中、鄂州高中高三11月联考化学试卷(已下线)2014高考名师推荐化学NA与粒子(已下线)2014-2015学年辽宁省沈阳二中高一上学期10月月考化学试卷(已下线)2014-2015浙江省宁波市效实中学高一上学期期中化学试卷2015-2016学年重庆巴蜀中学高一上10月月考化学试卷2016届吉林省东北师大附属中学高三上第二次模拟化学试卷2015-2016学年河北石家庄一中高一下学情反馈一化学卷2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷2016届内蒙古集宁一中高三上第一次月考化学试卷2016-2017学年天津市静海一中高一上9月调研化学试卷2016-2017学年江西省南昌二中高一上月考一化学试卷吉林省白城市第一中学2018-2019学年高一上学期第一次月考化学试题河南省辉县市一中2018-2019学年高一上学期第一次阶段性考试化学试题(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第1讲 物质的量 气体摩尔体积 (教学案)(已下线)2019年7月7日 《每日一题》 2020年高考一轮复习-每周一测吉林省吉林市第五十五中学2018-2019学年高二下学期期末考试化学试题辽宁省沈阳市第二十八中学2020-2021学年高一上学期期中考试化学试题(已下线)衔接点19 气体摩尔体积-2022年初升高化学无忧衔接?上海市大同中学2020-2021学年高一上学期期中考试化学试题
四、填空题 添加题型下试题
21. 高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。已知制取高铁酸钠的化学方程式为:2Fe(NO3)3 + 16NaOH + 3Cl2 = 2Na2FeO4+6NaNO3+ 6NaCl + 8H2O,回答下列问题:
(1)该反应中__________ 得到电子,表现_________ (填“氧化性”或“还原性” ),Na2FeO4为______________ (填“氧化剂”、“还原剂”、“氧化产物”或 “还原产物” )。
(2)若有1 mol Cl2参加反应,则反应中转移电子的物质的量为______________ 。
(1)该反应中
(2)若有1 mol Cl2参加反应,则反应中转移电子的物质的量为
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算 高铁酸钠解读
您最近一年使用:0次
五、解答题 添加题型下试题
解答题-实验探究题
|
较易(0.85)
解题方法
22. 现用18.4 mol/L的浓H2SO4来配制500 mL 0.2 mol/L的稀H2SO4,可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平 ⑦药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时不需要使用的有___________ (填代号),还缺少的仪器是______________________ 。
(2)经计算,需浓H2SO4的体积为___________ ,量取浓硫酸时应选用___________ (选填①10 mL、②50 mL、③100 mL三种规格)的量筒。
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。请你分析配制过程中,引起浓度偏高的可能原因有___________
A.定容时,液面低于刻度线
B.未用蒸馏水洗涤实验时用的烧杯
C.量取浓硫酸时仰视读数
D.未冷却到室温就定容
(1)上述仪器中,在配制稀H2SO4时不需要使用的有
(2)经计算,需浓H2SO4的体积为
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。请你分析配制过程中,引起浓度偏高的可能原因有
A.定容时,液面低于刻度线
B.未用蒸馏水洗涤实验时用的烧杯
C.量取浓硫酸时仰视读数
D.未冷却到室温就定容
您最近一年使用:0次
六、填空题 添加题型下试题
填空题
|
较易(0.85)
解题方法
23. 常温下,某学生从一种强酸性的未知无色溶液中检出Ag+,他还想通过实验检验溶液中是否含有大量的 、Cl-、
、Cl-、 、Cu2+、Fe3+、K+等。
、Cu2+、Fe3+、K+等。
(1)你认为其中____________ 是需要检验的;而___________ 是不需要检验的(填离子符号);
(2)其原因是______________________________________________ 。(写出相关的所有离子方程式及文字说明)
 、Cl-、
、Cl-、 、Cu2+、Fe3+、K+等。
、Cu2+、Fe3+、K+等。(1)你认为其中
(2)其原因是
您最近一年使用:0次
七、计算题 添加题型下试题
计算题
|
较易(0.85)
解题方法
24. 常温下,在27.9 g水中溶解12.1 g Cu(NO3)2·3H2O,恰好达到饱和,设该溶液密度为1.20 g/cm3,(写出计算过程)求:
(1)该溶液中Cu(NO3)2的物质的量为___________ ;
(2)溶液的体积是________ mL;
(3)该溶液中Cu(NO3)2的物质的量浓度是_________ 。
(1)该溶液中Cu(NO3)2的物质的量为
(2)溶液的体积是
(3)该溶液中Cu(NO3)2的物质的量浓度是
您最近一年使用:0次
试卷分析
整体难度:较易
考查范围:认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础、物质结构与性质
试卷题型(共 24题)
题型
数量
单选题
19
未知
1
填空题
2
解答题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 物质的量浓度概念、含义 | |
| 2 | 0.94 | 二氧化硅的化学性质 钠与水反应原理 测定溶液pH的方法 仪器使用与实验安全 | |
| 3 | 0.85 | 物质的分离、提纯 萃取和分液 过滤 | |
| 4 | 0.94 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 5 | 0.85 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 6 | 0.85 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 7 | 0.85 | 阿伏加德罗定律的应用 | |
| 8 | 0.94 | 单质和化合物 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 化学键与物质类别关系的判断 | |
| 9 | 0.85 | 无附加条件的离子共存 | |
| 10 | 0.94 | 离子反应的发生及书写 离子反应的发生条件 离子方程式的书写 | |
| 11 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应方程式的配平 氧化还原反应的规律 | |
| 12 | 0.65 | 基于氧化还原反应守恒规律的计算 | |
| 13 | 0.85 | 电解质的电离 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 14 | 0.85 | 四种基本反应类型 氧化还原反应的应用 氧化还原反应的规律 | |
| 16 | 0.85 | 电解质的电离 离子反应的实际应用 | |
| 17 | 0.85 | 化学方程式中物质的量的运用 铝与酸溶液反应 铁与非氧化性酸的反应 | |
| 18 | 0.85 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 19 | 0.94 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化还原反应的规律 | |
| 20 | 0.85 | 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 二、未知 | |||
| 15 | 0.65 | 常见氧化剂与还原剂 氧化性、还原性强弱的比较 氧化还原反应的规律 Fe2+的还原性 | 未知 |
| 三、填空题 | |||
| 21 | 0.85 | 氧化还原反应基本概念 氧化还原反应有关计算 高铁酸钠 | |
| 23 | 0.85 | 限定条件下的离子共存 离子反应在化合物组成的分析、鉴定的应用 | |
| 四、解答题 | |||
| 22 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 五、计算题 | |||
| 24 | 0.85 | 根据n=m/M进行相关计算 依据物质的量浓度公式的基础计算 | |

 、
、 、
、 、
、 四种离子,已知前三种离子的个数比为3:2:1,则溶液中
四种离子,已知前三种离子的个数比为3:2:1,则溶液中

