四川省广安市武胜烈面中学校2020-2021学年高一下学期开学考试化学试题
四川
高一
开学考试
2021-04-03
184次
整体难度:
较易
考查范围:
化学与STSE、化学实验基础、常见无机物及其应用、认识化学科学
四川省广安市武胜烈面中学校2020-2021学年高一下学期开学考试化学试题
四川
高一
开学考试
2021-04-03
184次
整体难度:
较易
考查范围:
化学与STSE、化学实验基础、常见无机物及其应用、认识化学科学
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 化学与生产、生活密切相关。下列说法错误的是
| A.Cl2、ClO2、漂白粉都可用于自来水的杀菌消毒 |
| B.化石燃料的直接利用,促进了“低碳”经济的发展 |
| C.CO2、CH4气体的大量排放会造成温室效应的加剧 |
| D.市售的加钙盐、加碘盐,这里的“钙”、“碘”指的是元素 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
您最近一年使用:0次
2019-10-20更新
|
153次组卷
|
8卷引用:河南省长葛市第一高级中学2017-2018学年高一9月质量检测化学试题
单选题
|
较易(0.85)
名校
解题方法
3. 从碘水中提取碘可以采用的方法是
| A.萃取 | B.沉淀 | C.蒸馏 | D.过滤 |
【知识点】 物质分离、提纯的常见物理方法 萃取和分液解读
您最近一年使用:0次
2016-12-09更新
|
770次组卷
|
5卷引用:2011-2012学年黑龙江省牡丹江一中高一上学期期末考试化学试卷
(已下线)2011-2012学年黑龙江省牡丹江一中高一上学期期末考试化学试卷2016-2017学年黑龙江省牡丹江市第一高级中学高一下学期开学检测化学试卷江苏省常州市第一中学2019-2020学年高一上学期期中考试化学试题四川省南充市2020-2021学年高一上学期期末考试化学试题四川省广安市武胜烈面中学校2020-2021学年高一下学期开学考试化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 钠露置在空气中,最终产物是
| A.NaOH | B.Na2O2 | C.Na2CO3 | D.Na2CO3·10H2O |
【知识点】 钠与氧气等非金属的反应解读
您最近一年使用:0次
2020-12-14更新
|
187次组卷
|
3卷引用:江西省贵溪市实验中学2020-2021学年高一上学期12月月考化学试题
单选题
|
容易(0.94)
名校
5. 下列反应中不属于四种基本反应类型,但属于氧化还原反应的是
| A.Fe+CuSO4=FeSO4+Cu |
B.CO+CuO Cu+CO2 Cu+CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 |
D.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
您最近一年使用:0次
2021-01-25更新
|
219次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
名校
6. 设NA为阿伏加德罗常数,下列说法正确的是
| A.22.4LN2所含氮分子数为NA |
| B.NA个Al原子质量为27g |
| C.16gCH4所含原子数为NA |
| D.23g金属钠所含电子数为NA |
您最近一年使用:0次
2021-01-25更新
|
158次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
二、未知 添加题型下试题
三、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
8. 已知有如下反应∶ ①ClO +5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是
+5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是
 +5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是
+5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是A.ClO >Cl2>Fe3+>I2 >Cl2>Fe3+>I2 | B.Cl2>ClO >I2>Fe3+ >I2>Fe3+ |
C.ClO >Cl2>I2>Fe3+ >Cl2>I2>Fe3+ | D.ClO >Fe3+ >Cl2>I2 >Fe3+ >Cl2>I2 |
【知识点】 常见氧化剂与还原剂解读 氧化性、还原性强弱的比较解读
您最近一年使用:0次
2021-01-25更新
|
305次组卷
|
5卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
名校
9. 等质量的镁铝合金粉末分别与下列4种过量的溶液反应,在相同条件下,放出氢气最多的是
| A.2mol/L H2SO4溶液 | B.3mol/L CuSO4溶液 |
| C.6mol/L NaOH溶液 | D.3mol/L Ba(OH)2溶液 |
您最近一年使用:0次
2020-12-18更新
|
213次组卷
|
4卷引用:广东省东莞市七校2020-2021学年高一上学期联考化学试题
单选题
|
适中(0.65)
名校
解题方法
10. 下列离子反应方程式正确的是
| A.铁和稀硫酸反应∶2Fe+6H+=2Fe3++3H2↑ |
B.澄清石灰水中通入足量二氧化碳∶CO2+OH-=HCO |
| C.钠和硫酸铜溶液混合;2Na+Cu2+= 2Na++Cu |
| D.碳酸钙中加入过量醋酸;CaCO3+2H+=Ca2++CO2↑+H2O |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
您最近一年使用:0次
2021-01-25更新
|
139次组卷
|
2卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
名校
解题方法
11. 在无色透明溶液中,下列离子组能大量共存的是
| A.Na+、K+、OH-、Cl- |
B.Na+、Cu2+、SO 、NO 、NO |
C.Mg²+、Ba2+、SO 、Cl- 、Cl- |
D.Ca2+、HCO 、OH-、K+ 、OH-、K+ |
【知识点】 限定条件下的离子共存解读
您最近一年使用:0次
2021-01-25更新
|
190次组卷
|
2卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 下列有关氢氧化亚铁及其制备方法的叙述中,不正确的是


| A.可利用如图所示装置,制备氢氧化亚铁 |
| B.氢氧化亚铁为灰绿色絮状沉淀 |
| C.氢氧化亚铁易被空气氧化 |
| D.实验制备中,氢氧化钠溶液应预先煮沸 |
您最近一年使用:0次
2020-02-24更新
|
274次组卷
|
6卷引用:贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
名校
您最近一年使用:0次
2021-01-25更新
|
222次组卷
|
5卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
名校
14. 实验室用浓盐酸和MnO2制取Cl2下列说法中错误的是
| A.可以用浓硫酸干燥Cl2 | B.可以用排饱和食盐水法收集Cl2 |
| C.该反应需要加热 | D.用NaOH溶液除去Cl2中混有的HCl |
您最近一年使用:0次
2021-01-25更新
|
282次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
名校
解题方法
您最近一年使用:0次
2022-11-30更新
|
508次组卷
|
38卷引用:2015-2016学年河北省枣强中学高一上学期期中测试化学试卷
2015-2016学年河北省枣强中学高一上学期期中测试化学试卷2015-2016学年河北衡水冀州中学高一上月考三理化学卷2015-2016学年河北省冀州中学高一上第三次月考化学试卷2016-2017学年吉林长春外国语学校高一上月考二化学卷江西省临川实验学校2017-2018学年高一(普通班)上学期第一次月考化学试题湖北省宜昌市示范高中协作体2017-2018学年高一上学期期末化学试题【校级联考】辽宁省六校协作体2018-2019学年高一上学期期中考试化学试题【全国百强校】四川省成都外国语学校2018-2019学年高一上学期半期考试化学试题四川外语学院重庆第二外国语学校2017-2018学年高一上学期期中考试化学试题黑龙江省大庆市东风中学2019-2020学年高一上学期期中考试化学试题广东省广州市2019-2020学年高一上学期期中模拟卷试化学试题(二)山东省济宁邹城市第一中学2020-2021学年高一10月月考化学试题广东省江门市第二中学2020-2021学年高一上学期第一次月考化学试题湖南省张家界市民族中学2020-2021学年高一10月月考化学试题(已下线)【浙江新东方】39广东省湛江市第四中学2020-2021学年高一上学期期中考试化学试题安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题广东珠海市2020~2021学年高一上学期9月月考化学试题四川省广安市武胜烈面中学校2020-2021学年高一下学期开学考试化学试题河北省石家庄市第十中学2020-2021学年高一上学期第一次月考化学试题河北省石家庄市第二十三中学2020-2021学年高一上学期10月阶段考试化学试题黑龙江省鸡西实验中学2020-2021学年高一上学期第一次月考化学试题广东省东莞市光明中学2021-2022学年高一上学期第一次月考化学试题广东省湛江市第二十一中学2021-2022学年高一上学期期中考试化学试题广东省揭阳市榕城区仙桥中学2021-2022学年高一上学期期中考试化学试题天津市河东区三校2021-2022学年高一上学期期中考试化学试题新疆乌鲁木齐市第六十八中学2022-2023学年高一10月阶段性期中检测化学试题乌鲁木齐市第六十八中学2022-2023学年高一上学期期中考试化学试题天津市民族中学2022~2023学年高一上学期期中考试化学试题天津市南开大学附属中学2022-2023学年高一上学期期中阶段检测化学试题贵州省贵阳市花溪第六中学2022-2023学年高一上学期期中考试化学试题云南省昆明北大博雅实验中学2021-2022学年高一上学期第一次月考化学试题河北省石家庄市第十五中学2023-2024学年高一上学期第一次月考化学试题天津市红桥区2023-2024学年高一上学期11月期中考试化学试题云南省宣威市第三中学2023-2024学年高一上学期第一次月考化学试题河北省石家庄市第二十三中学2023-2024学年高一上学期期中考试化学试题云南省曲靖市罗平县第一中学2023-2024学年高一上学期9月月考化学试题广东省广州市白云中学2023-2024学年高一上学期12月月考化学试题
单选题
|
容易(0.94)
名校
16. 下列操作正确且能达到实验目的是
| 选项 | 实验操作 | 实验目的 |
| A | 将混合气体通过饱和的碳酸钠的洗气瓶 | 除去CO2中的HCl |
| B | 向25mL的沸水中逐滴滴加5~6滴饱和FeCl3溶液,继续加热至产生红褐色沉淀 | 制备Fe(OH)3胶体 |
| C | 将混合气体通过盛有碱石灰的干燥管 | 除去Cl2中的水蒸气 |
| D | 用棉花包裹Na2O2,放入充满CO2的集气瓶中 | 证明Na2O2与CO2反应是放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-25更新
|
178次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
名校
解题方法
17. 2个XO 恰好能将5个SO
恰好能将5个SO 氧化为SO
氧化为SO ,则生成的唯一还原产物中唯一变价元素X化合价为
,则生成的唯一还原产物中唯一变价元素X化合价为
 恰好能将5个SO
恰好能将5个SO 氧化为SO
氧化为SO ,则生成的唯一还原产物中唯一变价元素X化合价为
,则生成的唯一还原产物中唯一变价元素X化合价为| A.- 3 | B.-1 | C.0 | D.+2 |
【知识点】 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算解读
您最近一年使用:0次
2021-01-25更新
|
207次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
18. 某合金粉末11 g,加入到足量的稀硫酸中,在标准状况下产生的气体体积为11.2 L,此合金可能是( )
| A.Mg-Al合金 | B.Cu-Zn合金 | C.Zn-Fe合金 | D.Mg-Zn合金 |
【知识点】 镁 铝 铁 探究物质组成或测量物质的含量解读
您最近一年使用:0次
2019-02-16更新
|
262次组卷
|
6卷引用:【走进新高考】(人教版必修一)3.3用途广泛的金属材料 同步练习02
单选题
|
较易(0.85)
名校
解题方法
19. 把一定量的Fe和Cu的混和粉末投入到FeCl3溶液中,充分反应后,下列情况不可能的是
| A.Fe 和 Cu都剩 | B.Fe 和 Cu 都不剩 |
| C.Fe 剩余,Cu无剩余 | D.Cu剩余,Fe无剩余 |
【知识点】 Fe、Cu与Fe3+反应几种情况分析及判断
您最近一年使用:0次
2021-01-25更新
|
164次组卷
|
2卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
20. 向200mL的NaOH和Na2CO3混合溶液中滴加0.1 mol/L稀盐酸,CO2的生成量与加入盐酸的体积的关系如图所示。下列判断正确的是


| A.0~a段只发生中和反应 |
| B.原混合液中NaOH 的物质的量浓度为 0.1mol/L |
| C.a=0.2 |
| D.原混合溶液中 NaOH与 Na2CO3的物质的量之比为1∶2 |
您最近一年使用:0次
2021-01-25更新
|
374次组卷
|
6卷引用:辽宁省实验中学东戴河分校、兴城市高级中学2020-2021学年高一12月月考化学试题
四、填空题 添加题型下试题
填空题
|
较易(0.85)
名校
解题方法
21. 有以下9种物质 ①Cu ②Na2O ③酒精 ④氨水 ⑤HCl ⑥NaOH溶液 ⑦KNO3⑧NaHSO4⑨AgCl,请用序号回答下面问题。
(1)能导电的是_______ ,属于电解质的是_______ ,属于非电解_______ ,属于盐的是_______ ,属于酸的是_______
(2)写出以下物质在水溶液中的电离方程式,⑤HCl∶_______ ,⑧NaHSO4:_______ 。
(1)能导电的是
(2)写出以下物质在水溶液中的电离方程式,⑤HCl∶
您最近一年使用:0次
2021-01-25更新
|
216次组卷
|
2卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
填空题
|
较易(0.85)
名校
解题方法
22. 根据氯气及氯的化合物的相关知识,回答下列问题(用化学式或离子符号填写)
(1)氯气与水反应得到的新制氯水含多种微粒。下列现象是由新制氯水中哪种微粒引起的。
①使氯水呈现黄绿色的是_______ ,②能使AgNO3溶液产生白色沉淀的是_______ ,③能使紫色石蕊试液显红色的是_______ ,④能使红色布条褪色的是_______ 。
(2)反应8NH3+3Cl2=N2+6NH4Cl可用于氯气管道的检漏,在该反应中,氧化剂为_______ ,氧化产物为_______ ,氧化剂与还原剂的物质的量之比为_______ 。
(3)氯气可以用于制备漂白粉,漂白粉中的有效成分为_______
(4)在抗击新冠疫情中,"84"消毒液发挥了重要作用。但若将"84"消毒液(主要成分NaClO)与洗厕剂洁厕灵(主要成分盐酸)混合使用,则会产生氯气,其反应的离子方程式为_______ 。
(1)氯气与水反应得到的新制氯水含多种微粒。下列现象是由新制氯水中哪种微粒引起的。
①使氯水呈现黄绿色的是
(2)反应8NH3+3Cl2=N2+6NH4Cl可用于氯气管道的检漏,在该反应中,氧化剂为
(3)氯气可以用于制备漂白粉,漂白粉中的有效成分为
(4)在抗击新冠疫情中,"84"消毒液发挥了重要作用。但若将"84"消毒液(主要成分NaClO)与洗厕剂洁厕灵(主要成分盐酸)混合使用,则会产生氯气,其反应的离子方程式为
您最近一年使用:0次
2021-01-25更新
|
217次组卷
|
2卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
五、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
名校
解题方法
23. A、B、C、D均为中学化学常见的纯净物,A是单质,B为含氧化合物。它们有如图反应关系∶
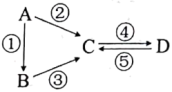
(1)若B是淡黄色固体,②③的反应物中均有同一种液态氢化物,D俗称苏打。则C的化学式为_______ 反应①的化学反应方程式为_______ A、B、C、D 均含同一种元素,检验该元素可采用_______ 法。
(2)若A是制作太阳能电池光伏材料的单质,②③的反应物中均有NaOH,D为酸。则C的水溶液俗称_______ ,反应①②③④⑤中,属于氧化还原反应的有_______ (填序号)写出C中通入过量CO2生成D的化学反应方程式_______ 。
(3)若D为两性氢氧化物。若反应②③在盐酸中完成,则C的化学式为_______ ;若反应②③在NaOH溶液中完成,则C的化学式为_______ 。反应⑤的离子方程式为_______ 。

(1)若B是淡黄色固体,②③的反应物中均有同一种液态氢化物,D俗称苏打。则C的化学式为
(2)若A是制作太阳能电池光伏材料的单质,②③的反应物中均有NaOH,D为酸。则C的水溶液俗称
(3)若D为两性氢氧化物。若反应②③在盐酸中完成,则C的化学式为
您最近一年使用:0次
2021-01-25更新
|
255次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
解答题-实验探究题
|
较易(0.85)
名校
24. 用硫铁矿烧渣(主要成分为Fe2O3和少量 SiO2)为原料可以制得绿矾(FeSO4·7H2O),制备流程如图∶

I.配制250mL4.8 mol/L的硫酸溶液
(1)需用量筒量取18.4 mol/L的浓硫酸_______ mL。
(2)配制时,除量筒、烧杯、玻璃棒和胶头滴管外,还需玻璃仪器_______ .(填仪器名称)。
(3)配制时,一般可分为以下几个步骤∶①量取②计算③稀释④摇匀⑤转移 ⑥洗涤 ⑦定容⑧装瓶,贴标签。操作正确顺序为_______ (填代号)。
(4)配制时,下列操作会引起结果偏高的是_______ 。
①未洗涤烧杯、玻璃棒 ②容量瓶不干燥,含有少量蒸馏水 ③定容时俯视标线④定容时仰视标线⑤超过刻度线,吸出一部分水⑥摇匀后液面下降,补充水
Ⅱ.绿矾的制备流程图中
(5)滤渣的主要化学成分是_______ (填化学式)。
(6)操作I、II、III是同一分离操作,该操作为_______
(7)向溶液X中加入过量的铁粉,发生的主要反应的离子方程式为_______
(8)绿矾长期放置于空气中会变质,原因是_______ 。将绿矾溶于水后,加入试剂_______ (填化学式),出现_______ 的现象,说明已变质。

I.配制250mL4.8 mol/L的硫酸溶液
(1)需用量筒量取18.4 mol/L的浓硫酸
(2)配制时,除量筒、烧杯、玻璃棒和胶头滴管外,还需玻璃仪器
(3)配制时,一般可分为以下几个步骤∶①量取②计算③稀释④摇匀⑤转移 ⑥洗涤 ⑦定容⑧装瓶,贴标签。操作正确顺序为
(4)配制时,下列操作会引起结果偏高的是
①未洗涤烧杯、玻璃棒 ②容量瓶不干燥,含有少量蒸馏水 ③定容时俯视标线④定容时仰视标线⑤超过刻度线,吸出一部分水⑥摇匀后液面下降,补充水
Ⅱ.绿矾的制备流程图中
(5)滤渣的主要化学成分是
(6)操作I、II、III是同一分离操作,该操作为
(7)向溶液X中加入过量的铁粉,发生的主要反应的离子方程式为
(8)绿矾长期放置于空气中会变质,原因是
您最近一年使用:0次
2021-01-25更新
|
274次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
试卷分析
整体难度:较易
考查范围:化学与STSE、化学实验基础、常见无机物及其应用、认识化学科学
试卷题型(共 24题)
题型
数量
单选题
19
未知
1
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 大气污染的治理原理及方法 | |
| 2 | 0.94 | 仪器使用与实验安全 实验安全 | |
| 3 | 0.85 | 物质分离、提纯的常见物理方法 萃取和分液 | |
| 4 | 0.65 | 钠与氧气等非金属的反应 | |
| 5 | 0.94 | 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 6 | 0.85 | 阿伏加德罗常数的求算 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 8 | 0.65 | 常见氧化剂与还原剂 氧化性、还原性强弱的比较 | |
| 9 | 0.85 | 铝与酸溶液反应 铝与强碱溶液反应 | |
| 10 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 11 | 0.94 | 限定条件下的离子共存 | |
| 12 | 0.65 | 氢氧化亚铁 氢氧化亚铁的制备 | |
| 13 | 0.94 | 金属与合金性能比较 | |
| 14 | 0.94 | 氯气的实验室制法 氯气与碱溶液反应 常见气体的制备与收集 | |
| 15 | 0.94 | 离子方程式的书写 | |
| 16 | 0.94 | 胶体的制备 氯气与碱溶液反应 过氧化钠和二氧化碳反应 碳酸钠与碳酸氢钠的相互转化 | |
| 17 | 0.85 | 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算 | |
| 18 | 0.65 | 镁 铝 铁 探究物质组成或测量物质的含量 | |
| 19 | 0.85 | Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 20 | 0.65 | 碳酸钠与盐酸的反应 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 二、未知 | |||
| 7 | 0.65 | 单线桥、双线桥分析氧化还原反应 | 未知 |
| 三、填空题 | |||
| 21 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 物质水溶液的导电性 电离方程式 | |
| 22 | 0.85 | 离子方程式的书写 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 氯水的成分及检验 | |
| 四、解答题 | |||
| 23 | 0.65 | 无机综合推断 硅酸钠与二氧化碳反应 碳酸钠与碳酸氢钠的相互转化 氢氧化铝 | 无机推断题 |
| 24 | 0.85 | 亚铁盐 铁盐的检验 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 | 实验探究题 |





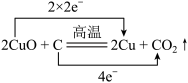
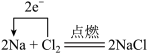

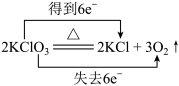
 来表示的是
来表示的是 溶液的反应
溶液的反应

