吉林省长春市第二十九中学2019-2020学年高二下学期第三次月考化学试题
吉林
高二
阶段练习
2020-07-22
303次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
| A.碳酸钠可用于去除餐具的油污 | B.漂白粉可用于生活用水的消毒 |
| C.氢氧化铝可用于中和过多胃酸 | D.碳酸钡可用于胃肠X射线造影检查 |
| A.H2O、CH3COOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| B.溶液、胶体、浊液均为分散系,都属于混合物 |
| C.Al、Al2O3、Al(OH)3均能与盐酸反应又能与氢氧化钠溶液反应,都是具两性的化合物 |
| D.H2SO4、NaOH、NaCl均为强电解质,BaSO4是弱电解质 |
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
【知识点】 既能与酸反应又能与碱反应的无机物质解读
| A.Na2CO3的热稳定性比NaHCO3强 |
| B.Al2O3既是金属氧化物,也是碱性氧化物 |
| C.氧气和臭氧的相互转化是物理变化 |
| D.利用过滤法可把Fe(OH)3胶体从FeCl3溶液中分离出来 |
A.1 mol 所含电子数为11NA 所含电子数为11NA |
| B.标准状况下,22.4LH2O所含原子数为3NA |
| C.1 molFe溶于过量硝酸,电子转移数为2NA |
| D.标准状况下,2.24 L N2和O2的混合气体中分子数为0.1NA |
| A.KClO3在反应中得到电子 | B.ClO2是氧化产物 |
| C.H2C2O4在反应中被还原 | D.1mol KClO3参加反应有2 mol电子转移 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算
| A.CaCO3溶于CH3COOH溶液中,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O |
B.向AlCl3溶液中通入过量NH3,反应的离子方程式为:Al3++4OH—= +2H2O +2H2O |
C.用铝粉和NaOH溶液反应制取少量H2:Al+2OH−= +H2↑ +H2↑ |
D.向稀硫酸中滴入Ba(OH)2溶液,反应的离子方程式为:Ba2++2OH-+2H++ =2H2O+BaSO4↓ =2H2O+BaSO4↓ |
【知识点】 离子方程式的正误判断解读
| A.过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显血红色 |
| B.在酒精灯上灼烧铝箔,会发现熔化的铝不断滴落 |
| C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可 |
| D.向饱和FeCl3溶液中滴加少量NaOH溶液,煮沸后即可得到红褐色的Fe(OH)3胶体 |
| A.3 g 3He含有的中子数为1NA |
B.2.4 g Mg与H2SO4完全反应,转移的电子数为0.1 |
| C.1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA |
| D.同等质量的氧气和臭氧中,电子数相同 |
 沉淀完全时,铝元素的存在形式是
沉淀完全时,铝元素的存在形式是| A.Al(OH)3和Al3+ | B.Al(OH)3和 |
| C.全部为Al(OH)3 | D.全部为 |
A.K+、 、Cl-、 、Cl-、 | B.Na+、Ba2+、 、Cl- 、Cl- |
C.Na+、 、Al3+、Cl- 、Al3+、Cl- | D.Na+、Mg2+、 、 、 |
【知识点】 限定条件下的离子共存解读
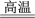 TiCl4+2CO。下列关于该反应的说法正确的是( )
TiCl4+2CO。下列关于该反应的说法正确的是( )| A.TiO2是氧化剂 | B.四氯化钛是还原产物 |
| C.Cl2发生氧化反应 | D.氧化剂与还原剂的物质的量之比为1∶2 |
【知识点】 氧化还原反应基本概念
A.0.1 mol·L−1NaOH溶液:Na+、K+、 、 、 |
B.0.1 mol·L−1FeCl2溶液:K+、Mg2+、 、 、 |
| C.0.1 mol·L−1K2CO3溶液:Na+、Ba2+、Cl−、OH− |
D.0.1 mol·L−1H2SO4溶液:K+、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
A.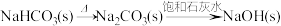 |
B.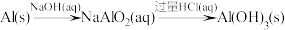 |
C.Fe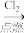 FeCl2 FeCl2 Fe(OH)2 Fe(OH)2 |
D.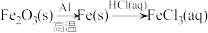 |
【知识点】 碳酸钠与碳酸氢钠的相互转化解读 铝 偏铝酸钠与盐酸的反应解读 铁
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③铝与NaOH溶液④硝酸与铁 ⑤氯化铁溶液与铁 ⑥碳酸氢钠溶液与澄清的石灰水
| A.③⑤ | B.①③⑥ | C.仅有⑤ | D.②④ |
 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为| A.3.0 mol | B.1.5 mol | C.1.0 mol | D.0.75 mol |
【知识点】 基于氧化还原反应守恒规律的计算解读
 的稀溶液中加入足量的Na2O2固体并加热,充分反应加入过量的稀盐酸,反应完全后,离子数目几乎没有变化的是
的稀溶液中加入足量的Na2O2固体并加热,充分反应加入过量的稀盐酸,反应完全后,离子数目几乎没有变化的是| A.Fe3+ | B.Fe2+ | C.Al3+ | D.NH |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 过氧化钠 氢氧化铝
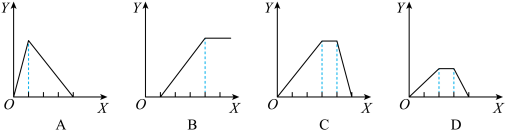
| A.如图A:向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡 |
| B.如图B:向NaAlO2溶液中滴加盐酸且边滴边振荡 |
| C.如图C:向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量 |
| D.如图D:向等物质的量的NaOH、Ba(OH)2的混合溶液中逐渐通入二氧化碳至过量 |
 ,则
,则 的物质的量为( )
的物质的量为( )| A.0.1mol | B.0.15mol | C.0.3mol | D.0.5mol |
二、填空题 添加题型下试题
 NaNO2+
NaNO2+ HI―→
HI―→ NO↑+
NO↑+ I2+
I2+ NaI+
NaI+ H2O
H2O(1)配平上述化学方程式
(2)上述反应的氧化剂是
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读
(1)KClO4中氯元素的化合价是
(2)Fe2O3可处理产生的Na,反应为
 ,反应中Na做
,反应中Na做【知识点】 氧化还原反应的几组概念解读 氧化还原反应的应用
三、解答题 添加题型下试题
(1)用脱脂棉包住过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,看到脱脂棉剧烈燃烧起来。
由上述实验现象所得到的有关过氧化钠跟水反应的结论是:第一,有
a.氧化剂 b.还原剂 c.既是氧化剂,又是还原剂 d.既不是氧化剂,又不是还原剂
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体SO2。甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中有Fe2+,应选用的试剂编号为
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
写出相应的离子方程式:
【知识点】 过氧化钠与水的反应解读 铁盐与亚铁盐鉴别试剂的选择解读

(1)推断(写化学式):A.
(2)请写出反应D→F的化学方程式:
(3)检验F中金属阳离子的常用试剂是
(4)写出C与过量氢氧化钠溶液反应的离子方程式
(5)若向D溶液中滴加氢氧化钠溶液,现象是:
 。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):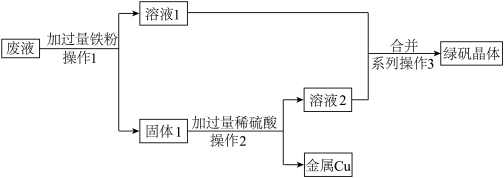
请回答以下问题:
(1)操作1和操作2的名称是
(2)废液中加过量铁时发生反应的离子方程式为
(3)若使用得到的绿矾晶体制备净水剂Fe2(SO4)3溶液,除在绿矾中加入适量稀硫酸外,还需要加入
①稀H2SO4②Cl2③H2O2④Fe粉
四、填空题 添加题型下试题
(1)基态Cr原子的价电子排布式为
(2)PO
 的空间构型为
的空间构型为(3)碳化硅(SiC)晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因是
(4)用“>”或“<”填空:
第一电离能:N
(5)铁和氮形成一种晶体,晶胞结构如图所示,则该晶体的化学式为

试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 漂白粉和漂粉精 碳酸钠的俗称、物理性质及用途 明矾的净水作用及原理 化学科学对人类文明发展的意义 | |
| 2 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 分散系概念 电解质、非电解质概念 既能与酸反应又能与碱反应的无机物质 | |
| 3 | 0.65 | 既能与酸反应又能与碱反应的无机物质 | |
| 4 | 0.94 | 酸、碱、盐、氧化物的概念及其相互联系 物理变化与化学变化 碳酸氢钠的不稳定性 渗析 | |
| 5 | 0.94 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 6 | 0.85 | 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 7 | 0.85 | 离子方程式的正误判断 | |
| 8 | 0.85 | 胶体的制备 氧化铝 铁盐 铁盐与亚铁盐鉴别试剂的选择 | |
| 9 | 0.65 | 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 10 | 0.85 | 明矾与氢氧化钡溶液反应的离子方程式 铝盐与强碱溶液反应 | |
| 11 | 0.85 | 限定条件下的离子共存 | |
| 12 | 0.4 | 氧化还原反应的规律 | |
| 13 | 0.94 | 氧化还原反应基本概念 | |
| 14 | 0.65 | 限定条件下的离子共存 | |
| 15 | 0.85 | 碳酸钠与碳酸氢钠的相互转化 铝 偏铝酸钠与盐酸的反应 铁 | |
| 16 | 0.65 | 离子方程式的书写 碳酸钠与碳酸氢钠性质的比较 偏铝酸钠与盐酸的反应 铁与强氧化性酸的反应 | |
| 17 | 0.85 | 基于氧化还原反应守恒规律的计算 | |
| 18 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 过氧化钠 氢氧化铝 | |
| 19 | 0.65 | 氢氧化铝与强酸反应 氢氧化铝与强碱反应 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 20 | 0.94 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 二、填空题 | |||
| 21 | 0.65 | 离子方程式的书写 | |
| 22 | 0.85 | 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 23 | 0.85 | 氧化还原反应的几组概念 氧化还原反应的应用 | |
| 27 | 0.65 | 电离能 键能、键长、键角及应用 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | |
| 三、解答题 | |||
| 24 | 0.65 | 过氧化钠与水的反应 铁盐与亚铁盐鉴别试剂的选择 | 实验探究题 |
| 25 | 0.65 | 无机综合推断 铝三角转化 铁盐的检验 与“铁三角”有关的推断 | 无机推断题 |
| 26 | 0.85 | 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 | 工业流程题 |

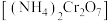 是一种受热易分解的盐,下列各项中的物质可能是重铬酸铵受热分解的产物是
是一种受热易分解的盐,下列各项中的物质可能是重铬酸铵受热分解的产物是 、
、 、
、
 、
、 、
、 、
、

