重庆市江北中学2019-2020学年高一上学期期末模拟考试化学试题
重庆
高一
阶段练习
2020-02-25
296次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.将BaSO4放入水中不能导电,所以硫酸钡不是电解质 |
| B.NaCl溶液能导电,所以NaCl溶液是电解质 |
| C.氯化氢溶于水能导电,所以盐酸是电解质 |
| D.固态的NaCl不导电,熔融态NaCl可以导电 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
 。下列说法正确的是
。下列说法正确的是A.1L0.1mol· NH4Cl溶液中, NH4Cl溶液中, 的数量为0.1 的数量为0.1 |
B.2.4gMg与H2SO4完全反应,转移的电子数为0.1 |
C.标准状况下,2.24LN2和O2的混合气体中分子数为0.2 |
D.0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2 |
【知识点】 阿伏加德罗常数 阿伏加德罗定律 氧化还原反应有关计算
| A.1:1 | B.2:1 | C.1:2 | D.3:2 |
【知识点】 氧化还原反应的几组概念解读 与氧化剂、还原剂有关的计算解读

| A.Y的最高价氧化物对应水化物的酸性比X的弱 |
| B.Z位于元素周期表中第二周期,第ⅥA族 |
| C.X的气态氢化物的稳定性比Z的弱 |
| D.M的原子半径比Y的原子半径大 |
A.在无色溶液中: 、Fe2+、 、Fe2+、 、 、 |
B.在含大量Ba2+的溶液中: 、Na+、Cl-、OH- 、Na+、Cl-、OH- |
C.在强碱性溶液中:Na+、K+、 、 、 |
D.在强酸性溶液中:K+、Fe2+、Cl-、 |
【知识点】 离子共存 限定条件下的离子共存解读
| A.常温常压下,11.2L二氧化碳含有的原子数等于1.5NA |
| B.标准状况下,22.4LCCl4中所含分子数为NA |
| C.标准状况下,18g水所含原子数为NA |
| D.常温常压下,48gO2与O3混合物含有的氧原子数为3NA |
【知识点】 阿伏加德罗常数的求算解读 阿伏加德罗常数的应用解读
 将转化为
将转化为| A.S2- | B.S | C.SO | D.SO |
【知识点】 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算解读
| A.上述反应中每生成1mol N2O,消耗67.2LCO |
| B.等质量的N2O和CO2含有相等的电子数 |
| C.N2O只有氧化性,无还原性 |
| D.上述反应中若有3 mol的CO被还原,则转移6NA个电子 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
| A.NH4Cl | B.H2SO4 | C.I2 | D.NaCl |
【知识点】 共价键 化学键与物质类别关系的判断解读
| A.0.34 mol | B.0.38 mol | C.0.28 mol | D.0.18 mol |
| A.3 mol | B.2 mol | C.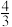 mol mol | D.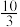 mol mol |
| A.二种 | B.三种 | C.四种 | D.五种 |
二、解答题 添加题型下试题

(1)只根据图I、II所示实验,能够达到实验目的是(填装置序号)
(2)图III、IV所示实验均能鉴别这两种物质,其加热时都能发生的反应的化学方程式为
(3)有同学认为,除上述试验方法外,向两种固体配成的溶液中加入澄清石灰水也可以区分它们,这种说法是
 溶液中加入足量澄清石灰水,发生反应的离子方程式为:
溶液中加入足量澄清石灰水,发生反应的离子方程式为:(4)另有两瓶溶液,已知分别是
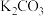 溶液和
溶液和 溶液,请你写出鉴别方法。
溶液,请你写出鉴别方法。
已知:反应Ⅱ包含2NaHSO3⇌Na2S2O5+H2O等多步反应。
(1) 反应Ⅰ的化学方程式为
(2)“灼烧”时发生反应的化学方程式为
(3)已知Na2S2O5与稀硫酸反应放SO2,其离子方程式为
(4)副产品X化学式为
(5)为了减少产品Na2S2O5中的杂质含量,理论上需控制反应Ⅱ中气体与固体反应物的物质的量之比为
①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水 ④饱和碳酸氢钠溶液 ⑤NaOH溶液 ⑥稀盐酸
【知识点】 碳酸钠 物质分离、提纯综合应用解读 物质制备的探究解读
三、填空题 添加题型下试题
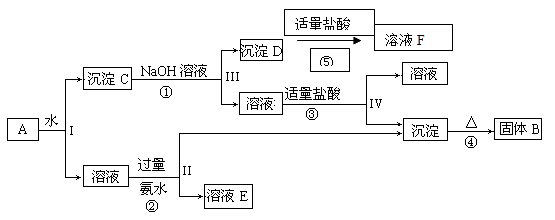
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B
溶液E
(3)写出①、④两个反应的化学方程式
①
(4)写出②、③两个反应的离子方程式
②
(5)设计实验检验溶液F中所含溶质:
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3
(1)制备KBr的一种方法如下:80℃时,向溶有CO(NH2)2的KOH溶液中缓慢加入Br2,至pH为6~7时反应完全,生成CO2、N2等。该反应的化学方程式为
(2)KBr可用于测定苯酚(C6H5OH)样品的纯度,方法如下:取0.5000g苯酚试样,用NaOH溶液溶解后定容成250.00mL溶液;移取25.00mL该溶液,加入25.00mL0.03000mol•L﹣1的KBrO3(含过量KBr)标准溶液,然后加入足量盐酸,充分反应后再加足量KI溶液,充分反应;用0.1000mol•L﹣1Na2S2O3溶液滴定至淡黄色,加入指示剂,继续滴定至终点,用去16.20mL。测定过程中物质的转化关系如下:

①加入的指示剂为
②计算苯酚样品的纯度(写出计算过程)
【知识点】 酸碱中和滴定原理的应用解读 物质含量的测定
试卷分析
试卷题型(共 16题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 2 | 0.4 | 阿伏加德罗常数 阿伏加德罗定律 氧化还原反应有关计算 | |
| 3 | 0.85 | 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 | |
| 4 | 0.65 | 元素周期表提供的元素信息 金属与非金属在周期表中位置及其性质递变的规律 “位构性”关系理解及应用 | |
| 5 | 0.94 | 离子共存 限定条件下的离子共存 | |
| 6 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 | |
| 7 | 0.65 | 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算 | |
| 8 | 0.65 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 9 | 0.65 | 共价键 化学键与物质类别关系的判断 | |
| 10 | 0.94 | 硝酸的强氧化性 | |
| 11 | 0.65 | 氧化还原反应的定义及实质 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 12 | 0.65 | 铵盐与碱反应 含镁化合物 既能与酸反应又能与碱反应的无机物质 铝三角转化 | |
| 二、解答题 | |||
| 13 | 0.65 | 碳酸钠 碳酸氢钠 化学实验探究 | 实验探究题 |
| 14 | 0.65 | 碳酸钠 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 三、填空题 | |||
| 15 | 0.65 | 氧化铝与碱溶液反应 | |
| 16 | 0.65 | 酸碱中和滴定原理的应用 物质含量的测定 | |



