山东省日照市五莲县2020届高三9月模块诊断性测试化学试题
山东
高三
阶段练习
2020-05-01
428次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础、化学反应原理
山东省日照市五莲县2020届高三9月模块诊断性测试化学试题
山东
高三
阶段练习
2020-05-01
428次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学与人类生产、生活密切相关。下列叙述正确的是
| A.氢氧化铝、碳酸钠都是常见的胃酸中和剂 |
| B.二氧化硫可用作葡萄酒的防腐剂和抗氧化剂 |
| C.制造普通水泥和硅酸盐玻璃的主要原料相同 |
| D.高压钠灯所发出的黄光是通过钠燃烧产生 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
2. 下列各组物质的分类正确的是
| A.混合物:氯水、水玻璃、水银、福尔马林、聚乙烯 |
| B.电解质:SO2、冰醋酸、石膏、纯碱 |
| C.胶体:碘酒、牛奶、豆浆、淀粉溶液 |
| D.同素异形体:C60、C80、金刚石、石墨 |
您最近一年使用:0次
单选题
|
适中(0.65)
真题
名校
4. 下列有关实验操作的叙述错误的是
| A.过滤操作中,漏斗的尖端应接触烧杯内壁 |
| B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 |
| C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 |
| D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 |
您最近一年使用:0次
2019-01-30更新
|
1829次组卷
|
30卷引用:2016年全国普通高等学校招生统一考试化学(海南卷精编版)
2016年全国普通高等学校招生统一考试化学(海南卷精编版)2015-2016学年吉林长春外国语学校高二下期末理化学卷2015-2016学年吉林长春外国语高二下期末理科化学试卷2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷2017届内蒙古临河区巴彦淖尔一中高三上9月月考化学卷2017届上海市黄浦区高三下学期4月等级考调研测试化学试卷江西省赣中南五校2017届高三下学期期中联合考试化学试题福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题山东省潍坊市2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题十对接高考精练--化学实验常用仪器及基本操作新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题湖南省岳阳市第一中学2018届高三12月月考化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)解密16 化学实验基础(教师版)——备战2018年高考化学之高频考点解密甘肃省酒泉市敦煌中学2019届高三一诊化学试题2018-2019学年鲁科版高一化学必修一1.1走进化学科学练习题黑龙江省哈尔滨师范大学青冈实验中学校2016-2017学年高二下学期期末考试化学试题河南省驻马店经济开发区高级中学2019届高三上学期第一次月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点03 物质的量浓度及溶液的配制2016年全国普通高等学校招生统一考试化学(海南卷参考版)黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(理)试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题6 化学实验复习题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题浙江省宁波市效实中学2018-2019学年高二下学期期中考试化学试题山东省日照市五莲县2020届高三9月模块诊断性测试化学试题(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)押全国卷理综第9题 化学实验基础-备战2021年高考化学临考题号押题(课标全国卷)湖南省永州市2021-2022学年高三上学期第一次适应性考试化学试题上海市曹杨第二中学2021-2022学年高二上学期期末考试化学试题(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)
单选题
|
较易(0.85)
名校
5. 下列对有关文献的理解错误的是
| A.《天工开物》记载制造青瓦“窑泥周寒其孔,浇水转釉”,红瓦转化为青瓦的原因是Fe2O3转化为其他铁的氧化物 |
| B.《物理小识》记载“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不没,“气”凝即得 “矾油”。青矾厂气是CO 和CO2 |
| C.《开宝本草》中记载了中药材铁华粉的制作方法:“取钢煅作时如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”中药材铁华粉是醋酸亚铁 |
| D.《本草经集注》对“消石”的注解如下:“……如握雪不冰。强烧之,紫青烟起,仍成灰……”这里的“消石”指的是硝酸钾 |
您最近一年使用:0次
2018-06-03更新
|
1371次组卷
|
4卷引用:河北省衡水中学2018届高三第二十次模拟考试(B)化学试题
单选题
|
适中(0.65)
6. 用NA表示阿伏加 德罗常数的值。下列说法正确的是
| A.常温下,56g铁片投入足量浓H2SO4中,充分反应,生成NA个SO2分子 |
| B.向100mL 1mol·L-1Fe(NO3)3溶液中滴加足量HI溶液,转移0.1NA个电子 |
| C.4.6 g SO2和CO2的混合气体含有的电子数为2.3NA |
| D.120g NaHSO4固体中阳离子和阴离子的总数为3NA |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
| 物质(括号内为杂质) | 除杂试剂 | |
| A | FeCl2溶液(FeCl3) | Fe粉 |
| B | NaCl溶液(MgCl2) | NaOH溶液、稀HCl |
| C | Cl2(HCl) | H2O、浓H2SO4 |
| D | NO(NO2) | H2O、无水CaCl2 |
| A.A | B.B | C.C | D.D |
【知识点】 氧化还原反应的规律解读 物质分离、提纯的常见化学方法解读
您最近一年使用:0次
2019-06-09更新
|
12028次组卷
|
104卷引用:2019年北京高考化学试题
2019年北京高考化学试题(已下线)专题04 氧化还原反应——2019年高考真题和模拟题化学分项汇编四川省威远中学2018-2019学年高一下学期第二次月考化学试题河北省易县中学2018-2019学年高二下学期期末考试化学试题福建省华安一中2018-2019学年高二下学期期末考试化学试题(已下线)专题2.3 氧化还原反应(讲)-《2020年高考一轮复习讲练测》广西桂林十八中2020届高三上学期8月第一次月考化学试题浙江省东阳中学2019-2020学年高二10月月考化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应2020届高考化学小题狂练(全国通用版)专练18 物质的检验、分离和提纯江西省南昌市新建县第一中学2020届高三上学期第一次月考化学试题(共建部)【全国百强校】广西壮族自治区玉林高级中学2020届高三上学期第一次月考(8月)理综化学试题北京市房山区2019-2020学年高一上学期期末考试化学试题专题5.1 化学实验基础(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升专题1.3 氧化还原反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)《2020年新高考政策解读与配套资源》模拟试题03-2020年北京新高考化学模拟试题天津市海河中学2020届高三第二学期化学测试(二)试卷(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训云南省曲靖市会泽县第一中学2019-2020高二上学期开学考试化学试题山东省日照市五莲县2020届高三9月模块诊断性测试化学试题北京市第八十中学2019-2020学年高一下学期期中考试化学试题上海市黄浦区2019-2020学年高三下学期学业等级考科目阶段性调研化学试题福建省安溪一中、养正中学、惠安一中、泉州实验中学2019-2020学年高二下学期期末联考化学试题山西省孝义市第二中学校2019-2020学年高一下学期期末考试化学(B卷)试题(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测(已下线)第08讲 氧化还原反应的基本概念和规律(精讲)——2021年高考化学一轮复习讲练测四川省成都经济技术开发区实验中学2021届高三上学期入学考试化学试题黑龙江省哈尔滨市三中2020届高三第二次月考化学试题天津市南开中学2020届高三第二次月考化学试题人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 高考帮全国百强名校2021届高三上学期领军考试化学试题(9月)宁夏回族自治区青铜峡市高级中学2021届高三上学期第二次月考化学试题四川省遂宁市射洪中学校2021届高三上学期第二次月考理综化学试题(已下线)【南昌新东方】3. 师大附中 左佳鑫北京首都师范大学第二附属中学2021届高三9月月考化学试题高一必修第一册(苏教2019)专题3 第一单元 氯气及氯的化合物3内蒙古自治区乌兰察布市集宁一中(西校区)2021届高三上学期期中考试化学试题湖南平江县第一中学2021届高三上学期第二次月考化学试题上海市七宝中学2021届高三上学期期中考试化学试题专题9 专题强化练6 铁及其化合物-高中化学必修第二册苏教版2019(已下线)专题04 氧化还原反应-备战2021届高考化学二轮复习题型专练(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)解题达人.化学选择题(2021全国卷)巩固小卷01山西省长治市第二中学校2020-2021学年高一下学期期中考试化学试题河北省衡水市安平中学2020-2021学年高一下学期第一次月考化学试题山西省忻州市岢岚县中学2020-2021学年高一下学期3月月考化学试题(已下线)第06讲 氧化还原反应(精讲)-2022年一轮复习讲练测(已下线)课时09 氧化还原反应概念及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向05 氧化还原反应-备战2022年高考化学一轮复习考点微专题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)四川省蓬安中学校2020届高三上学期入学考试化学试题(已下线)第5讲 氧化还原反应(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)课时52 物质的分离、提纯和检验-2022年高考化学一轮复习小题多维练(全国通用)福建省厦门第六中学2021-2022学年高二上学期开学适应性练习化学试题河南省南阳市内乡县菊潭高级中学2022届高三入学考试化学试题上海市上海交通大学附属中学2021届高三期中考试化学试题(已下线)第28讲 物质的分离、提纯、检验与鉴别(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题05 氧化还原反应-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)宁夏青铜峡市高级中学2021-2022学年高三上学期11月测试化学试题(已下线)查补易混易错点05 氧化还原反应-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)查补易混易错点05 氧化还原反应-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)考点50 物质的分离、提纯和检验-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题01 物质及其变化-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第26讲 物质的分离、提纯、检验与鉴别(练)-2023年高考化学一轮复习讲练测(新教材新高考)内蒙古彦淖尔市临河区第三中学2022届高三上学期第一次月考化学试题北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题河南省鹤壁市高中2022-2023学年高三上学期第三次模拟考试化学试题(已下线)化学(北京B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)专题04 氧化还原反应及其应用(练)-2023年高考化学二轮复习讲练测(新高考专用)陕西省西安市鄠邑区第二中学2021-2022学年高三上学期第二次月考化学试题(已下线)【知识图鉴】单元讲练测必修第二册第五单元 02基础练(已下线)专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第一章 化学物质及其变化 第4讲 氧化还原反应(已下线)题型15 氧化还原反应的判断(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)北京市一零一中学2022-2023学年高三下学期3月统练二化学试题北京交通大学附属中学2022-2023学年高一下学期开学考试化学试题天津市西青区杨柳青一中2022-2023学年高一下学期第一次适应性测试化学试题四川省资阳市乐至中学2022-2023学年高一下学期3月月考化学试题广东省湛江市雷州市第一中学2022-2023学年高一下学期4月月考化学试题(已下线)查补易混易错03 基本概念和基础理论部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)北京师范大学第二附属中学2022-2023学年高一下学期期中测试化学试题(已下线)考点04 氧化还原反应的基本概念和规律(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)T10-物质的分离、提纯陕西省西安中学2023-2024学年高三上学期8月月考化学试题广东省台山市第一中学2023-2024学年高三上学期第一次月考化学试题河南省南阳市第一中学校2023-2024学年高三上学期第三次月考化学试题福建省福州八县协作校2023-2024学年高三上学期期中考试化学试题(已下线)第2讲 物质的分离与提纯安徽省安庆第二中学东区2021-2022学年高三上学期9月月考化学试卷广东省惠州市博罗县博师高级中学2023-2024学年高三上学期9月月考化学试题北京市交通大学附属中学2023-2024学年高一上学期12月月考化学试题北京市清华大学附属中学朝阳学校2023-2024学年高三下学期开学考化学试题黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题
单选题
|
适中(0.65)
解题方法
8. 室温下,下列各组离子在指定溶液中能大量共存的是
| A.0.1 mol·L−1的NH4Al(SO4)2溶液中:K+、Na+、CO32−、Cl- |
| B.0. 1 mol·L−1的Fe2(SO4)3溶液:Cu2+、NH4+ 、NO3−、SO42− |
| C.0. 1 mol·L−1的HCl 溶液:Ba2+、K+、CH3COO−、NO3− |
| D.0. 1 mol·L−1的NaOH溶液:Mg2+、Na+、SO42−、HCO3− |
【知识点】 离子反应的发生条件解读 离子共存 限定条件下的离子共存解读
您最近一年使用:0次
单选题
|
适中(0.65)
9. 下列物质均有漂白作用,其漂白原理相同的是
①二氧化硫 ②漂白粉 ③过氧化钠 ④活性炭⑤过氧化氢
①二氧化硫 ②漂白粉 ③过氧化钠 ④活性炭⑤过氧化氢
| A.①②⑤ | B.②③⑤ | C.①②③④ | D.①④ |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 下列有关离子方程式的书写正确的是
| A.向偏铝酸钠溶液中加入过量的稀盐酸:AlO2-+H++H2O= Al(OH)3↓ |
| B.将磁性氧化铁溶于氢碘酸:Fe3O4+8H+=2Fe3++Fe2++4H2O |
| C.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3=2FeO42−+3Cl−+4H++H2O |
| D.向NaClO溶液中通入足量CO2:ClO-+CO2+H2O=HClO+HCO3− |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 制备Fe(OH)₃胶体 | 将NaOH浓溶液滴加到饱和FeCl₃溶液中 |
| B | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| C | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| D | 配制0.4000mol·L⁻¹的NaOH溶液250mL | 称取4.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,立刻转移至250 mL容量瓶中定容 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
12. 下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合有
| 序号 | X | Y | Z | W |  |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A.①②③ | B.①③④ | C.①②④ | D.②③④ |
【知识点】 物质的转化 铝三角转化解读 与“铁三角”有关的推断解读
您最近一年使用:0次
2020-04-29更新
|
183次组卷
|
3卷引用:【全国百强校】山西省山西大学附属中学2018-2019学年高一下学期2月模块诊断化学试题
单选题
|
适中(0.65)
解题方法
13. 取 1LFeCl3溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法错误的是
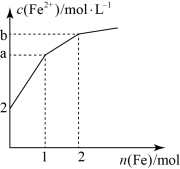
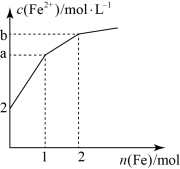
| A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+ |
| B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu |
| C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1 |
| D.腐蚀之前原溶液中n(Fe3+)=4 mol |
您最近一年使用:0次
14. 在隔绝空气的情况下,9.2 g铜、镁混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到标准状况下4.48 LNO气体。向反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为
| A.19.4 g | B.18.6 g | C.20 g | D.24 g |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
15. 一种废水处理剂可表示为MxFey(SO4)z(OH)w,可按下列实验步骤确定其组成(气体体积在标准状况下测定):

下列有关叙述错误的是

下列有关叙述错误的是
| A.检验a中是否含有Fe3+可用KSCN溶液 |
| B.气体b能使湿润的红色石蕊试纸变蓝 |
| C.加入稀盐酸的目的是溶解其中的氢氧化物 |
| D.若V=448,m1=13.6,m2=9.32,可确定该化合物为NH4Fe3(SO4)2(OH)3 |
您最近一年使用:0次
2019-03-19更新
|
284次组卷
|
4卷引用:2019年3月24日 《每日一题》二轮复习 -每周一测
(已下线)2019年3月24日 《每日一题》二轮复习 -每周一测山东省日照市五莲县2020届高三9月模块诊断性测试化学试题山东省济宁市兖州一中2021届高三10月月考化学试题(已下线)第三章 金属及其化合物 第14练 铁及其化合物的转化关系
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
16. 如图A~E是中学化学常用的五种仪器:

回答下列问题:
(1)上述仪器中,使用时需首先检查是否漏水的有_________ (填标号)。
(2)下列实验操作中,使用到仪器C的是________ (填标号)。
a.分离水和酒精的混合物
b.分离水和四氯化碳的混合物
c.分离水和泥砂的混合物
d.提纯Fe(OH)3胶体
(3)某化学兴趣小组实验过程中,需要480 mL0.5mol·L-1 NaOH溶液。
①除上述提供的仪器外,还用到的玻璃仪器有_________________ 。

②如图所示,转移操作中的一处错误是_____________________ 。
③在配制过程中,下列情况会导致所配溶液浓度偏低的是_______ (填标号)。
a.准确称量9.6gNaOH
b.溶解时未冷却至室温就转移
c.在定容时,仰视刻度线
d.加水至刻度线后摇匀,发现液面低于刻度线

回答下列问题:
(1)上述仪器中,使用时需首先检查是否漏水的有
(2)下列实验操作中,使用到仪器C的是
a.分离水和酒精的混合物
b.分离水和四氯化碳的混合物
c.分离水和泥砂的混合物
d.提纯Fe(OH)3胶体
(3)某化学兴趣小组实验过程中,需要480 mL0.5mol·L-1 NaOH溶液。
①除上述提供的仪器外,还用到的玻璃仪器有

②如图所示,转移操作中的一处错误是
③在配制过程中,下列情况会导致所配溶液浓度偏低的是
a.准确称量9.6gNaOH
b.溶解时未冷却至室温就转移
c.在定容时,仰视刻度线
d.加水至刻度线后摇匀,发现液面低于刻度线
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
解题方法
17. 物质的类别和核心元素的化合价是研究物质性质的两个角度。请根据图所示回答下列问题:

(1)X与Y反应可生成淡黄色固体,反应的化学方程式____________________ 。
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是______ (填序号)。
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为___________ 。
(4)处理SO2废气的一种工艺如图所示:
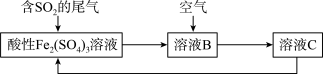
①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是________________________ 。
②溶液B与空气发生反应生成溶液C,其中氧化剂是______________ 。
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是______________ 。

(1)X与Y反应可生成淡黄色固体,反应的化学方程式
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为
(4)处理SO2废气的一种工艺如图所示:

①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是
②溶液B与空气发生反应生成溶液C,其中氧化剂是
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
解题方法
18. 下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。

请回答下列问题:
(1)A在B中燃烧的现象是__________________________________________ 。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是_________________________ 。
(3)G+J→M的离子方程式是____________________________________ 。
(4)Y受热分解的化学方程式是______________________________________ 。
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是____________________ 。

请回答下列问题:
(1)A在B中燃烧的现象是
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是
(3)G+J→M的离子方程式是
(4)Y受热分解的化学方程式是
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
19. 亚硝酰氯(NOCl)是有机合成中的重要试剂,可由一氧化氮与氯气在常温常压下合成。已知NOCl是一种红褐色液体或黄色气体,其熔点是-64.5℃,沸点是-5.5℃,遇水易水解。回答下列问题:
(1)实验室制备原料气NO和Cl2的装置如下图所示。
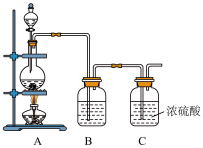
①实验室制NO时,装置A中烧瓶内发生反应的化学方程式为______________ 。
②实验室制Cl2时,装置B的作用是______________________ 。
(2)将上述收集到的Cl2充入集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_____________ 。
②装置D中的现象为_____________________________________________ 。
③装置E中无水氯化钙的作用为_______________________________ 。
④某同学认为装置F不能吸收NO,为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是______________ 。
(1)实验室制备原料气NO和Cl2的装置如下图所示。

①实验室制NO时,装置A中烧瓶内发生反应的化学方程式为
②实验室制Cl2时,装置B的作用是
(2)将上述收集到的Cl2充入集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
②装置D中的现象为
③装置E中无水氯化钙的作用为
④某同学认为装置F不能吸收NO,为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是
您最近一年使用:0次
20. 工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下。回答下列问题:
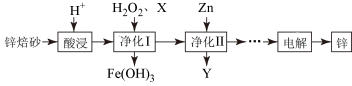
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是________ 。
②工业上利用反应ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是________ 。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是________________________ (任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有____________________________________________ 。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_________ ;试剂X的作用是_______ 。

(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是
②工业上利用反应ZnFe2(C2O4)3·6H2O
 ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是
(3)净化Ⅰ中H2O2参与反应的离子方程式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础、化学反应原理
试卷题型(共 20题)
题型
数量
单选题
15
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 焰色试验 钠单质的保存与用途 氢氧化铝的物理性质及用途 传统硅酸盐材料 | |
| 2 | 0.65 | 分类方法的应用 胶体的定义及分类 非电解质、电解质物质类别判断 几组常见同素异形体 | |
| 3 | 0.65 | 常见硫酸盐的性质 二氧化硅的用途 蛋白质的变性 常用仪器及使用 | |
| 4 | 0.65 | 酸碱中和滴定实验相关仪器 仪器使用与实验安全 一定物质的量浓度的溶液的配制 化学实验基础操作 | |
| 5 | 0.85 | 化学科学对人类文明发展的意义 化学在农业中的应用 化学在工业中的应用 | |
| 6 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 7 | 0.65 | 氧化还原反应的规律 物质分离、提纯的常见化学方法 | |
| 8 | 0.65 | 离子反应的发生条件 离子共存 限定条件下的离子共存 | |
| 9 | 0.65 | 漂白粉和漂粉精 二氧化硫的漂白性 过氧化钠的强氧化性 | |
| 10 | 0.65 | 离子反应的发生及书写 离子反应的发生条件 离子方程式的正误判断 | |
| 11 | 0.65 | 胶体的制备 铜与强氧化性酸的反应 配制一定物质的量浓度的溶液的步骤、操作 物质分离、提纯的常见化学方法 | |
| 12 | 0.65 | 物质的转化 铝三角转化 与“铁三角”有关的推断 | |
| 13 | 0.65 | 依据Fe3+与其他物质氧化性强弱关系的相关计算 Fe、Cu及相关离子的反应 印刷电路板 Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 14 | 0.65 | 基于氧化还原反应守恒规律的计算 铜与强氧化性酸的反应 探究物质组成或测量物质的含量 | |
| 15 | 0.65 | 铵根离子的检验 铁盐 氢氧化铁化学性质 探究物质组成或测量物质的含量 | |
| 二、解答题 | |||
| 16 | 0.65 | 常用仪器及使用 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的仪器 萃取和分液 | 实验探究题 |
| 17 | 0.65 | 氧化性、还原性强弱的比较 含硫化合物之间的转化 二氧化硫的弱氧化性 电子转移计算 | 无机推断题 |
| 18 | 0.65 | 无机综合推断 氯气与非金属单质的反应 硝酸盐的不稳定性 Fe2+的鉴别及其应用 | 无机推断题 |
| 19 | 0.65 | 氯气的实验室制法 常见无机物的制备 常见气体的制备与收集 物质制备的探究 | 实验探究题 |
| 20 | 0.65 | 化学反应条件的控制及其应用 物质分离、提纯综合应用 物质制备的探究 电子转移计算 | 工业流程题 |



