2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷
广东
高三
开学考试
2017-07-27
352次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学反应原理、化学实验基础、常见无机物及其应用、物质结构与性质
2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷
广东
高三
开学考试
2017-07-27
352次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学反应原理、化学实验基础、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 化学与人们的日常生活密切相关,下列叙述正确的是
| A.聚乙烯塑料的老化是由于发生了加成反应 |
| B.乙酸乙酯在碱性条件下的水解反应称为皂化反应 |
| C.葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 |
| D.棉、麻、合成纤维完全燃烧都只生成CO2和H2O |
您最近一年使用:0次
2016-12-09更新
|
199次组卷
|
3卷引用:2016届天津市第一中学高三下学期第五次月考化学试卷
单选题
|
适中(0.65)
真题
名校
2. 下列有关实验操作的叙述错误的是
| A.过滤操作中,漏斗的尖端应接触烧杯内壁 |
| B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 |
| C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 |
| D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 |
您最近一年使用:0次
2019-01-30更新
|
1829次组卷
|
30卷引用:2016年全国普通高等学校招生统一考试化学(海南卷精编版)
2016年全国普通高等学校招生统一考试化学(海南卷精编版)2015-2016学年吉林长春外国语学校高二下期末理化学卷2015-2016学年吉林长春外国语高二下期末理科化学试卷2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷2017届内蒙古临河区巴彦淖尔一中高三上9月月考化学卷2017届上海市黄浦区高三下学期4月等级考调研测试化学试卷江西省赣中南五校2017届高三下学期期中联合考试化学试题福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题山东省潍坊市2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题十对接高考精练--化学实验常用仪器及基本操作新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题湖南省岳阳市第一中学2018届高三12月月考化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)解密16 化学实验基础(教师版)——备战2018年高考化学之高频考点解密甘肃省酒泉市敦煌中学2019届高三一诊化学试题2018-2019学年鲁科版高一化学必修一1.1走进化学科学练习题黑龙江省哈尔滨师范大学青冈实验中学校2016-2017学年高二下学期期末考试化学试题河南省驻马店经济开发区高级中学2019届高三上学期第一次月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点03 物质的量浓度及溶液的配制2016年全国普通高等学校招生统一考试化学(海南卷参考版)黑龙江省哈尔滨市第三中学2019-2020学年高二上学期期中考试化学(理)试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题6 化学实验复习题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题浙江省宁波市效实中学2018-2019学年高二下学期期中考试化学试题山东省日照市五莲县2020届高三9月模块诊断性测试化学试题(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)押全国卷理综第9题 化学实验基础-备战2021年高考化学临考题号押题(课标全国卷)湖南省永州市2021-2022学年高三上学期第一次适应性考试化学试题上海市曹杨第二中学2021-2022学年高二上学期期末考试化学试题(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)
单选题
|
适中(0.65)
名校
3. 下列有关说法正确的是
| A.当H2O与Na2O2反应生成1molO2时,转移的电子数目为2×6.02×1023 |
| B.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
C.常温下2S2O(g) 3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应 3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应 |
| D.氯水通入SO2后溶液的酸性减弱 |
【知识点】 二氧化硫的化学性质 化学反应进行方向的判据 酸碱中和滴定
您最近一年使用:0次
2016-08-26更新
|
213次组卷
|
5卷引用:2016届天津市第一中学高三下学期第五次月考化学试卷
单选题
|
适中(0.65)
解题方法
4. 下列实验对应的现象及结论均正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | SO2 通入氯化钡溶液,然后滴入稀硝酸 | 白色沉淀,白色沉淀不溶于稀硝酸 | 所得沉淀为BaSO3,后转化为BaSO4 |
| B | 浓硫酸滴入蔗糖中,并搅拌 | 得黑色蓬松的固体并有刺激性气味气体 | 该过程中浓硫酸仅体现吸水性和脱水性 |
| C | 向氯化亚铁溶液中加入足量的过氧化钠 | 出现红褐色沉淀和无色气体 | 氯化亚铁部分变质 |
| D | 向足量的淀粉碘化亚铁溶液中滴加氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
168次组卷
|
11卷引用:2016届吉林省东北师范大学附属中学高三上第三次模拟化学试卷
2016届吉林省东北师范大学附属中学高三上第三次模拟化学试卷2016届广东省松山湖学校、东莞一中高三上12月联考理综化学试卷2016届江苏省清江中学高三下学期2月月考化学试卷2016届江苏省百校高三下学期第一次联考化学试卷2015-2016学年陕西西藏民族学院附中高一下期末化学试卷2015-2016学年河北省唐山市开滦二中高二下期末化学试卷2017届广西南宁二中等三校高三上8月联考化学卷2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷2017届河北省武邑中学高三上学期第二次调研化学试卷2017届湖南省郴州市高三上第二次教学质量监测化学卷海南省华中师范大学海南附属中学2021届高三上学期第二次月考化学试题
单选题
|
较易(0.85)
5. 向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是
A.c( ) ) | B.c(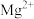 ) ) | C.c(H+) | D.Ksp(Mg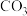 ) ) |
【知识点】 影响盐类水解程度的主要因素 难溶电解质的溶解平衡 沉淀溶解平衡的应用
您最近一年使用:0次
2016-12-09更新
|
1238次组卷
|
28卷引用:2016年全国普通高等学校招生统一考试化学(海南卷精编版)
2016年全国普通高等学校招生统一考试化学(海南卷精编版)2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷安徽省铜陵市第一中学2017-2018学年高二12月月考化学试题天津市和平区2017-2018学年高二上学期期末考试化学试题(已下线)《考前20天终极攻略》-5月23日 溶液中的离子平衡(已下线)解密13 沉淀溶解平衡——备战2018年高考化学之高频考点解密广东省蓝精灵中学2018-2019学年高二上学期联考化学试题(已下线)2018年11月18日 《每日一题》人教选修4-每周一测2016年全国普通高等学校招生统一考试化学(海南卷参考版)(已下线)2019年11月17日《每日一题》人教版(选修4)—— 每周一测吉林省吉林市普通高中2020届高三上学期第一次调研测试化学试题新疆维吾尔自治区石河子第二中学2019-2020学年高二上学期第二次月考化学试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训江苏省南京市南京师I范大学附属中学 2019-2020 学年高二下学期期中考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡(已下线)3.4.1 难溶电解质的沉淀溶解平衡(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)山西省运城市临猗县临晋中学2020-2021学年高二上学期12月月考化学试题广西桂林市第十八中学2020-2021学年高二下学期期中考试化学试题(已下线)3.4.1 难溶电解质的沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)云南省澄江市第一中学2021-2022年高二下学期3月月考化学试题云南省昆明师范专科学校附属中学2021-2022学年高二上学期期末考试化学试题陕西省延安市富县高级中学2021-2022学年高二上学期期中考试化学试题云南省玉龙纳西族自治县田家炳民族中学2021-2022学年高二上学期期中考试化学试题(已下线)第一部分 二轮专题突破 专题14 溶液中的三大平衡及应用甘肃省兰州第一中学2022-2023学年高二上学期期末考试化学试题江西省抚州创新实验学校2021-2022学年高二上学期期末考试化学试题
单选题
|
较难(0.4)
名校
6. 电-Fenton法是用于水体里有机污染物降解的高级氧化技术。其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2=Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
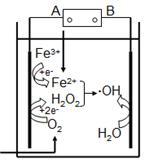

| A.电源的A极是负极 |
| B.电解池中只有O2、Fe3+发生还原反应 |
| C.阳极上发生电极反应:H2O-e-=·OH + H+ |
| D.消耗1molO2,可以产生4mol ·OH |
您最近一年使用:0次
2016-09-30更新
|
647次组卷
|
6卷引用:2016届浙江省宁波市高考模拟理综化学试卷
单选题
|
适中(0.65)
真题
名校
7. 已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定正确 的是( )
| A.原子半径:X>Y>Z>W |
| B.W的含氧酸的酸性比Z的含氧酸的酸性强 |
| C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性 |
| D.若W与X原子序数差为5,则形成化合物的化学式为X3W2 |
您最近一年使用:0次
2016-06-13更新
|
1218次组卷
|
31卷引用:2016年全国普通高等学校招生统一考试化学(上海卷精编版)
2016年全国普通高等学校招生统一考试化学(上海卷精编版)2015-2016学年吉林省松原市油田高中高一下期末化学试卷2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷2017届广东省中山一中高三上第二次统测化学试卷2016-2017学年陕西省西安市长安区第一中学高一(平行班)下学期第一次教学检测化学试卷2016-2017学年江西省奉新县第一中学高一下学期第一次月考化学试卷江苏省东台市2017届高三5月模拟化学试题安徽省师范大学附属中学2016-2017学年高一下学期期末考试化学试题河南省林州市第一中学2018届高三8月调研考试化学试题湖北省武汉市部分学校2018届高三9月起点调研考试化学试题江西省横峰中学、铅山一中、德兴一中2018届高三上学期第一次月考化学试题陕西省西北工业大学附属中学2018届高三第一次月考化学试题江西省铅山县第一中学2018届高三上学期第一次月考化学试题江苏省泰州中学2018届高三3月月度检测(二模模拟)化学试题广西桂林市第十八中学2017-2018学年高一下学期开学考试化学试题【全国百强校】江苏省南菁高级中学2017-2018学年高二上学期期中考试化学试题安徽省阜阳市临泉县第一中学2019届高三上学期第三次模拟(12月)化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)2016年全国普通高等学校招生统一考试化学(上海卷参考版)湖南省示范性高中江华一中2020年高考理科综测试化学试题(14)第2章 化学键与分子间作用力——C挑战区模拟高考(鲁科版选修3)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训吉林省长春市东北师大附中2020届高中毕业班四月份教学质量监测卷理科综合化学部分河北正定中学2019-2020学年高一下学期摸底考试化学试题(已下线)期末模拟卷(二)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)河北省保定市唐县第一中学2021-2022学年高二10月月考化学试题四川省江油市第一中学2021-2022学年高二上学期期中考试化学试题上海市风华中学2020-2021学年高三下学期第一次月考化学试题四川省成都市树德中学2022-2023学年高一下学期4月月考化学试题 四川省眉山市仁寿县2022-2023学年高一下学期5月期中联考化学试题湖北省武汉三牛中学2023-2024学年高一上学期期末考试 化学试卷
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 某实验小组用下图装置制备家用消毒液,并探究其性质。
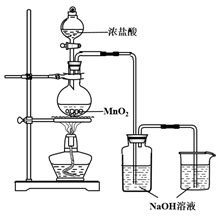
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
(1)写出利用上述装置制备消毒液涉及反应的化学方程式_________ 、________ 。
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
获得结论:此实验小组制备的消毒液具有________ 性。
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因:________ (用离子方程式表示)。
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是________ 。
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32-+ I2="==" S4O62-+ 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是________ 。
②此消毒液有效氯含量为________ %(保留一位有效数字)。获得结论:此实验制得的消毒液________ (填“符合”或“不符合”)家用要求。

反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
| 操作 | 现象 |
| a. 测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
| b. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(1)写出利用上述装置制备消毒液涉及反应的化学方程式
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作a中溶液褪色的原因,又补充了如下实验:
| 操作 | 现象 |
| 取 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有
(3) 该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降。
① 操作b中溶液变成黄绿色的原因:
② 有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是
(4) 有效氯的含量是检测含氯消毒剂消毒效果的重要指标。具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上。小组同学进行如下实验测定有效氯:取此消毒液5 g,加入20 mL 0.5 mol·L-1 KI溶液,10 mL 2 mol·L-1的硫酸溶液;加几滴淀粉溶液后,用0.1 mol·L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3 20 mL。(已知:2S2O32-+ I2="==" S4O62-+ 2I-) 。注:相对原子质量Cl35.5,Na23,S32,O 16 ,I 127, K39
①达到滴定终点时的实验现象是
②此消毒液有效氯含量为
【知识点】 化学实验探究 物质性质的探究解读 物质性质实验方案的设计解读
您最近一年使用:0次
2016-12-09更新
|
513次组卷
|
4卷引用:2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷
解答题-原理综合题
|
适中(0.65)
真题
解题方法
9. 铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72-的酸性废水通过铁炭混合物,在微电池正极上Cr2O72-转化为Cr3+,其电极反应式为_____________ 。
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如右图所示。
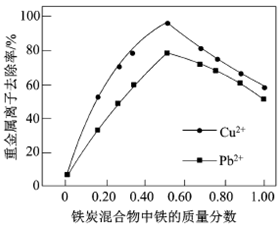
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是__________ 。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________ 。
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为_________________ 。
②纳米铁粉与水中NO3-反应的离子方程式为 4Fe+ NO3-+10H+=4Fe2++NH4++3H2O,研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是_________ 。
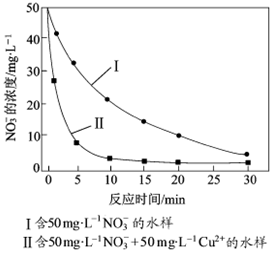
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见右图),产生该差异的可能原因是__________________ 。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72-的酸性废水通过铁炭混合物,在微电池正极上Cr2O72-转化为Cr3+,其电极反应式为
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如右图所示。

①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为
②纳米铁粉与水中NO3-反应的离子方程式为 4Fe+ NO3-+10H+=4Fe2++NH4++3H2O,研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见右图),产生该差异的可能原因是

您最近一年使用:0次
2016-12-09更新
|
1002次组卷
|
4卷引用:2016年全国普通高等学校招生统一考试化学(江苏卷精编版)
三、填空题 添加题型下试题
填空题
|
较难(0.4)
10. 运用化学反应原理分析解答以下问题:
(1)弱酸在水溶液中存在电离平衡,部分0.1 mol·L-1弱酸的电离平衡常数如下表:
①当弱酸的浓度一定时,降低温度,K值___________ (填“变大”“变小”或“不变”)。
②下列离子方程式和有关说法错误的是___________ 。
a.少量的CO2通入次氯酸钠溶液中:2ClO-+H2O+CO2=2HClO+CO
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO =2HCO
=2HCO +SO
+SO
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性。往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式:___________ 。
(2)工业废水中常含有一定量的Cr2O 和CrO
和CrO ,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放。
,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放。
①在废水中存在平衡:2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O。若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是
(橙色)+H2O。若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是___________ 。
a.平衡常数K值可以不改变
b.达到新平衡CrO 的消耗速率等于Cr2O
的消耗速率等于Cr2O 的消耗速率
的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O 和CrO
和CrO 最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)
最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol·L-1,溶液的pH调至4时,
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol·L-1,溶液的pH调至4时,___________ (填“有”或“没有”)沉淀产生。
(3)已知:①2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
②CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
③CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3,则该温度下反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)的化学平衡常数K=
CH3OCH3(g)+CO2(g)的化学平衡常数K=___________ (用含K1、K2、K3的代数式表示)。向某固定体积的密闭容器中加入3 mol CO和3 mol H2,充分反应后恢复至原温度,测定容器的压强为反应前的1/2,则CO的转化率为___________ 。
(1)弱酸在水溶液中存在电离平衡,部分0.1 mol·L-1弱酸的电离平衡常数如下表:
| 弱酸 | 电离平衡常数(25 ℃) |
| HClO | K=2.98×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| H2SO3 | K1=1.54×10-2 K2=1.02×10-7 |
①当弱酸的浓度一定时,降低温度,K值
②下列离子方程式和有关说法错误的是
a.少量的CO2通入次氯酸钠溶液中:2ClO-+H2O+CO2=2HClO+CO

b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO
 =2HCO
=2HCO +SO
+SO
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性。往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式:
(2)工业废水中常含有一定量的Cr2O
 和CrO
和CrO ,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放。
,它们对人类及生态系统会产生很大损害,必须进行处理后方可排放。①在废水中存在平衡:2CrO
 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O (橙色)+H2O。若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是
(橙色)+H2O。若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是a.平衡常数K值可以不改变
b.达到新平衡CrO
 的消耗速率等于Cr2O
的消耗速率等于Cr2O 的消耗速率
的消耗速率c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O
 和CrO
和CrO 最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)
最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol·L-1,溶液的pH调至4时,
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的Ksp=10-32,当c(Cr3+)降至10-3 mol·L-1,溶液的pH调至4时,(3)已知:①2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)②CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)③CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)某温度下三个反应的平衡常数的值依次为K1、K2、K3,则该温度下反应3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g)的化学平衡常数K=
CH3OCH3(g)+CO2(g)的化学平衡常数K=
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-有机推断题
|
困难(0.15)
名校
11. [化学——选修5:有机化学基础]
PVB(聚乙烯醇缩丁醛)和PI(聚异戊二烯)均为用途广泛的有机制品,用乙炔为原料制备PVB和PI的流程如图。
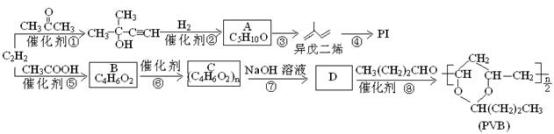
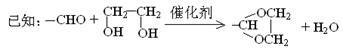
(1)A中的官能团名称是________________ 。反应③的条件是_________________ 。
(2)已知反应⑤属于加成反应,上述转化中还有____________ (填序号)也属于该反应类型。
(3)E是A的同分异构体,E的核磁共振氢谱显示有2种不同化学环境的氢,且E能发生银镜反应E发生银镜反应的化学方程式是_________________________ 。
(4)反应⑦的化学方程式是_________________________ 。
(5)依照PI的合成路线,若将反应①中的反应物“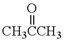 ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是__________________ 。
(6) ,以
,以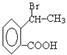 为原料合成
为原料合成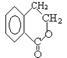 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。

PVB(聚乙烯醇缩丁醛)和PI(聚异戊二烯)均为用途广泛的有机制品,用乙炔为原料制备PVB和PI的流程如图。

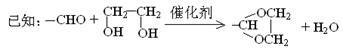
(1)A中的官能团名称是
(2)已知反应⑤属于加成反应,上述转化中还有
(3)E是A的同分异构体,E的核磁共振氢谱显示有2种不同化学环境的氢,且E能发生银镜反应E发生银镜反应的化学方程式是
(4)反应⑦的化学方程式是
(5)依照PI的合成路线,若将反应①中的反应物“
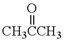 ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是(6)
 ,以
,以 为原料合成
为原料合成 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式。
您最近一年使用:0次
2016-12-09更新
|
693次组卷
|
2卷引用:2017届广东省蕉岭县蕉岭中学高三上学期开学考试化学试卷
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、化学反应原理、化学实验基础、常见无机物及其应用、物质结构与性质
试卷题型(共 11题)
题型
数量
单选题
7
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 胶体的性质和应用 油脂在碱性条件下水解 淀粉和纤维素 塑料的老化和降解 | |
| 2 | 0.65 | 酸碱中和滴定实验相关仪器 仪器使用与实验安全 一定物质的量浓度的溶液的配制 化学实验基础操作 | |
| 3 | 0.65 | 二氧化硫的化学性质 化学反应进行方向的判据 酸碱中和滴定 | |
| 4 | 0.65 | 氯气与还原性化合物的反应 二氧化硫与其他强氧化剂的反应 浓硫酸的脱水性 过氧化钠的强氧化性 | |
| 5 | 0.85 | 影响盐类水解程度的主要因素 难溶电解质的溶解平衡 沉淀溶解平衡的应用 | |
| 6 | 0.4 | 电化学计算 电解原理的应用 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.65 | 元素周期律、元素周期表的推断 金属与非金属在周期表中位置及其性质递变的规律 “位构性”关系理解及应用 | |
| 二、解答题 | |||
| 8 | 0.65 | 化学实验探究 物质性质的探究 物质性质实验方案的设计 | 实验探究题 |
| 9 | 0.65 | 离子方程式的书写 影响化学反应速率的因素 原电池电极反应式书写 | 原理综合题 |
| 11 | 0.15 | 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 10 | 0.4 | 化学平衡 弱电解质的电离 | |



