四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
四川
高三
阶段练习
2021-04-01
1037次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学反应原理、化学与STSE、物质结构与性质、化学实验基础
四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
四川
高三
阶段练习
2021-04-01
1037次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学反应原理、化学与STSE、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸( )、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法正确的是
)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法正确的是
 )、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法正确的是
)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法正确的是| A.次氯酸钠稀溶液可用作公用餐具的消毒剂 |
| B.乙醚、乙醇、漂白粉、过氧乙酸、氯仿均为非电解质 |
| C.酒精溶液、含氯消毒剂的浓度越高,其消毒效果越好 |
| D.75%乙醇、过氧乙酸均通过氧化灭活病毒 |
您最近一年使用:0次
2020-12-19更新
|
567次组卷
|
4卷引用:湖北省荆州市2021届高三上学期第一次质量检查化学试题
湖北省荆州市2021届高三上学期第一次质量检查化学试题(已下线)热点1 化学与STSE-2021年高考化学【热点·重点·难点】专练(山东专用)四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题江西省景德镇市景德镇一中2022届高三10月月考化学试题
单选题
|
适中(0.65)
名校
2. 下列有关说法不正确的是
| A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.铅蓄电池在放电过程中,负极和正极质量均增加 |
| C.在硫酸型酸雨地区,不纯的铜发生电化学腐蚀,正极反应为:O2 + 4e- + 4H+ = 2H2O |
| D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe - 2e- = Fe2+ |
您最近一年使用:0次
2017-07-10更新
|
398次组卷
|
6卷引用:吉林省辽源市第五中学2016-2017学年高一下学期第二次月考化学试题
单选题
|
适中(0.65)
名校
3. 用惰性电极电解下列溶液,电解一段时间后,电解液的pH不变的是
| A.H2SO4 | B.Na2SO4 | C.AgNO3 | D.KOH |
【知识点】 根据电解产物进行相关推断解读 电解过程中溶液pH的变化解读
您最近一年使用:0次
2018-10-16更新
|
180次组卷
|
3卷引用:【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题
单选题
|
适中(0.65)
真题
名校
4. 下列能量转化过程与氧化还原反应无关的是
| A.硅太阳能电池工作时,光能转化成电能 |
| B.锂离子电池放电时,化学能转化成电能 |
| C.电解质溶液导电时,电能转化成化学能 |
| D.葡萄糖为人类生命活动提供能量时,化学能转化成热能 |
【知识点】 氧化还原反应的应用
您最近一年使用:0次
2017-11-25更新
|
2384次组卷
|
56卷引用:河北省安平中学2016-2017学年高二下学期期末考试化学试题
河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(天津卷精编版)浙江省嘉兴市第一中学2017-2018学年高二上学期期中考试化学试题河南省洛阳市2018届高三上学期第一次质量预测(1月)化学试题河南省郑州市2018届高三高中毕业班第一次质量检测(模拟)化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.4 氧化还原反应安徽省池州一中(贵池中学)2017-2018学年高一下学期期中质量检测化学试题(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密(已下线)学科网2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【教学案】山西省临猗县临晋中学2019届高三9月月考化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题【校级联考】福建省晋江市(安溪一中、养正中学、惠安一中、泉州实验中学四校)2018-2019学年高二上学期期中考试化学试题【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (教学案)(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)河南省郑州市实验中学2019届高三上学期期中考试化学试题(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点河北省易县中学2018-2019学年高二下学期期末考试化学试题(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》黑龙江省龙东南联合体2018-2019学年高二下学期期末考试化学试题福建省莆田九中2019-2020学年高二上学期期中考试化学试题福建省莆田第七中学2020届高三上学期期中复习检测化学试题2福建省厦门市思明区厦门外国语学校2019-2020学年高三上学期周末练习12——化学试题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题天津市海河中学2020届高三第二学期化学测试(二)试卷河北省保定市2019-2020学年高二上学期期末调研考试化学试题江苏省宿迁市沭阳县修远中学2019-2020学年高二下学期4月月考化学试题(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分河北省衡水中学2020届高三下学期二月份网络教学质量监测理科综合化学试题湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学(已下线)【南昌新东方】2019-2020 雷氏中学 高一下 周练(已下线)2.3.1 认识氧化还原反应 氧化剂和还原剂练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)高一必修第二册(人教2019版)第六章 化学反应与能量 素养检测黑龙江省大庆市让胡路区大庆铁人中学2021届高三上学期阶段考试化学试题(已下线)高中化学苏教2019版必修第二册-专题6 第三单元综合拔高练青海省西宁市普通高中五校2020-2021学年高三上学期期末联考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题天津市河北区2021届高三一模考试化学试题(已下线)押山东卷第02题 氧化还原反应在生产生活中的应用-备战2021年高考化学临考题号押题(山东卷)甘肃省武威市民勤县第四中学2020-2021学年高二下学期期中考试化学(普通班)试题江西省景德镇一中2020-2021学年高一下学期期末考试化学试题(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)江苏省宿迁市泗阳县实验高级中学2021-2022学年高一下学期第一次月考化学试题福建省莆田第一中学2021-2022学年高二上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题山东省滨州市沾化区实验高级中学2022-2023学年高三10月月考化学试题河北保定市唐县田家炳中学2021-2022学年高三上学期11月化学试题(已下线)江苏省南通市如皋市2022-2023学年高三上学期期末考试化学试题
单选题
|
容易(0.94)
名校
解题方法
5. 下列说法中不正确的是
| A.铜在酸性环境中易发生析氢腐蚀 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| C.用锡焊接的铁质器件,焊接处易生锈 |
| D.在船体外嵌入锌块,可以减缓船体的腐蚀,属于牺牲阳极的阴极保护法 |
【知识点】 金属的电化学腐蚀与防护 金属的防护解读 金属腐蚀与防护解读
您最近一年使用:0次
单选题
|
容易(0.94)
6. NA为阿伏加 德罗常数的值,下列说法正确的是
| A.1L0.1 mol·L-1NaClO溶液中含有的ClO-数目为NA |
| B.在电解精炼粗铜的过程中,当阴极质量增重32g时转移的电子数为NA |
| C.常温常压下,1 mol分子式为C2H6O的有机物中含有C-O键的数目为NA |
| D.氢氧燃料电池正极消耗22.4 L气体时,负极消耗气体的分子数为2NA |
您最近一年使用:0次
2020-08-03更新
|
290次组卷
|
2卷引用:四川省绵阳市2019-2020学年高二下学期期末教学质量测试化学试题
单选题
|
适中(0.65)
名校
7. 下列说法正确的是
| A.pH=1的醋酸加水稀释到原体积的100 倍,稀释后 pH=3 |
| B.室温下 pH 相同的 NH4Cl 溶液和CH3COOH 溶液,由水电离产生的 c(H+)相同 |
| C.室温下pH=3的醋酸溶液和 pH=11的 Ba(OH)2 溶液等体积混合后溶液呈酸性 |
| D.某温度下,水的离子积常数为 1×10-12,该温度下 pH=7的溶液呈中性 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
8. 为达到相应实验目的,下列实验设计可行的是
| 编号 | 实验目的 | 实验过程 |
| A | 探究浓度对反应速率的影响 | 向 2 支盛有 2mL 0.01mol/L 酸性 KMnO4溶液的试管中分别加入 2mL 0.1mol/L 和 1mL 0.2mol/L的 H2C2O4 溶液,观察溶液褪色所需时间 |
| B | 证明碳酸酸性强于硼酸 | 向饱和碳酸氢钠溶液中滴加少量的硼酸溶液,无气泡产生 |
| C | 证明 Ksp[Fe(OH)3])<Ksp[Mg(OH)2] | 向 盛 有 1mL0.1mol/LMgCl2溶液中滴加1mL0.4mol/LNaOH 溶液,有白色沉淀出现,再滴加 2滴 0.1mol/LFeCl3,静止,有红棕色沉淀出现 |
| D | 除去碱式滴定管内的气泡 | 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-03-31更新
|
248次组卷
|
2卷引用:四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 下列反应的离子方程式书写正确的是
A.向 Na2CO3 溶液中通入过量 SO2: |
B.用铁电极电解饱和MgCl2 溶液:MgCl2+2H2O Mg(OH)2↓+Cl2↑+H2↑ Mg(OH)2↓+Cl2↑+H2↑ |
| C.向 FeBr2 溶液中通入过量 Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
D.向NaHSO4 溶液中逐滴加入 Ba(OH)2 溶液至溶液呈中性:2H++SO +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
10. 下列说法不正确的是
| A.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)⇌Mg2+(aq)+2OH-,该固体可溶于NH4Cl溶液 |
| B.向ZnS沉淀上滴加CuSO4溶液沉淀变为黑色,可推知同温下Ksp(ZnS)<Ksp(CuS) |
| C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色,反应的离子方程式为:2AgCl(s)+S2-(aq)⇌Ag2S(s)+2Cl-(aq) |
| D.向2mL浓度均为1.2 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1的AgNO3溶液,振荡沉淀呈黄色,说明Ksp(AgCl)>Ksp(AgI) |
【知识点】 难溶电解质的溶解平衡 沉淀溶解平衡的应用
您最近一年使用:0次
2021-01-07更新
|
393次组卷
|
10卷引用:湖南省长沙市南雅中学2020-2021学年高二上学期第三次月考化学试题
湖南省长沙市南雅中学2020-2021学年高二上学期第三次月考化学试题四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题浙江省山河联盟2021-2022学年高二上学期12月考试化学试题(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期末考试化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题上海市控江中学2023-2024学年高二上学期等级班阶段测验卷二 化学试题山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题山东省百师联盟2023-2024学年高二上学期12月大联考化学试题
单选题
|
适中(0.65)
名校
11. 根据下图判断,下列说法正确的是
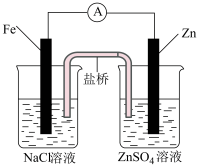 | 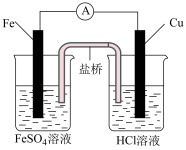 |
| Ⅰ | Ⅱ |
A.装置Ⅰ和装置Ⅱ中负极反应均是 |
B.装置Ⅰ和装置Ⅱ中正极反应均是 |
| C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动 |
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的 均增大 均增大 |
您最近一年使用:0次
2023-10-11更新
|
271次组卷
|
25卷引用:2012届河南省郑州市高三第一次质量预测化学试卷
(已下线)2012届河南省郑州市高三第一次质量预测化学试卷(已下线)2015届辽宁省大连二十中高三上学期期中化学试卷2016届湖南省浏阳市第一中学高三上学期第二次月考化学试卷2016届广西钦州港经济技术开发区中学高三上学期第二次月考化学试卷2016届山东省菏泽市高三上学期期末考试化学试卷2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷福建省泉州市泉港区第一中学2017-2018学年高二上学期期中考试化学试题(已下线)2018年9月13日 《每日一题》一轮复习-原电池工作原理以及正、负极的判定(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点(已下线)2019年9月12日《每日一题》2020年一轮复习—— 原电池工作原理以及正、负极的判定(已下线)考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 教材帮(已下线)第20讲 原电池 化学电源(精练)-2021年高考化学一轮复习讲练测四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题福建省莆田第二中学2020-2021学年高二上学期期中考试化学试题(已下线)第16讲 原电池 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)广西壮族自治区贺州市2021-2022学年高二上学期期末考试化学试题山东省德州市2020-2021学年高二上学期反应原理月考(A)化学试题(已下线)第16讲 原电池 新型电源 (练)-2023年高考化学一轮复习讲练测(新教材新高考)河北省邯郸市魏县旭日中学2021-2022学年高二上学期期中考试化学试题重庆市巫山县官渡中学2021-2022学年高二下学期期末考试化学试题黑龙江省牡丹江市阳明区2022-2023学年高三上学期第四次阶段考试化学试题山东省青岛第二中学2020-2021学年高二上学期期中考试化学试题山东省青岛第二中学2021-2022学年高二上学期10月月考化学试题重庆市育才中学校2023-2024学年高二上学期三校联考模拟考化学试题(平行班)
单选题
|
适中(0.65)
名校
解题方法
12. X、Y、Z和W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y、W均相邻;Y、Z和W三种元素的原子最外层电子数之和为17.则下列有关叙述正确的是
A.两化合物均由X、Y、Z和W四种元素组成且它们的水溶液能发生化学反应,则反应的离子方程式为:H++ =SO2↑+H2O =SO2↑+H2O |
| B.上述元素形成的氢化物中,W的氢化物相对分子质量最大,熔沸点最高 |
| C.Y和W分别形成的含氧酸均为强酸,是离子化合物 |
| D.Y、Z和W三种元素可能位于同一周期 |
【知识点】 元素周期律、元素周期表的推断 “位构性”关系理解及应用解读
您最近一年使用:0次
2020-11-08更新
|
185次组卷
|
3卷引用:四川省遂宁市安居区2020-2021学年高二上学期期中考试化学试题
13. 铬酸银(Ag2CrO4)微溶于水,作化学试剂。常用作分析试剂,有机合成催化剂,电镀,卤化物滴定确定终点的指示剂等。在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10−10。下列说法不正确的是
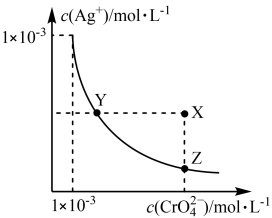

| A.t℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 |
| C.t℃时,Ag2CrO4的Ksp为1×10−8 |
| D.t℃时,将0.01 mol·L−1 AgNO3溶液滴入20 mL 0.01 mol·L−1 KCl和0.01 mol·L−1 K2CrO4的混合溶液中,Cl-先沉淀 |
您最近一年使用:0次
2020-11-24更新
|
1027次组卷
|
6卷引用:山东省聊城市2020-2021学年高二上学期期中考试化学试题
山东省聊城市2020-2021学年高二上学期期中考试化学试题(已下线)本册综合检测(二)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)广东省深圳市龙华区2020-2021学年高二上学期期末检测化学试题四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题江西赣州市2022~2023学年高二上学期期末考试化学试题河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题
单选题
|
适中(0.65)
名校
14. 镁原子电池放电时电压高而平稳,电池反应为xMg + Mo3S4 MgxMo3S4,下列说法错误的是
MgxMo3S4,下列说法错误的是
 MgxMo3S4,下列说法错误的是
MgxMo3S4,下列说法错误的是| A.放电时负极反应为Mg-2e-===Mg2+ |
| B.充电时阳极反应为Mo3S4+xMg2++2xe-===MgxMo3S4 |
| C.放电时Mg2+向正极区移动 |
| D.充电时电池的负极接充电电源的负极 |
您最近一年使用:0次
2018-10-16更新
|
301次组卷
|
4卷引用:2013-2014学年江西省南昌市四校高二上学期期末联考化学试卷
(已下线)2013-2014学年江西省南昌市四校高二上学期期末联考化学试卷2018-2019学年鲁科版高中化学选修四:第1章检测题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
15. 如图所示的装置,X、Y 都是惰性电极。将电源接通后,向(甲)中滴入酚酞溶液,在 Fe 极附近显红色。试回答下列问题:

(1)在电源中,B 电极为_______ 极(填电极名称,下同);丙装置中Y 电极为_______ 极。
(2)丙装置在通电一段时间后,X 电极上发生的电极反应式是_______ 。
(3)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为_______ L。
(4)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为_______ 。

(1)在电源中,B 电极为
(2)丙装置在通电一段时间后,X 电极上发生的电极反应式是
(3)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为
(4)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
名校
解题方法
16. (I)电池在生产和生活中应用极其广泛,根据电化学原理回答下列问题。
(1)微型纽扣电池总反应为 Ag2O+Zn+H2O=Zn(OH)2+2Ag,电解质溶液为 KOH 溶液, 则负极材料为_______ ,正极的电极反应式为_______ 。
(2)甲醇(CH3OH)燃料电池为绿色化学电源,以NaOH溶液为电解质溶液时,负极的电极反应式为_______ ,该电池工作时,外电路每流过1×103mol e-,消耗标准状况下的 O2_______ m3。
(II)图表示几种难溶氢氧化物在不同 pH下的溶解度(S/mol·L-1)。回答下列问题:

(3)向 Cu(OH)2悬浊液中滴加饱和 FeCl3 溶液,反应的离子方程式为_______ , 已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.0×10-20,该反应的平衡常数 K=_______ 。
(1)微型纽扣电池总反应为 Ag2O+Zn+H2O=Zn(OH)2+2Ag,电解质溶液为 KOH 溶液, 则负极材料为
(2)甲醇(CH3OH)燃料电池为绿色化学电源,以NaOH溶液为电解质溶液时,负极的电极反应式为
(II)图表示几种难溶氢氧化物在不同 pH下的溶解度(S/mol·L-1)。回答下列问题:

(3)向 Cu(OH)2悬浊液中滴加饱和 FeCl3 溶液,反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
17. 铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态 Fe 原子的外围电子排布图为_______ ,基态 Fe2+中,核外电子占据最高能层的符号是_______ 。
(2)Fe3+可以与 SCN-形成一系列不同配位数的红色配合物,所以常用 KSCN 溶液检验 Fe3+ 的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN-的几何 构型为_______ ,中心原子的杂化类型为_______ 。
(3)实验中常用 K3[Fe(CN)6]检验 Fe2+,K3[Fe(CN)6]晶体中的化学键有_______ (填写选项字母)1molK3[Fe(CN)6]中含有 σ 键与π键的数目比为_______ 。
a.离子键 b.共价键 c.氢键 d .配位键 e.金属键
(4)FexO 为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度 ρ=_______ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。(列出计算式)
(1)基态 Fe 原子的外围电子排布图为
(2)Fe3+可以与 SCN-形成一系列不同配位数的红色配合物,所以常用 KSCN 溶液检验 Fe3+ 的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用 K3[Fe(CN)6]检验 Fe2+,K3[Fe(CN)6]晶体中的化学键有
a.离子键 b.共价键 c.氢键 d .配位键 e.金属键
(4)FexO 为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度 ρ=
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
名校
解题方法
18. 化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效广谱的灭菌消毒剂。某化学小组针对氯气及其化合物展开以下实验。
Ⅰ.氯碱工业是工业上制备氯气的主要方法,该实验小组采用如图所示的装置来模拟工业制取氯气。回答下列问题:

(1)氯气的逸出口是_______ (填“a”或“b”),为了获得比较纯净的 NaOH 溶液,电解过程中最好选用离子交换膜________ (填“阴”或“阳”),电解过程总反应的离子方程式为_______
Ⅱ.“84”消毒液是生活中常见的高效杀毒剂,其主要成分为 NaClO。某校学生为了测定蓝月亮牌“84”消毒液中 NaClO 的浓度,进行了如下实验:
①取 10.00ml “84”消毒液于烧杯中,加水稀释并恢复至室温后,转移到 1000ml 容量瓶中定容后备用。
②取 20.00ml 稀释后的溶液于锥形瓶中,滴加稀 H2SO4和过量的 KI 溶液,NaClO 将 KI 氧化成 I2。
③用淀粉做指示剂,生成的I2用0.0800 mol/L Na2S2O3标准溶液滴定至终点,发生的反应为:I2 + 2S2O =2I-+S4O
=2I-+S4O 。
。
④重复滴定 4 次。所得数据如表:
回答下列问题:
(2)步骤①定容时还需要的玻璃仪器是_______ 。
(3)步骤②发生反应的离子方程式为_______
(4)步骤③滴定终点的现象为_______
(5)若滴定前标准液滴定管尖嘴管处有气泡,滴定结束后气泡消失,则会使测定结果_______ (填“偏高”或“偏低”或“不变”)。经过计算测出蓝月亮牌“84”消毒液中 NaClO的物质的量浓度为_______ mol/L(精确到小数点后 2 位)
Ⅰ.氯碱工业是工业上制备氯气的主要方法,该实验小组采用如图所示的装置来模拟工业制取氯气。回答下列问题:

(1)氯气的逸出口是
Ⅱ.“84”消毒液是生活中常见的高效杀毒剂,其主要成分为 NaClO。某校学生为了测定蓝月亮牌“84”消毒液中 NaClO 的浓度,进行了如下实验:
①取 10.00ml “84”消毒液于烧杯中,加水稀释并恢复至室温后,转移到 1000ml 容量瓶中定容后备用。
②取 20.00ml 稀释后的溶液于锥形瓶中,滴加稀 H2SO4和过量的 KI 溶液,NaClO 将 KI 氧化成 I2。
③用淀粉做指示剂,生成的I2用0.0800 mol/L Na2S2O3标准溶液滴定至终点,发生的反应为:I2 + 2S2O
 =2I-+S4O
=2I-+S4O 。
。④重复滴定 4 次。所得数据如表:
| 待测液体积 (ml) | 标准液滴定前 读数(ml) | 标准液滴定 后读数(ml) | 消耗标准液体 积(ml) | |
| 1 | 20.00 | 0.02 | 20.02 | |
| 2 | 20.00 | 0.24 | 20.26 | |
| 3 | 20.00 | 0.12 | 20.10 | |
| 4 | 20.00 | 0.20 | 21.20 |
(2)步骤①定容时还需要的玻璃仪器是
(3)步骤②发生反应的离子方程式为
(4)步骤③滴定终点的现象为
(5)若滴定前标准液滴定管尖嘴管处有气泡,滴定结束后气泡消失,则会使测定结果
【知识点】 酸碱中和滴定原理的应用解读 氯碱工业解读
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
名校
解题方法
19. Mg(OH)2可用作塑料的阻燃剂。现以某矿石(主要成分为 3MgO·2SiO2·2H2O,还有少量 Fe2O3、FeO、CaO 和Al2O3)为原料生产 Mg(OH)2,其工艺流程如图:
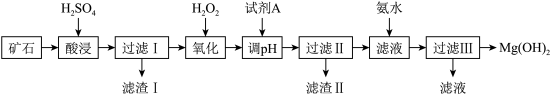
已知:生成氢氧化物沉淀的 pH
回答下列问题:
(1)酸浸时,为提高矿石的浸出率可采取的措施为_______ (任写一条)。该过程H2SO4适当过量的目的除了使固体充分溶解外还有_______
(2)写出氧化过程加H2O2发生反应的离子方程式_______
(3)为了提高产品纯度加入试剂A 为_______ (填化学式),为控制 Mg2+浓度为1.0mol/L,调节溶液 pH 范围为_______ ;得到滤渣 II 的成分是_______ (填化学式)
(4)实际生产中,可由 Mg(OH)2为原料制备单质镁,请写出制备过程中涉及氧化还原的方程式方法_______ 。

已知:生成氢氧化物沉淀的 pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的 pH | 7.6 | 1.9 | 3.4 | 9.0 |
| 完全沉淀的 pH (c=1.0×10-5 mol/L) | 9.6 | 3.2 | 4.8 | 11.1 |
(1)酸浸时,为提高矿石的浸出率可采取的措施为
(2)写出氧化过程加H2O2发生反应的离子方程式
(3)为了提高产品纯度加入试剂A 为
(4)实际生产中,可由 Mg(OH)2为原料制备单质镁,请写出制备过程中涉及氧化还原的方程式方法
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、化学反应原理、化学与STSE、物质结构与性质、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
14
填空题
1
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 电解质与非电解质 蛋白质的变性 | |
| 2 | 0.65 | 浓度对化学反应速率的影响 原电池原理的应用 析氢腐蚀 吸氧腐蚀 | |
| 3 | 0.65 | 根据电解产物进行相关推断 电解过程中溶液pH的变化 | |
| 4 | 0.65 | 氧化还原反应的应用 | |
| 5 | 0.94 | 金属的电化学腐蚀与防护 金属的防护 金属腐蚀与防护 | |
| 6 | 0.94 | 22.4L/mol适用条件 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 7 | 0.65 | 溶液pH的计算 水溶液中水的电离程度及的计算 酸碱混合时的定性判断及计算 浓度对电离平衡的影响 | |
| 8 | 0.65 | 浓度对化学反应速率的影响 酸碱中和滴定实验基本操作及步骤 沉淀转化 | |
| 9 | 0.65 | 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 电解池电极反应式及化学方程式的书写与判断 | |
| 10 | 0.65 | 难溶电解质的溶解平衡 沉淀溶解平衡的应用 | |
| 11 | 0.65 | 原电池原理的应用 原电池正负极判断 | |
| 12 | 0.65 | 元素周期律、元素周期表的推断 “位构性”关系理解及应用 | |
| 13 | 0.85 | 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积定义及表达式 溶度积常数相关计算 | |
| 14 | 0.65 | 新型电池 其他二次电池 原电池、电解池综合考查 | |
| 二、填空题 | |||
| 15 | 0.65 | 电解池电极反应式及化学方程式的书写与判断 铜的电解精炼 利用电子守恒法进行多池串联相关计算 | |
| 三、解答题 | |||
| 16 | 0.4 | 溶度积常数相关计算 原电池电极反应式书写 甲醇燃料电池 原电池有关计算 | 原理综合题 |
| 17 | 0.65 | 元素性质与电负性的关系 杂化轨道理论 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 18 | 0.4 | 酸碱中和滴定原理的应用 氯碱工业 | 实验探究题 |
| 19 | 0.4 | 溶度积常数相关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |



