2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分
湖南
高三
阶段练习
2020-05-18
489次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分
湖南
高三
阶段练习
2020-05-18
489次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
真题
名校
1. 与氢硫酸反应有沉淀生成的电解质是
| A.硫酸铜 | B.氢氧化钠 | C.硫酸亚铁 | D.二氧化硫 |
您最近一年使用:0次
2016-12-09更新
|
1739次组卷
|
16卷引用:2015年全国普通高等学校招生统一考试化学(上海卷)
2015年全国普通高等学校招生统一考试化学(上海卷)2015-2016学年河北省唐山一中高二下期末化学试卷2016-2017学年河北省武邑中学高一下学期第一次月考化学试卷苏教版2017届高三单元精练检测四化学试题黑龙江省大庆中学2017届高三上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化 第2讲 离子反应和离子方程式【教学案】(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第4讲 用途广泛的金属材料及开发利用金属矿物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】(已下线)2019届高考热点题型和提分秘籍 第二章 化学物质及其变化 第2讲 离子反应 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (教学案)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)鲁教版高中化学必修1第三章《自然界中的元素》测试卷1湖南省长沙市长郡中学2020届高三4月份教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开区2022-2023学年高三下学期质量检测(一)化学试题
单选题
|
较难(0.4)
真题
名校
2.  为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是
 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A.0.1 mol 的 中,含有 中,含有 个中子 个中子 |
B.pH=1的H3PO4溶液中,含有 个 个 |
C.2.24L(标准状况)苯在O2中完全燃烧,得到 个CO2分子 个CO2分子 |
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加 个P-Cl键 个P-Cl键 |
您最近一年使用:0次
2017-08-08更新
|
10722次组卷
|
36卷引用:河北省安平中学2016-2017学年高二下学期期末考试化学试题
河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)(已下线)【中等生百日捷进提升系列-技能方法】专题03 阿伏加德罗常数类选择题解题方法和策略(已下线)《考前20天终极攻略》-5月17日 阿伏加德罗常数的相关判断与计算(已下线)解密02 化学常用计量——备战2018年高考化学之高频考点解密安徽省皖中地区2019届高三入学摸底考试化学试题(已下线)学科网2019年高考化学一轮复习讲练测1.1 物质的量 气体摩尔体积 练辽宁省葫芦岛市第六中学2019届高三上学期开学考试(8月)化学试题甘肃省甘谷县第一中学2019届高三上学期第一次检测考试化学试题(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第1讲 物质的量、气体摩尔体积【教学案】山东省临沂市第十九中学2019届高三上学期第三次质量调研考试化学试题四川省攀枝花市第十二中学2019届高三上学期10月月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点02 物质的量(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第1讲 物质的量 气体摩尔体积 (教学案)(已下线)2019高考备考二轮复习精品资料-专题2 化学常用计量(教学案)(已下线)2019年高考总复习巅峰冲刺-专题02 阿佛加德罗常数应试策略河北省邯郸市大名县第一中学2018-2019学年高二(清北班)5月月考化学试题(已下线)2019年7月7日 《每日一题》 2020年高考一轮复习-每周一测辽宁省阜新市第二高级中学2018-2019学年高二下学期期末考试化学试题百所名校联考-从实验学化学(已下线)专题1.1 物质的量 气体摩尔体积(练)-《2020年高考一轮复习讲练测》黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期末考试化学试题黑龙江省宾县一中2020届高三上学期第一次月考化学试题新疆霍城县江苏中学2019届高三第二次模拟考试化学试题云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题河北省石家庄市第二中学2020届高三下学期教学质量检测模拟考试理综化学试题河北省承德市第一中学2019-2020学年高二下学期3月疫情期间直播课堂检测化学试题(已下线)专题三 化学常用计量与阿伏加德罗常数(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分西藏自治区拉萨市拉萨中学2020届高三第七次月考试理综化学试题广西北流市实验中学2019-2020学年高二下学期期中考试理科综合化学试题(已下线)专题讲座(一) 阿伏加德罗常数的突破(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)山西省运城市稷山中学2022届高三上学期月考(一)化学试题云南省罗平县第五中学2021-2022学年高二下学期6月月考化学试题四川省成都市树德中学2022-2023学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
3. 常温下,下列各组离子在指定溶液中能大量共存的是
| A.无色透明的溶液中: Fe3+、Mg2+、SCN −、Cl − |
B. =1×10-12的溶液中:K+、Na+、CO32−、NO3− =1×10-12的溶液中:K+、Na+、CO32−、NO3− |
C.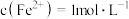 的溶液中: K+、NH4+、MnO4−、SO42- 的溶液中: K+、NH4+、MnO4−、SO42- |
| D.能使甲基橙变红的溶液中: Na+、NH4+、SO42-、HCO3- |
【知识点】 限定条件下的离子共存解读
您最近一年使用:0次
2019-12-02更新
|
591次组卷
|
29卷引用:河北省定州中学2018届高三上学期第一次调研化学试题
河北省定州中学2018届高三上学期第一次调研化学试题黑龙江省哈尔滨市第十八中学2018届高三第一次月考化学试题宁夏六盘山高级中学2018届高三上学期第一次月考化学试题河南省林州市第一中学2018届高三10月调研化学试题山东省淄博第一中学2018届高三上学期开学考试化学试题天津市耀华中学2018届高三上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题2019届高考化学一轮复习离子反应(已下线)学科网2019年高考化学一轮复习讲练测 2.2 离子反应 离子共存及检验 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化 第2讲 离子反应和离子方程式【教学案】山东省淄博市淄川中学2019届高三上学期10月月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期期中考试化学试题河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题陕西省吴起高级中学2018-2019学年高二下学期第二次月考化学试题(已下线)专题2.2 离子反应 离子共存及检验(练)-《2020年高考一轮复习讲练测》四川省成都实验高级中学2020届高三上学期入学考试化学试题黑龙江省宾县一中2020届高三上学期第一次月考化学试题云南省南华县一中2020届高三上学期开学考试化学试题甘肃省临夏回族自治州积石山县移民中学2019-2020学年高三上学期期中考试化学试题重庆市万州新田中学2019-2020学年高二上学期期中考试化学试题2020届高三化学大二轮增分强化练——离子共存(已下线)专题五 离子反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训天津市实验中学2020届高三下学期4月第一次测试化学试题(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学
单选题
|
适中(0.65)
真题
名校
4. 下列能量转化过程与氧化还原反应无关的是
| A.硅太阳能电池工作时,光能转化成电能 |
| B.锂离子电池放电时,化学能转化成电能 |
| C.电解质溶液导电时,电能转化成化学能 |
| D.葡萄糖为人类生命活动提供能量时,化学能转化成热能 |
【知识点】 氧化还原反应的应用
您最近一年使用:0次
2017-11-25更新
|
2384次组卷
|
56卷引用:河北省安平中学2016-2017学年高二下学期期末考试化学试题
河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(天津卷精编版)浙江省嘉兴市第一中学2017-2018学年高二上学期期中考试化学试题河南省洛阳市2018届高三上学期第一次质量预测(1月)化学试题河南省郑州市2018届高三高中毕业班第一次质量检测(模拟)化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.4 氧化还原反应安徽省池州一中(贵池中学)2017-2018学年高一下学期期中质量检测化学试题(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密(已下线)学科网2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【教学案】山西省临猗县临晋中学2019届高三9月月考化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题【校级联考】福建省晋江市(安溪一中、养正中学、惠安一中、泉州实验中学四校)2018-2019学年高二上学期期中考试化学试题【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (教学案)(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)河南省郑州市实验中学2019届高三上学期期中考试化学试题(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点河北省易县中学2018-2019学年高二下学期期末考试化学试题(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》黑龙江省龙东南联合体2018-2019学年高二下学期期末考试化学试题福建省莆田九中2019-2020学年高二上学期期中考试化学试题福建省莆田第七中学2020届高三上学期期中复习检测化学试题2福建省厦门市思明区厦门外国语学校2019-2020学年高三上学期周末练习12——化学试题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题天津市海河中学2020届高三第二学期化学测试(二)试卷河北省保定市2019-2020学年高二上学期期末调研考试化学试题江苏省宿迁市沭阳县修远中学2019-2020学年高二下学期4月月考化学试题(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分河北省衡水中学2020届高三下学期二月份网络教学质量监测理科综合化学试题湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学(已下线)【南昌新东方】2019-2020 雷氏中学 高一下 周练(已下线)2.3.1 认识氧化还原反应 氧化剂和还原剂练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)高一必修第二册(人教2019版)第六章 化学反应与能量 素养检测黑龙江省大庆市让胡路区大庆铁人中学2021届高三上学期阶段考试化学试题(已下线)高中化学苏教2019版必修第二册-专题6 第三单元综合拔高练青海省西宁市普通高中五校2020-2021学年高三上学期期末联考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练四川省绵阳市南山中学2021届高三下学期3月月考试题化学试题天津市河北区2021届高三一模考试化学试题(已下线)押山东卷第02题 氧化还原反应在生产生活中的应用-备战2021年高考化学临考题号押题(山东卷)甘肃省武威市民勤县第四中学2020-2021学年高二下学期期中考试化学(普通班)试题江西省景德镇一中2020-2021学年高一下学期期末考试化学试题(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)江苏省宿迁市泗阳县实验高级中学2021-2022学年高一下学期第一次月考化学试题福建省莆田第一中学2021-2022学年高二上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题山东省滨州市沾化区实验高级中学2022-2023学年高三10月月考化学试题河北保定市唐县田家炳中学2021-2022学年高三上学期11月化学试题(已下线)江苏省南通市如皋市2022-2023学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
真题
名校
5. 下列有关物质性质与用途具有对应关系的是
| A.Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂 |
| B.ClO2具有还原性,可用于自来水的杀菌消毒 |
| C.SiO2硬度大,可用于制造光导纤维 |
| D.NH3易溶于水,可用作制冷剂 |
您最近一年使用:0次
2017-07-01更新
|
2702次组卷
|
68卷引用:河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题
河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题2017年全国普通高等学校招生统一考试化学(江苏卷精编版)河北省涞水波峰中学2018届高三第一次调研考试化学试题黑龙江省大庆实验中学2017-2018学年高二上学期开学考试化学试题黑龙江省哈尔滨市第十八中学2018届高三第一次月考化学试题河南省林州市第一中学2018届高三10月调研化学试题福建省福州市八县(市)协作校2017-2018学年高二上学期期中联考化学(理)试题江西省抚州市临川区第一中学2018届高三上学期期中考试化学试题黑龙江省哈尔滨市122中学2017-2018学年高一上学期期末考试化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.11 非金属及其化合物重庆市第二中学2018届高三3月测试化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期4月月考化学试题北京市密云区2017-2018学年高三第二学期阶段性练习理综化学试题(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密江苏省盐城市田家炳中学2019届高三上学期开学考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第1讲 碳、硅及其无机非金属材料【教学案】【全国百强校】西藏自治区拉萨市北京实验中学2019届高三上学期第一次月考化学试题安徽省黄山市徽州区第一中学2018-2019学年高二上学期开学考试化学试题湖南省怀化市2018届高三上学期期末统一考试化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第2讲 氯及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第4讲 氮及其化合物 (教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)安徽省阜阳市第三中学2018-2019学年高一下学期开学考试化学试题(已下线)2019年7月8日 《每日一题》2020年高考一轮复习-物质的性质及变化云南省石屏县第二中学2020届高三上学期开学考试化学试题宁夏青铜峡市高级中学(吴忠中学分校)2020届高三上学期第二次月考化学试题河北省秦皇岛市六校2020届高三上学期期初检测联考化学试题天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题海南省嘉积中学2020届高三上学期第二次月考化学试题浙江省宁波市效实中学2020届高三上学期第一次模拟考试化学试题(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分陕西省渭南市澄城县城关中学2019-2020学年高二检测化学试题陕西省延安市第一中学2019-2020学年高一下学期线上摸底考试化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷广东省肇庆市广宁第一中学2021届高三上学期9月月考化学试题安徽省安庆市宿松县程集中学2019-2020学年高二下学期6月月考化学试题甘肃省武威市民勤县第一中学2019-2020学年高一下学期期中考试化学(文) 试题湖南省宁乡市第一高级中学2021届高三上学期11月摸底考试化学试题贵州省台江县民族中学2020-2021学年高一下学期3月月考化学试题山东省郯城第二中学2020-2021学年下学期高一4月月考化学试题吉林省长白实验中学2020-2021学年高一下学期第一次月考化学试题江苏省吴江汾湖高级中学2020-2021学年高一下学期阶段性教学反馈训练化学试题(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)云南省曲靖市第二中学2021-2022学年高二上学期开学收心检测化学试题天津市第三中学2021-2022学年高三上学期10月阶段性检测化学试题云南省昆明市第八中学2020-2021学年高一下学期第二次月考化学试题(已下线)卷01 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省密山市第四中学2021-2022学年高二上学期期中考试化学(文)试题江西省新余市第六中学2021-2022学年高一下学期期中考试化学试题湖南省株洲世纪星高级中学2022-2023学年高一上学期期末考试化学试题陕西省横山清源中学2022-2023学年高一下学期3月月考化学试题贵州省松桃民族中学2022-2023学年高一下学期3月月考化学试题北京市育才学校2022-2023学年高一下学期期中考试化学试题江苏省淮安市淮阴区2022-2023学年高二上学期11月期中化学试题北京市第二中学2022-2023学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
6. a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层电子数相同,c所在周期数与族序数相同;d与a同族,下列叙述正确的是
| A.四种元素中b的金属性最强 |
B.原子半径: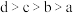 |
| C.d的单质氧化性比a的单质氧化性强 |
| D.c的最高价氧化物对应水化物是一种强碱 |
您最近一年使用:0次
2022-07-16更新
|
2885次组卷
|
97卷引用:四川省广安市2016-2017学年高二下学期期末考试化学试题
四川省广安市2016-2017学年高二下学期期末考试化学试题山东省济南市平阴县玛钢外国语学校2016-2017学年高一下学期期末考试化学试题陕西省石泉中学2016-2017学年高一下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅱ卷精编版)内蒙古北京八中乌兰察布分校2016-2017学年高一下学期期末考试化学试题新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题浙江省绍兴市新昌中学2018届高三10月选考适应性考试化学试题山西省山西大学附属中学2017-2018学年高二上学期9月月考化学试题内蒙古赤峰市2018届高三上学期期末考试理综化学试题(已下线)狂刷04 原子核外电子的排布 元素周期律—《小题狂刷》2017-2018学年高一化学人教必修2西藏拉萨北京实验中学2018届高三第五次月考理科综合化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期4月月考化学试题【全国百强校】四川省南充高级中学2017-2018学年高一下学期期中考试化学试题(已下线)《考前20天终极攻略》-5月19日 物质结构 元素周期律(已下线)解密07 物质结构和元素周期律(教师版)——备战2018年高考化学之高频考点解密【全国百强校】陕西省西安市长安区第一中学2017-2018学年高一下学期期末考试(理)化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二上学期开学考试(8月月考)化学试题【全国百强校】福建省三明市第一中学2019届高三第二次返校考试化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)吉林省白城市通榆县第一中学2018-2019学年高一下学期第一次月考化学试题江苏省东台市创新高级中学2018-2019学年高一下学期3月月考化学试题河南省周口市扶沟县高级中学2018-2019学年高一下学期第一次月考化学试题湖北省襄阳市东风中学2018-2019学年高一下学期3月月考化学试题安徽省亳州市第二中学2018-2019学年高二下学期期中考试化学试题步步为赢 高一化学暑假作业:作业三 元素周期表和元素周期律的应用福建省厦门市湖滨中学2018-2019学年高一下学期期中考试化学试题【全国百强校】西藏自治区拉萨中学2018-2019学年高一下学期期中考试化学试题(已下线)2019年6月10日 《每日一题》选修3-微粒半径的大小比较【区级联考】天津市和平区2019届高三下学期一模化学试题上海市青浦区2019届高三高三第二次学业质量调研(二模)化学试题辽宁省六校协作体2019-2020学年高二上学期开学考试化学试题黑龙江省大庆市铁人中学2018-2019学年高一下学期期末化学试题云南省文山壮族苗族自治州马关县第一中学2020届高三上学期9月份考试化学试题云南省文山州砚山县一中2020届高三上学期开学考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题云南省元阳县第一中学2020届高三上学期开学考试化学试题云南省双柏县一中2020届高三上学期开学考试化学试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题陕西省榆林市第二中学2020届高三第四次模拟考试化学试题2020届高三化学理论复习 元素周期律和元素周期表(专题训练)黑龙江省哈尔滨市第六中学2020届高三上学期第三次调研考试化学试题湖北省恩施州清江外国语学校2019-2020学年高二上学期期末考试化学试题辽宁省滨海实验中学2019-2020学年高一上学期期末化学试题专题2.1 物质结构(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题专题1微观结构与物质的多样性 模拟高考第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训第1章 第3节 元素周期表的应用第1章 第3节 元素周期表的应用(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分四川省内江市市中区天立学校2019-2020学年高一下学期第二次月考化学试题天津市南开中学2020届高三教学质量监测理科综合化学部分湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学(已下线)专题5.2 元素周期律和元素周期表(讲)——2020年高考化学一轮复习讲练测四川省眉山市彭山区第一中学2019-2020学年高一下学期期中考试化学试题(已下线)专题5.2 元素周期律和元素周期表(练)——2020年高考化学一轮复习讲练测(已下线)【南昌新东方】2019-2020 雷氏中学 高一下 周练甘肃省兰州市第一中学2019-2020学年高一4月月考化学试题湖北省黄冈市黄梅国际育才高级中学2018-2019学年高一下学期3月月考化学试题(已下线)第04章 物质结构 元素周期律(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)苏教版(2020)高一必修第一册专题5 总结检测人教版(2019)高一必修第一册第四章 物质结构 元素周期律 高考挑战区四川省新津中学2019-2020学年高二上学期开学考试化学试题人教版(2019)高一必修第一册 第四章素养检测四川省武胜烈面中学校2020-2021学年高二上学期开学考试化学试题人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第二节 元素周期律 高考帮高一必修第一册(苏教2019版)专题5 高考挑战区高一必修第一册(苏教2019)专题5 第一单元 元素周期律和元素周期表3(鲁科版2019)必修第二册 第1章 原子结构 元素周期律 学科素养提升云南省保山第九中学2021届高三上学期开学考试化学试题山西省怀仁市第一中学云东校区2020-2021学年高一下学期第一次月考化学试题青海省湟川中学2019-2020学年高一下学期期中考试化学试题四川省阆中中学校2020-2021学年高一(仁智班)下学期第一次月考化学试题山东省齐河县第一中学2020-2021学年高一下学期第一次月考化学试题山东省济南市第一中学2020-2021学年高一下学期期中考试化学试题(等级考)湖北省竹山县第二中学2020-2021学年高一下学期第一次月考化学试题(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)河北省张家口市第一中学2020-2021学年高一下学期期中考试化学试题云南省玉溪市2021-2022学年高一上学期期末教学质量检测化学试题安徽工业大学附属中学2020-2021学年高二上学期文理分科考试化学试题陕西省安康中学2021-2022学年高二上学期期末考试化学试题北京市中国人民大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)海南省三亚市第一中学2021-2022学年高三下学期最后一卷化学试题云南省马关县第一中学校2021-2022学年高一下学期开学考试化学试题福建省厦门市松柏中学2021-2022学年高一下学期第一次月考(3月)化学试题专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第1课时 原子核外电子排布的周期性陕西省西安市长安区第一中学2021-2022学年高一下学期期中考试化学试题安徽工业大学附属中学2019-2020学年高一下学期(高二文理分科考试)化学试题四川省凉山宁南中学2019-2020学年高二下学期第一次月考化学试题河北省石家庄市第二中学2022-2023学年高一下学期3月月考化学试题2.2.1原子核外电子排布的周期性 课后
单选题
|
较易(0.85)
7. 油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热△H为
| A.3.8×104kJ·mol-1 | B.-3.8×104kJ·mol-1 |
| C.3.4×104kJ·mol-1 | D.-3.4×104kJ·mol-1 |
您最近一年使用:0次
2016-07-11更新
|
2812次组卷
|
34卷引用:2016年全国普通高等学校招生统一考试化学(海南卷精编版)
2016年全国普通高等学校招生统一考试化学(海南卷精编版)2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2017届河北省沧州市第一中学高三上周测化学试卷2016-2017学年广东省仲元中学高二上学期期末考试化学(理)试卷湖北省新洲一中、黄陂一中、麻城一中2017-2018学年高二上学期期中联考化学试题安徽省合肥八中、马鞍山二中、阜阳一中2017-2018学年第一学期联考高二化学试卷福建省泉州市泉港区第一中学2017-2018学年高二年上学期期末考化学试题(已下线)《考前20天终极攻略》-5月24日 盖斯定律及反应热的有关计算(已下线)解密08 化学反应与热能(教师版)——备战2018年高考化学之高频考点解密【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期10月模块诊断化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点2016年全国普通高等学校招生统一考试化学(海南卷参考版)(已下线)2019年高考总复习巅峰冲刺-专题05 化学反应中的能量变化应试策略海南省文昌中学2019-2020学年高二上学期第二次月考化学试题湖南省师范大学附属中学2020届高三上学期第二次月考化学试题山西省大同市天镇县第一中学校2019-2020学年高二上学期第二次月考化学试题2020届高三化学二轮冲刺新题专练——燃烧热的定义与应用(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训安徽省定远县育才学校2019-2020学年高二4月月考化学试题河南省郑州市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热 高考帮广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题海南省八所中学2020届高三上学期期末考试化学试题(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)黑龙江省哈尔滨市第一六二中学2021-2022学年高三上学期第三次月考化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题(已下线)第六章 化学反应与能量 第34讲 反应热的计算第一章 化学反应的热效应 第一节 反应热 第2课时 热化学方程式 燃烧热湖北省武汉市第三中学2023-2024学年高一下学期3月月考化学试卷
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
真题
名校
8. 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________ 、_______________ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是____________________ 。
②将下列实验操作步骤正确排序___________________ (填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________ (列式表示)。若实验时按a、d次序操作,则使x__________ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
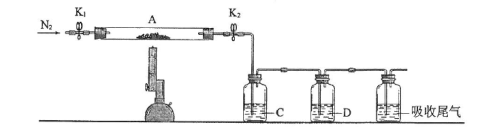
①C、D中的溶液依次为_________ (填标号)。C、D中有气泡冒出,并可观察到的现象分别为_______________ 。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_____________________ 。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式
【知识点】 氧化还原反应方程式的书写与配平解读 亚铁盐 物质的分离、提纯 化学实验探究
您最近一年使用:0次
2017-08-08更新
|
9202次组卷
|
30卷引用:2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)
2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题四川省双流中学2017-2018学年高二上学期开学考试化学试题江西省上高二中2018届高三上学期第三次月考化学试题(已下线)《考前20天终极攻略》-5月27日 综合实验设计、探究和评价(已下线)解密18 物质的制备、实验方案的设计与评价——备战2018年高考化学之高频考点解密百所名校联考-金属及其化合物吉林省延边市第二中学2020届高三入学考试化学试题安徽省黄山市屯溪第一中学2019-2020学年高二上学期入学摸底考试化学试题2020届高考化学二轮复习大题精准训练——定量分析化学实验中物质含量的测定2020届高考化学二轮复习大题精准训练——化学实验方案的设计及评价河北省衡水中学2020届高三四月份质量监测理综化学试题湖南省长沙市长郡中学2020届高三4月份教学质量监测理综化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题河北省石家庄市第二中学2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分河南省郑州市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精讲)——2021年高考化学一轮复习讲练测山东济南市历城第二中学2020-2021学年高二上学期开学考试化学试题高一必修第一册(鲁科2019)第3章 第2节 硫的转化 高考帮福建省福州市第二中学2021届高三上学期第一次月考化学试题(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物云南省保山第九中学2021届高三上学期开学考试化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题(已下线)【教材实验热点】04 Fe(OH)2与Fe(OH)3胶体的制备云南省普洱市第一中学2021-2022学年高三下学期3月份考试理综化学试题(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型31 Fe2+、Fe3+的检验与性质探究
解答题-实验探究题
|
适中(0.65)
名校
解题方法
9. 某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水
利用如图所示的实验装置进行实验。
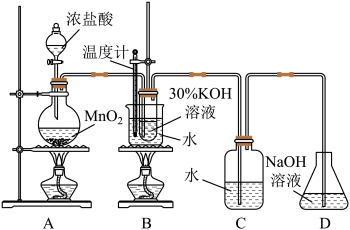
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有__ 。
(2)若对调B和C装置的位置,__ (填“能”或“不能”)提高B中氯酸钾的产率。
实验二:氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的是__ 。
②设计1号试管实验的作用是__ 。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__ 。
实验三:测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用如图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是__ 。(不考虑实验装置及操作失误导致不可行的原因)
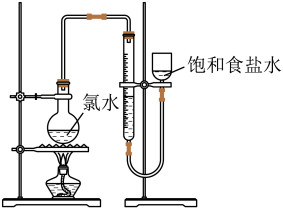
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):__ 。
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
实验一:制取氯酸钾和氯水
利用如图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有
(2)若对调B和C装置的位置,
实验二:氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水 | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
实验三:测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用如图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是

(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
【知识点】 化学实验探究 实验方案设计的基本要求解读 物质性质实验方案的设计解读
您最近一年使用:0次
2020-05-14更新
|
124次组卷
|
2卷引用:2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分
解答题-实验探究题
|
适中(0.65)
名校
解题方法
10. 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示,
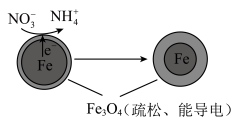
①作负极的物质是____ 。
②正极的电极反应式是____ 。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
pH=4.5时,NO3-的去除率低。其原因是____ 。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____ 。
(1)Fe还原水体中NO3-的反应原理如图所示,

①作负极的物质是
②正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 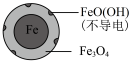 |  |
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 约10% | 约3% |
| 1小时pH | 接近中性 | 接近中性 |
您最近一年使用:0次
2020-05-07更新
|
372次组卷
|
6卷引用:河北省衡水中学2020届高三四月份质量监测理综化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
11. [Zn(CN)4]2–在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2–+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________ 。
(2)1 mol HCHO分子中含有σ键的数目为____________ mol。
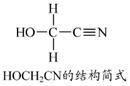
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________ 。
(4)与H2O分子互为等电子体的阴离子为________________ 。
(5)[Zn(CN)4]2–中Zn2+与CN–的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为_____________ 。
4HCHO+[Zn(CN)4]2–+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为
(2)1 mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化类型是
(4)与H2O分子互为等电子体的阴离子为
(5)[Zn(CN)4]2–中Zn2+与CN–的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为

您最近一年使用:0次
2016-12-09更新
|
3647次组卷
|
10卷引用:2016年全国普通高等学校招生统一考试化学(江苏卷精编版)
2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)第2章 化学键与分子间作用力——C挑战区模拟高考(鲁科版选修3)山东省泰安市新泰市第二中学2019-2020学年高二下期中考试化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分天津市南开中学2020届高三教学质量监测理科综合化学部分江苏省启东中学2020-2021学年高二上学期期初考试化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题山西省忻州市岢岚县中学2020-2021学年高二下学期4月月考化学试题河南省安阳市汤阴县第一中学2019-2020学年高二下学期4月月考化学试卷
四、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
12. 高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):
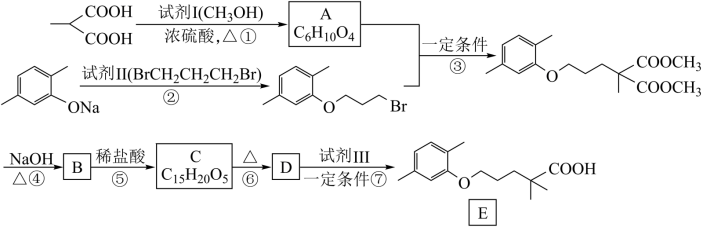
已知: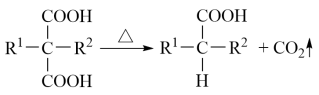 (R1和 R2代表烷基)
(R1和 R2代表烷基)
请回答下列问题:
(1)试剂Ⅰ的名称是______ ,试剂Ⅱ中官能团的名称是______ ,第② 步的反应类型是_______ 。
(2)第①步反应的化学方程式是_____________ 。
(3)第⑥步反应的化学方程式是_____________ 。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________ 。

已知:
 (R1和 R2代表烷基)
(R1和 R2代表烷基) 请回答下列问题:
(1)试剂Ⅰ的名称是
(2)第①步反应的化学方程式是
(3)第⑥步反应的化学方程式是
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是
【知识点】 有机官能团的性质及结构 同分异构体书写 酯的水解反应机理解读 缩聚反应
您最近一年使用:0次
2016-12-09更新
|
2417次组卷
|
9卷引用:2016年全国普通高等学校招生统一考试化学(四川卷精编版)
2016年全国普通高等学校招生统一考试化学(四川卷精编版)2017届广西陆川中学高三上8月月考理综化学试卷2018版化学(苏教版)高考总复习专题十二对接高考精练--烃的含氧衍生物——醇、酚(已下线)2018年5月20日 每周一测——《每日一题》2017-2018学年高二化学人教选修5山西省朔州市怀仁县第一中学2018-2019学年高二下学期第二次月考化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题(已下线)2016年全国普通高等学校招生统一考试化学(四川卷参考版)
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、有机化学基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
4
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 非电解质、电解质物质类别判断 含硫化合物之间的转化 硫化氢 | |
| 2 | 0.4 | 物质的量有关计算 物质结构基础与NA相关推算 可逆反应及反应限度 弱电解质的电离平衡 | |
| 3 | 0.65 | 限定条件下的离子共存 | |
| 4 | 0.65 | 氧化还原反应的应用 | |
| 5 | 0.65 | 酸、碱、盐、氧化物 氨的物理性质及用途 酸性氧化物通性 | |
| 6 | 0.65 | 元素金属性与非金属性递变规律的理解及应用 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 7 | 0.85 | 燃烧热的计算 | |
| 二、解答题 | |||
| 8 | 0.4 | 氧化还原反应方程式的书写与配平 亚铁盐 物质的分离、提纯 化学实验探究 | 实验探究题 |
| 9 | 0.65 | 化学实验探究 实验方案设计的基本要求 物质性质实验方案的设计 | 实验探究题 |
| 10 | 0.65 | 硝酸盐 化学反应条件的控制及优化 原电池原理的综合应用 物质性质实验方案的设计 | 实验探究题 |
| 12 | 0.65 | 有机官能团的性质及结构 同分异构体书写 酯的水解反应机理 缩聚反应 | 有机推断题 |
| 三、填空题 | |||
| 11 | 0.65 | 等电子原理的应用 利用杂化轨道理论判断化学键杂化类型 简单配合物的成键 | |



