2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷
江西
高三
阶段练习
2017-07-27
373次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础、化学与STSE、常见无机物及其应用
2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷
江西
高三
阶段练习
2017-07-27
373次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础、化学与STSE、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
容易(0.94)
真题
名校
1. 运用有关概念判断下列叙述正确的是
| A.1mol H2燃烧放出的热量为H2的燃烧热 |
| B.Na2SO3和H2O2的反应为氧化还原反应 |
C.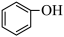 和 和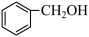 互为同系物 互为同系物 |
| D.BaSO4的水溶液不导电,故BaSO4是弱电解质 |
您最近一年使用:0次
2019-01-30更新
|
1583次组卷
|
11卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)(已下线)2014届黑龙江阿城一中高三上学期期末考试化学试卷(已下线)2013-2014学年江苏省常州市某重点中学高二上学期期末检测化学试卷2015届北京市第66中学高三上学期期中考试化学试卷2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷山西省太原市第二十一中学2020届高三上学期期中考试化学试题2020届高三化学知识点强化训练—燃烧热天津市实验中学2020届高三下学期4月第二次测试化学试题天津市大港油田实验中学2020届高三开学考试化学试题
单选题
|
较易(0.85)
解题方法
2. 某学习兴趣小组讨论辨析以下说法,其中说法正确的是
①通过化学变化可以实现16O与18O间的相互转化
②煤的气化与液化都是物理变化
③碱性氧化物一定是金属氧化物
④只由一种元素组成的物质一定为纯净物
⑤石墨和C60是同素异形体
⑥糖类、蛋白质、油脂属于天然高分子化合物
①通过化学变化可以实现16O与18O间的相互转化
②煤的气化与液化都是物理变化
③碱性氧化物一定是金属氧化物
④只由一种元素组成的物质一定为纯净物
⑤石墨和C60是同素异形体
⑥糖类、蛋白质、油脂属于天然高分子化合物
| A.③⑤⑥ | B.①② | C.③⑤ | D.①③④ |
您最近一年使用:0次
2016-10-12更新
|
168次组卷
|
12卷引用:2016届四川省彭州中学高三9月月考化学试卷
2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2015-2016学年河北省衡水二中高二上期中测试化学试卷2016届安徽省庐江县六校高三上学期第四次联考化学试卷2017届江西省上高二中高三上第二次月考化学试卷湖北省部分重点中学2018届高三起点考试化学试题江西省红色七校2018届高三第一次联考化学试题陕西省西铁一中2018届高三第二次月考化学试题(已下线)学科网2019年高考化学一轮复习讲练测 2.1 物质的组成、性质及分类 讲福建省建瓯市芝华中学2022-2023学年高三上学期暑期考试化学试题(已下线)第一章 化学物质及其变化 第1练 物质的组成、性质和分类
单选题
|
适中(0.65)
真题
名校
3. 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA |
| B.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
【知识点】 阿伏加德罗常数的应用解读
您最近一年使用:0次
2019-01-30更新
|
3073次组卷
|
23卷引用:2012年普通高等学校招生全国统一考试理综化学部分(四川卷)
2012年普通高等学校招生全国统一考试理综化学部分(四川卷)(已下线)2013届山西省忻州一中高三第一次月考化学试卷(已下线)2015届江西师大附中高三年级10月月考化学试卷2015届江苏常州市高三第一次调研试卷化学试卷2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2015-2016学年湖南省双峰一中高一下期中理科化学试卷2017届江西省上高二中高三上第二次月考化学试卷2016-2017学年辽宁省铁岭市清河高级中学高二下学期第一阶段考试化学试卷江西省南昌市第三中学2016-2017学年高一下学期期末考试化学试题广东省阳东广雅学校2018届高三上学期第一次月考化学试题湖南省衡阳县第一中学2018届高三上学期第二次月考化学试题河南省安阳市第三十六中学2018届高三上学期第一次月考化学试题浙江省杭州市学军中学2018届高三选考前适应性练习(2)化学试题安徽省滁州市定远县民族中学2017-2018学年高一下学期期末考试化学试题河南省安阳市第三实验中学2019届高三上学期11月月考化学试题陕西省榆林市第二中学2018-2019学年高二下学期期中考试化学试题江西省奉新县第一中学2021届高三上学期第二次月考化学试题广西梧州市2021届高三3月联考理科综合化学试题山西省晋中市新一双语学校2021-2022学年高三上学期8月月考化学试题(已下线)专题01 阿伏加德罗常数正误判断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)河南省郑州中学2023-2024学年高三上学期第二次月考化学试题
单选题
|
适中(0.64)
4. 下列各组离子能在指定环境中大量共存的是
| A.在c(HCO3-)="0.1" mol·L-1的溶液中:NH4+、AlO2-、Cl-、NO3- |
| B.在由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Fe2+、ClO-、Na+、SO42- |
| C.在加入铝粉产生H2的溶液中:SO42-、NO3-、Na+、NH4+ |
| D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+ |
【知识点】 离子共存
您最近一年使用:0次
2016-12-09更新
|
219次组卷
|
4卷引用:2015届江西师大附中高三年级10月月考化学试卷
(已下线)2015届江西师大附中高三年级10月月考化学试卷2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷
单选题
|
适中(0.65)
名校
5. 下列物质中,既能导电又属于强电解质的一组物质是( )
| A.熔融MgCl2、熔融NaOH | B.液氨、石灰水 |
| C.石墨、食醋 | D.稀硫酸、蔗糖 |
【知识点】 物质水溶液的导电性解读 强电解质和弱电解质的判断
您最近一年使用:0次
2016-06-27更新
|
296次组卷
|
11卷引用:2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷
2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2015-2016学年内蒙古巴彦淖尔一中高一上期末化学试卷22015-2016学年山东省寿光现代中学高二6月月考化学试卷2017届江西省上高二中高三上第二次月考化学试卷贵州省遵义航天高级中学2017-2018学年高二上学期期中考试化学试题江西省铅山县第一中学2018-2019学年高二上学期期中考试化学试题浙江省温州市求知中学2018-2019学年高一下学期第二次月考化学试题(已下线)2019年7月10日 《每日一题》2020年高考一轮复习-电解质及其强弱判断四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题四川省广安代市中学校2021-2022学年高二上学期第二次月考化学试题
单选题
|
较难(0.4)
6. 下列离子方程式与所述事实相符且正确的是
| A.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O===MnO2↓+Cl-+2H+ |
B.用稀硝酸清洗做过银镜反应的试管:Ag+NO +4H+===Ag++NO↑+2H2O +4H+===Ag++NO↑+2H2O |
| C.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl- |
D.用铁棒作阴极、碳棒作阳极电解饱和氯化钠溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
【知识点】 离子反应的发生及书写
您最近一年使用:0次
2016-12-09更新
|
155次组卷
|
5卷引用:2016届四川省彭州中学高三9月月考化学试卷
单选题
|
容易(0.94)
7. 下列说法正确的是
| A.石油分馏、煤的气化、海水制食盐、蛋白质变性等过程都包含化学变化 |
| B.酸性氧化物一定不能和酸反应 |
| C.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| D.爆鸣气、铝热剂、玻璃、花生油、聚乙烯均为混合物 |
【知识点】 分散系
您最近一年使用:0次
2016-12-09更新
|
126次组卷
|
3卷引用:2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷
单选题
|
适中(0.65)
名校
8. 除去下列物质中所含少量杂质的设计正确的是
| 选项 | 物质 | 杂质 | 试剂 | 提纯方法 |
| A | BaSO4 | BaCO3 | 盐酸 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 稀NaOH溶液 | 混合振荡、静置分液 |
| D | 蛋白质 | 葡萄糖 | 浓(NH4)2SO4溶液 | 盐析、过滤、洗涤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2015-12-14更新
|
200次组卷
|
4卷引用:2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷
单选题
|
容易(0.94)
真题
名校
9. 按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。

下列说法错误的是( )

下列说法错误的是( )
| A.步骤(1)需要过滤装置 | B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 | D.步骤(4)需要蒸馏装置 |
您最近一年使用:0次
2019-01-30更新
|
4394次组卷
|
71卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)(已下线)2013-2014吉林省临江一中高二下学期期中考试化学试卷(已下线)2013-2014学年陕西省南郑中学高二下学期期末考试化学试卷(已下线)2015届江苏省泰州市姜堰区高三上学期期中化学试卷2015届湖南省长沙长郡中学高三上学期第四次月考化学试卷2014届浙江省东阳中学高三下学期期中考试化学试卷2014-2015湖北省武汉市二中高二上学期期末化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届湖北省仙桃中学高三8月月考(开学摸底)化学试卷2015-2016学年湖南省益阳市箴言中学高一9月月考化学试卷2015-2016学年内蒙古奋斗中学高一上9月质检化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016届陕西省西安市曲江第一中学高三上学期期中测试化学试卷2016届上海市十三校高三上学期第一次联考化学试卷2016届河南省淮阳第一高级中学高三上学期教学质检化学试卷2015-2016学年湖北省黄石市高一上学期期末考试化学试卷2015-2016学年浙江省宁波市北仑中学高二下学期期中考试化学试卷2017届辽宁省东北育才学校高三上学期第一次模拟化学试卷2016-2017学年广西桂林十八中高二上开学考试化学卷2017届江西省上高二中高三上第二次月考化学试卷2017届福建省仙游一中高三上第一次月考化学试卷2017届辽宁省沈阳东北育才学校高三上模拟一化学试卷2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷2016-2017学年山西省临汾一中等三校高一上期中化学卷2016-2017学年湖北宜昌金东方中学、三峡高中高一11月月考化学卷甘肃省武威市第六中学2018届高三第一次阶段性过关考试化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一10月阶段测试化学试题河南省南阳市第一中学2018届高三第四次考试化学试题河南省安阳市第三十六中学2018届高三上学期第一次月考化学试题福建省闽侯第六中学2017-2018学年高二下学期第一次月考化学试题【全国百强校】广西壮族自治区桂林市第十八中学2019届高三上学期第一次月考化学试题【全国百强校】山西省怀仁县第一中学2018-2019学年高一上学期第一次月考化学试题2【全国百强校】山西省怀仁县第一中学2018-2019学年高一上学期第一次月考化学试题1河南省安阳市第三实验中学2019届高三上学期11月月考化学试题【全国百强校】云南省玉溪第一中学2018-2019学年高一下学期第一次月考化学试题河北省大名县第一中学2018-2019学年高二(普通班)5月月考化学试题黑龙江省大庆市东风中学2019-2020学年高一10月月考化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2019-2020学年高一上学期第一次月考化学试题甘肃省武威第十八中学2020届高三上学期第一次诊断考试化学试题2020届高考化学小题狂练(全国通用版)专练18 物质的检验、分离和提纯云南省耿马县民族中学2019-2020学年高二12月月考化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题2云南省昭通市永善县第二中学2019—2020学年高二上学期期末考试化学试题2020届高三化学二轮微专题突破训练:物质的检验、分离与提纯人教化学选修5第一章第四节课时4甘肃省张掖市高台县第一中学2018—2019学年高二下学期期中考试化学试题重庆市2019-2020学年高二下学期第一次网络考试化学试题重庆南开中学高2020届高三化学网络复习化学实验常用仪器和基本操作考点过关测试湖南省双峰县第一中学2019-2020学年高二下学期入学考试化学试题(已下线)专题11 自然资源的开发利用(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)甘肃省白银市靖远县第四中学2021届高三上学期10月月考化学试题(已下线)浙江省宁波市北仑中学2018-2019学年高二下学期期中考试化学试题高一必修第一册(苏教2019)专题2 第一单元 研究物质的实验方法2江西省南昌市新建区第二中学2020-2021学年高二上学期“新星计划”体验营10月考化学试题陕西省宝鸡市陈仓区虢镇中学2020-2021学年高一上学期第一次月考化学试题高二选择性必修3(人教版2019)第一章 有机化合物的结构特点与研究方法 第二节 综合训练甘肃省平凉市庄浪县第一中学2021届高三第四次模拟化学试题吉林省扶余市第二实验学校2020-2021学年高二下学期第一次月考化学 (B)试题四川宜宾屏山县中学校2020-2021学年高一下学期第一次月考化学试题(人教2019)选择性必修3第一章 B 素养拓展区云南省易门一中2020-2021学年高二6月月考化学试题陕西省耀州中学2021-2022学年高一上学期第一次月考化学试题课后-1.2.1 有机化合物的分离、提纯-人教2019选择性必修3(已下线)第03讲 有机物的分离、提纯(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)(已下线)1.3.3 萃取和分液-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)(已下线)专题16 有机化合物的结构特点和研究方法-2023年高考化学一轮复习小题多维练(全国通用)专题1 有机化学的发展及研究思路 本专题达标检测(已下线)【知识图鉴】单元讲练测选择性必修3第1单元01讲核心(已下线)有机化合物的结构特点和研究方法——课时3有机物的分离提纯云南省开远市第一中学校2023-2024学年高二上学期9月月考化学试题(已下线)第02讲 研究有机化合物的一般方法-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
10. 向CuSO4溶液中逐滴加入碘化钾溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变棕色,再向反应后的溶液中通入过量SO2,溶液变无色。则下列说法正确的是
| A.通入22.4L SO2参加反应时,有2NA个电子发生转移 |
| B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.滴加碘化钾溶液时,KI被氧化,CuI是氧化产物 |
| D.上述实验条件下,微粒的氧化性:Cu2+>I2>SO2 |
您最近一年使用:0次
2016-10-12更新
|
544次组卷
|
11卷引用:2016届四川省彭州中学高三9月月考化学试卷
2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016届甘肃省张掖、嘉峪关、山丹部分高中高三上学期期中联考化学试卷2017届江西省上高二中高三上第二次月考化学试卷2018届高三一轮复习化学:考点30-硫与二氧化硫性质探究辽宁省鞍山市第一中学2018届高三上学期第一次模拟考试化学试题山东省实验中学2018届高三上学期第二次诊断考试化学试题湖南省浏阳一中、株洲二中等湘东五校2018届高三12月联考化学试题湖南省衡阳市第八中学2018届高三上学期第五次月考化学试题甘肃省武威市凉州区武威第八中学2021届高三年级第一次诊断考试化学试题
单选题
|
较难(0.4)
名校
11. 在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是
| A.33.3% | B.40% | C.36% | D.54.5% |
您最近一年使用:0次
2016-12-09更新
|
2565次组卷
|
33卷引用:2013届四川省广元市高三第二次诊断性考试理综化学试卷
(已下线)2013届四川省广元市高三第二次诊断性考试理综化学试卷(已下线)2015届江西师大附中高三年级10月月考化学试卷(已下线)2015届辽宁省大连市第八中学高三10月月考理综化学试卷(已下线)2015届吉林省实验中学高三上学期第三次质量检测化学试卷2016届四川省彭州中学高三9月月考化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016届河南省三门峡市陕州中学高三上学期第二次月考化学试卷2015-2016学年天津市第一中学高一上学期期末化学试卷吉林省蛟河市友好学校2019-2020学年高一上学期期中联考化学试题(已下线)2.1.2 钠的几种化合物-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)高一必修第一册(鲁科2019)第1章第2节 研究物质性质的方法和程序 方法帮人教版(2019)高一必修第一册 第二章 海水中的重要元素 第一节 钠及其化合物 方法帮湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题黑龙江省鹤岗市第一中学2020-2021学年高一上学期期中考试化学试题高一必修第一册(苏教2019)专题3 第二单元 金属钠及钠的化合物2安徽省安庆市第一中学2020-2021学年高一上学期期中考试化学试题(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)江西省铜鼓中学2020-2021学年高二上学期开学考(非实验班)化学试题(已下线)易错专题11 Na2O2反应的增重问题-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)第一节 钠及其化合物 第2课时 钠的化合物 焰色试验(已下线)第06讲 钠及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)山东省泰安市宁阳县第四中学2022-2023学年高三上学期10月月考化学试题(等级考)黑龙江省鹤岗市绥滨县第一中学2021-2022学年高三上学期期中考试化学试题(已下线)题型22 Na2O2的性质及相关实验探究(已下线)第三章 金属及其化合物 第11练 钠及其氧化物广东省大埔县虎山中学2022-2023学年高三上学期1月期末考试化学试题(已下线)考点13 钠及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)湖南省长沙市长郡梅溪湖中学2023-2024学年高二上学期入学考试化学试题四川省南充高级中学2021-2022学年高一下学期开学考试化学试题山东省泰安市宁阳县第四中学2023-2024学年高三上学期10月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 关于下列各实验装置的叙述中,不正确的是
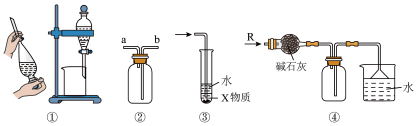

| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
【知识点】 仪器使用与实验安全 萃取和分液解读 常见气体的制备与收集解读
您最近一年使用:0次
2016-12-09更新
|
737次组卷
|
13卷引用:2012届山东省莱州一中高三第一次质量检测化学试卷
(已下线)2012届山东省莱州一中高三第一次质量检测化学试卷(已下线)2012届河南省三门峡市高三上学期调研考试化学试卷(已下线)2014届高考化学二轮专题冲刺第15讲 实验方案的设计与评价练习卷(已下线)2013届山东省潍坊一中高三过程性训练(三)化学试卷 2016届四川省彭州中学高三9月月考化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷陕西省西安市长安区第一中学2017-2018学年高一下学期第一次教学质量检测化学试题山西省实验中学2020届高三化学复习针对性试题集(七)河南省信阳市商城县上石桥高中2021届高三上学期第一次月考化学试题(已下线)学科网2020年高三11月大联考考后强化卷(山东卷)山东省潍坊第四中学2021-2022学年高三上学期10月月考化学试题山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题山东省潍坊市昌乐二中2023-2024学年高三上学期第一次月考化学试题
单选题
|
较难(0.4)
名校
13. 组成和结构可用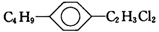 表示的有机物共有(不考虑立体异构)
表示的有机物共有(不考虑立体异构)
| A.9种 | B.12种 | C.24种 | D.36种 |
您最近一年使用:0次
2017-03-29更新
|
862次组卷
|
10卷引用:2014-2015学年宁夏银川唐徕回民中学高二下期末化学试卷
2014-2015学年宁夏银川唐徕回民中学高二下期末化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2015-2016学年陕西省长安区一中高二上期末理化学试卷2015-2016学年湖北沙市中学高二下第三次半月考化学试卷2015-2016学年陕西西安长安一中高二下第二次月考化学卷2015-2016学年河北省唐山市开滦二中高二下期末化学试卷吉林省实验中学2016-2017学年高二3月月考化学试题1【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一6月阶段性测试化学试题(已下线)吉林省实验中学2016-2017学年高二3月月考化学试题江西省南康唐江中学2020-2021学年高二下学期第一次月考化学试题
单选题
|
适中(0.65)
14. 下列说法正确的是( )
| A.在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| B.C2H6O和C4H10都有2种同分异构体 |
| C.乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D.淀粉和蛋白质均可水解生成葡萄糖 |
您最近一年使用:0次
2016-09-06更新
|
836次组卷
|
4卷引用:2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷
2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016-2017学年江西省金溪一中高二上开学考化学试卷2017-2018学年高中化学人教版必修2章末质量检测(三) 有机化合物(已下线)专题06 有机知识辨析(糖类、油脂、蛋白质、醇)-2021年高考化学必做热点专题
单选题
|
适中(0.65)
名校
15. 在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρg·cm-3,溶质的质量分数为ω,溶质的物质的量浓度为C mol/L。下列叙述中正确的是
①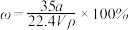 ②
②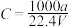
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH4+) > c(H+) > c(OH-)
①
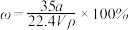 ②
②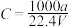
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH4+) > c(H+) > c(OH-)
| A.①④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
2019-01-30更新
|
856次组卷
|
21卷引用:福建省厦门双十中学2011届高三第一次月考化学试题
(已下线)福建省厦门双十中学2011届高三第一次月考化学试题(已下线)2012届湖南省衡阳市八中高三上学期第一次月考化学试卷(已下线)2012届浙江省临海市白云中学高三上学期第一次月考化学试题卷(已下线)2012届四川省成都外国语学校高三第二次月考理科综合化学试卷(已下线)2014-2015学年湖南省石门县一中高三上学期第一次月考化学试卷(已下线)2015届江西师大附中高三年级10月月考化学试卷2015届河南省周口中英文学校高三上学期12月月考化学试卷2013—2014福建省闽侯一中高三上学期10月月考化学试卷2016届湖南省石门县一中高三第一次月考化学试卷2016届湖南省常德市石门一中高三上学期10月月考化学试卷2016届浙江省宁波市柴桥中学高三上学期10月月考化学试卷2016届安徽省三校高三上学期二次模拟化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016届河南省偃师高级中学高三上学期第二次月考化学试卷2015-2016学年湖北省老河口一中高一上学期期末考试化学试卷2017届江西省上高二中高三上第二次月考化学试卷2017届江西省新余一中高三上学期第二次段考化学试卷江西省玉山县第一中学2017届高三化学板块复习测试:化学计算及其综合应用(已下线)二轮复习 专题2 化学常用计量 押题专练(已下线)2019高考备考二轮复习精品资料-专题2 化学常用计量(押题专练)第30届( 2016年)全国中学生化学竞赛(安徽赛区)初赛试题
单选题
|
较难(0.4)
名校
解题方法
16. 将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500ml 2mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为
| A.0.2mol | B.0.8mol | C.0.6mol | D.1.0mol |
您最近一年使用:0次
2020-06-20更新
|
333次组卷
|
8卷引用:2015届吉林省实验中学高三上学期第三次质量检测化学试卷
二、填空题 添加题型下试题
填空题
|
较难(0.4)
17. 综合利用CO2对环境保护及能开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是______________ 。
a. 可在碱性氧化物中寻找
b. 可在ⅠA、ⅡA族元素形成的氧化物中寻找
c. 可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是_________________________ 。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
已知:

反应A的热化学方程式是______________________________ 。
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生_____________ (填“氧化”或“还原”)反应。
② CO2在电极a放电的反应式是___________________________ 。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是
a. 可在碱性氧化物中寻找
b. 可在ⅠA、ⅡA族元素形成的氧化物中寻找
c. 可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:

已知:

反应A的热化学方程式是
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生
② CO2在电极a放电的反应式是
您最近一年使用:0次
填空题
|
较难(0.4)
18. 某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、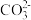 、
、 、
、 、Cl-、
、Cl-、 的一种或几种,取该溶液进行实验,实验内容如下:
的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是_______________________________ ;
(2)写出有关离子方程式:步骤①中生成A_______________________________ ;步骤②生成沉淀I_______________________________ ;
(3)假设测定A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,而沉淀C物质的量0.07mol,能说明(1)中不能确定的阴离子存在的理由是_______________________________ 。
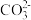 、
、 、
、 、Cl-、
、Cl-、 的一种或几种,取该溶液进行实验,实验内容如下:
的一种或几种,取该溶液进行实验,实验内容如下:
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是
(2)写出有关离子方程式:步骤①中生成A
(3)假设测定A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,而沉淀C物质的量0.07mol,能说明(1)中不能确定的阴离子存在的理由是
您最近一年使用:0次
2016-12-08更新
|
229次组卷
|
5卷引用:2015届湖南省益阳市六中高三上学期期中考试化学试卷
三、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
19. 硼、镁及其化合物在工农业生产中应用广泛。
已知:硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为_____________ 。X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为_______________ 。
(2)若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为_________ 。已知Ksp[Mg(OH)2]=5.6 10-12,当溶液pH=6时
10-12,当溶液pH=6时_____________ (填“有”或“没有”)Mg(OH)2沉淀析出。
(3)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL。该粗硼样品的纯度为_______________ 。(提示:I2+2S2O32-=2I-+S4O62-)
已知:硼镁矿主要成分为Mg2B2O5•H2O,硼砂的化学式为Na2B4O7•10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为
(2)若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为
 10-12,当溶液pH=6时
10-12,当溶液pH=6时(3)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL。该粗硼样品的纯度为
【知识点】 化学实验基础
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
20. 4,7—二甲基香豆素(熔点:132.6℃)是一种重要的香料,广泛分布于植物界中,由间—甲苯酚为原料的合成反应如下:

实验装置图如下:

主要实验步骤:
步骤1:向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2:保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3:粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)简述装置b中将活塞上下部分连通的目的_________________________ 。
(2)浓H2SO4需要冷却至0℃以下的原因是_____________________________ 。
(3)反应需要搅拌12h,其原因是____________________________________ 。
(4)本次实验产率为_____________________ (百分数保留一位小数)
(5)用____________ (填药品名称)收集粗产品,用____________ (填操作名称)的方法把粗产品分离。

实验装置图如下:

主要实验步骤:
步骤1:向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2:保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3:粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)简述装置b中将活塞上下部分连通的目的
(2)浓H2SO4需要冷却至0℃以下的原因是
(3)反应需要搅拌12h,其原因是
(4)本次实验产率为
(5)用
【知识点】 化学实验基础
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
21. 如图转化关系能合成E、F两种有机高分子化合物,其中E为缩聚产物,F为加聚产物。A中含有苯环(苯环上的一硝基取代物仅一种),A的核磁共振氢谱图中四个吸收峰的面积之比为1:2:6:1;J能发生银镜反应;C中滴入浓溴水能产生白色沉淀;G能使溴的四氯化碳溶液褪色。已知以下信息:
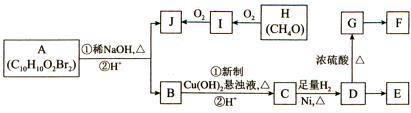
a.在稀碱溶液中,溴苯难以发生水解反应;
b.两个羟基同时连在同一碳原子上的结构是不稳定的,它将自动发生脱水反应,如:CH3CH (OH)2→CH3CHO十H2O。
回答下列问题:
(1)I中官能团的名称为_____________ 。 (2)H的结构式为_____________ 。
(3)D→G的反应类型是_____________ 。
(4)1 mol B与足量Cu(OH)2反应可生成_______ g Cu2O。
(5)F的结构简式为____________ 。
(6)写出下列反应的方程式:
①A与足量稀NaOH溶液共热的离子方程式_______________ 。
②D→E的化学方程式_______________ 。
(7)C的同系物中满足下列条件的同分异构体种类有______ 种(不考虑立体异构)。
①分子式为C8H8O3 ②既含有酚羟基又含有羧基

a.在稀碱溶液中,溴苯难以发生水解反应;
b.两个羟基同时连在同一碳原子上的结构是不稳定的,它将自动发生脱水反应,如:CH3CH (OH)2→CH3CHO十H2O。
回答下列问题:
(1)I中官能团的名称为
(3)D→G的反应类型是
(4)1 mol B与足量Cu(OH)2反应可生成
(5)F的结构简式为
(6)写出下列反应的方程式:
①A与足量稀NaOH溶液共热的离子方程式
②D→E的化学方程式
(7)C的同系物中满足下列条件的同分异构体种类有
①分子式为C8H8O3 ②既含有酚羟基又含有羧基
您最近一年使用:0次
2016-12-09更新
|
493次组卷
|
6卷引用:2015届湖南省常德市高三模拟考试理综化学试卷
2015届湖南省常德市高三模拟考试理综化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2016届四川省新津中学高三下学期3月月考化学试卷12016届四川省新津中学高三下学期3月月考化学试卷2江西省抚州市南城县第二中学2020-2021学年高二下学期第二次月考化学试题(已下线)专题08 有机化学基础之有机合成推断-【微专题·大素养】备战2022年高考化学核心突破(选考模块)
试卷分析
整体难度:适中
考查范围:认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础、化学与STSE、常见无机物及其应用
试卷题型(共 21题)
题型
数量
单选题
16
填空题
2
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 氧化还原反应定义、本质及特征 燃烧热 强电解质与弱电解质 同系物的判断 | |
| 2 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 物理变化与化学变化 元素、核素、同位素 几组常见同素异形体 | |
| 3 | 0.65 | 阿伏加德罗常数的应用 | |
| 4 | 0.64 | 离子共存 | |
| 5 | 0.65 | 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 6 | 0.4 | 离子反应的发生及书写 | |
| 7 | 0.94 | 分散系 | |
| 8 | 0.65 | 酯的化学性质 蛋白质 | |
| 9 | 0.94 | 化学实验基础操作 蒸馏与分馏 过滤 海水资源综合利用 | |
| 10 | 0.65 | 氧化还原反应基本概念 氧化性、还原性强弱的比较 氧化还原反应的应用 | |
| 11 | 0.4 | 过氧化钠与水的反应 过氧化钠和二氧化碳反应 过氧化钠的相关计算 | |
| 12 | 0.65 | 仪器使用与实验安全 萃取和分液 常见气体的制备与收集 | |
| 13 | 0.4 | 同分异构体确定途径——碳链异构 同分异构体确定途径——官能团位置异构 同分异构体的数目的确定 | |
| 14 | 0.65 | 酯的水解反应机理 蛋白质的水解 | |
| 15 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液稀释的有关计算 盐溶液中离子浓度大小的比较 | |
| 16 | 0.4 | 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算 硝酸的强氧化性 | |
| 二、填空题 | |||
| 17 | 0.4 | 化学反应热的计算 电解池 | |
| 18 | 0.4 | 化学实验基础 离子反应 | |
| 三、解答题 | |||
| 19 | 0.4 | 化学实验基础 | 实验探究题 |
| 20 | 0.4 | 化学实验基础 | 实验探究题 |
| 21 | 0.4 | 有机官能团的性质及结构 同分异构体的数目的确定 酯的水解反应机理 有机推断综合考查 | 有机推断题 |



