河北省大名县第一中学2018-2019学年高二(普通班)5月月考化学试题
河北
高二
阶段练习
2019-06-05
217次
整体难度:
容易
考查范围:
认识化学科学、化学与STSE、化学实验基础、常见无机物及其应用、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.李白的诗句:“日照香炉生紫烟,遥看瀑布挂前川。”生紫烟包含了物理变化。 |
| B.“熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 |
| C.唐末五代时期丹学著作《元妙道要略》中有云“以硫黄、雄黄台硝石并蜜烧之;焰起,烧手面及烬屋舍者”。描述的是丹药的制作过程 |
| D.古剑沈卢“以济钢为刃,柔铁为茎干,不尔则多折断”。济钢为钢铁。 |
| A.不慎打翻燃着的酒精灯,立即用湿抹布盖灭 |
| B.金属钠着火时,立即用泡沫灭火器进行灭火 |
| C.给盛有液体的试管加热时,要不断移动试管或加入碎瓷片 |
| D.浓碱液滴在皮肤上,立即用大量水冲洗,然后涂上3%~ 5%的硼酸溶液 |
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤;
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线;
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
| A.①②⑤ | B.①③⑤ | C.③④⑤ | D.②③⑤ |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
| A.除去碳酸氢钠固体中的少量碳酸钠:充入足量二氧化碳 |
| B.CuCl2溶液中含有FeCl3杂质:加入过量氧化铜粉末,过滤 |
| C.SO2中含有SO3杂质:通入饱和Na2SO3溶液,洗气 |
| D.CO2中含有HCl杂质:通入饱和Na2CO3溶液,洗气 |
【知识点】 物质的分离、提纯 物质分离、提纯的常见化学方法解读
| A.铝热反应(铝热剂、镁带、氯酸钾、蒸发皿) |
| B.钠的焰色反应(氯化钠溶液、盐酸、铂丝、蓝色钴玻璃) |
| C.中和热的测定(量筒、温度计、环形玻璃搅拌棒、酒精灯) |
| D.制取氢氧化铁胶体(饱和FeCl3溶液、NaOH溶液、烧杯、胶头滴管) |

| A.1处 | B.2处 | C.3处 | D.4处 |
| A.从石油中得到汽油,可用蒸馏的方法 |
| B.提取溴水中的溴,可用加入乙醇萃取的方法 |
| C.只含有泥沙的粗盐,可通过溶解、过滤、结晶的方法提纯 |
| D.除FeCl2溶液中的少量FeCl3,可用加入足量铁屑过滤的方法 |
| A.打开盛装NO的集气瓶;冷却NO2气体 |
| B.用冰水混合物冷却SO3气体;加热氯化铵晶体 |
| C.木炭吸附NO2气体;将氯气通入品红溶液中 |
| D.向酚酞溶液中加入Na2O2;向FeCl3溶液中滴加KSCN溶液 |
| A.蒸发操作时,不能等到混合物中的水分完全蒸干后才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,选择的萃取剂的密度必须比水大 |
【知识点】 化学实验基础操作解读 物质分离、提纯的常见物理方法

下列说法错误的是( )
| A.步骤(1)需要过滤装置 | B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 | D.步骤(4)需要蒸馏装置 |
| A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
| B.在溶液中先加盐酸无现象,再加BaCl2溶液,产生白色沉淀,证明原溶液中含SO42- |
| C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ |
| D.某气体可使湿润的淀粉KI试纸变蓝,证明该气体是Cl2 |
| A.14g分子式为CnH2n的烃中含有的C—H键的数目一定为2NA |
| B.1molFe与水蒸气反应生成的氢气为22.4L |
| C.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为NA |
| D.0.1molH2S分子中含氢离子数目为0.2NA |
【知识点】 阿伏加德罗常数的应用解读 烷烃的通式解读
| A.若两种气体体积相等,甲、乙两容器中气体的密度之比为35∶37 |
| B.若两种气体体积相等,甲、乙两容器中气体分子数之比为35∶37 |
| C.若两种气体质量相等,甲、乙两容器中气体所含质子数之比为37∶35 |
| D.若两种气体体积相等,甲、乙两容器中气体所含中子数之比为9∶10 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.在50 mL量筒中配制0.1000mol·L-1碳酸钠溶液 |
| B.仅用烧杯、量筒、玻璃棒就可配制100mL0.1000mol·L-1K2Cr2O7溶液 |
| C.用100mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管和pH=1的盐酸配制100mLpH=2的盐酸 |
| D.配制一定物质的量浓度的溶液时,称量药品时,若砝码生锈会导致所配溶液浓度偏低 |
A.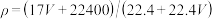 |
B.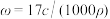 |
C.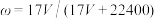 |
D. =1000Vρ/(17V+22400) =1000Vρ/(17V+22400) |
| A.0.1 mol·L-1 | B.0.2mol·L-1 | C.0.3mol·L-1 | D.0.4mol·L-1 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
| A.①④⑥ | B.②③④ | C.②③⑤ | D.①③④ |
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③同位素:1H、2H、3H;干冰、液氯都是非电解质
④电解质:明矾、冰醋酸、纯碱;同素异形体:C60、金刚石、石墨
⑤根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
| A.只有②④ | B.只有②③⑤ | C.只有①②④ | D.只有②③⑤ |
| A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 |
| B.用于人民币票面方案等处的油墨中所含有的Fe3O4是一种磁性物质 |
| C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 |
| D.某种验钞笔中含有碘酒,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖 |
| A.NaHSO4溶液与Ba(OH)2溶液混合 | B.NH4Cl溶液与Ca(OH) 2溶液混合 |
| C.HNO3溶液与KOH溶液混合 | D.Na2HPO4溶液与NaOH溶液混合 |
【知识点】 离子反应的发生及书写
| A.钠与水反应:Na +2H2O=Na++2OH–+H2↑ |
B.电解饱和食盐水获取烧碱和氯气:2Cl–+2H2O H2↑+Cl2↑+2OH– H2↑+Cl2↑+2OH– |
| C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH–+H++SO42-=BaSO4↓+H2O |
| D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH–=CaCO3↓+H2O |
【知识点】 离子反应的发生及书写
| A.NaHSO3溶液呈酸性:NaHSO3===Na++H++SO32- |
| B.向Na2SiO3溶液中通入少量CO2:SiO32-+CO2+H2O===H2SiO3↓+CO32- |
| C.将一小块钠投入稀醋酸中:2Na+2H+===2Na++H2↑ |
| D.在Na2S2O3溶液中滴加稀硝酸:2H++S2O32-===S↓+SO2↑+H2O |
【知识点】 离子方程式的正误判断解读
| A.29 : 8 : 13 | B.13 : 8 : 13 | C.22 : 1 : 14 | D.26 : 18 : 13 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.0.8g | B.1.6g | C.2.4g | D.3.2g |
【知识点】 物质的量有关计算
二、解答题 添加题型下试题

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
三、填空题 添加题型下试题
①硫酸 ②盐酸 ③氯气 ④硫酸钡 ⑤酒精 ⑥铜 ⑦醋酸 ⑧氯化氢 ⑨蔗糖 ⑩氨气 ⑪CO2 ⑫NaHCO3 ⑬A l(OH)3 ⑭NaOH
(1)属于非电解质的为
(2)写出下列反应的离子方程式
①NaHCO3溶于醋酸:
②过量CO2与NaOH溶液反应:
③Cl2通入NaOH溶液中:
四、解答题 添加题型下试题
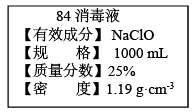
(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是
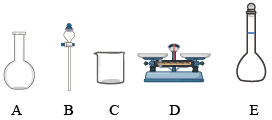
| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| D.需要称量NaClO固体的质量为143.0g |
①所配制的稀硫酸中,H+的物质的量浓度为
②需用浓硫酸的体积为
五、计算题 添加题型下试题
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是
(3)2.3gNa中含
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)
六、解答题 添加题型下试题
(1)分别写出三只烧杯中形成分散系的名称:A
(2)写出C中形成分散系的化学方程式:
(3)若不用化学试剂鉴别,写出鉴别B、C分散系的两种简单方法:
①
②
(4)向C中逐滴加入稀H2SO4,现象为
【知识点】 分散系概念及其分类解读 物质性质实验方案的设计解读
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 物理变化与化学变化 四种基本反应类型 化学科学对人类文明发展的意义 金属与合金性能比较 | |
| 2 | 0.65 | 仪器使用与实验安全 化学实验基础操作 实验安全 | |
| 3 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 4 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见化学方法 | |
| 5 | 0.65 | 胶体的制备 焰色试验 铝热反应 中和热的测定与误差分析 | |
| 6 | 0.85 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | |
| 7 | 0.85 | 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 8 | 0.65 | 氯水 一氧化氮的化学性质 过氧化钠 铁盐的检验 | |
| 9 | 0.65 | 化学实验基础操作 物质分离、提纯的常见物理方法 | |
| 10 | 0.94 | 化学实验基础操作 蒸馏与分馏 过滤 海水资源综合利用 | |
| 11 | 0.85 | 离子的检验 常见阳离子的检验 | |
| 12 | 0.65 | 阿伏加德罗常数的应用 烷烃的通式 | |
| 13 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 14 | 0.65 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | |
| 15 | 0.4 | 物质的量浓度的基础计算 物质的量浓度与溶质成分有关的计算 | |
| 16 | 0.94 | 物质的量浓度计算-溶液混合的有关计算 | |
| 17 | 0.85 | 胶体的定义及分类 胶体的性质和应用 | |
| 18 | 0.65 | 无机综合推断 铁 | |
| 19 | 0.65 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 分散系概念及其分类 非电解质、电解质物质类别判断 | |
| 20 | 0.85 | 淀粉和纤维素 糖类的来源及用途 | |
| 21 | 0.65 | 离子反应的发生及书写 | |
| 22 | 0.65 | 离子反应的发生及书写 | |
| 23 | 0.65 | 离子方程式的正误判断 | |
| 24 | 0.65 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 25 | 0.4 | 物质的量有关计算 | |
| 二、解答题 | |||
| 26 | 0.65 | 蒸发与结晶 蒸馏与分馏 萃取和分液 过滤 | 实验探究题 |
| 28 | 0.85 | 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液稀释的有关计算 一定物质的量浓度的溶液的配制 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 30 | 0.85 | 分散系概念及其分类 物质性质实验方案的设计 | 原理综合题 |
| 三、填空题 | |||
| 27 | 0.94 | 电解质与非电解质 非电解质、电解质物质类别判断 物质水溶液的导电性 离子方程式的书写 | |
| 四、计算题 | |||
| 29 | 0.94 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 以N=m·NA/M为中心的有关基本粒子的推算 | |