陕西省吴起高级中学2019-2020学年高一上学期期中考试化学(能力卷)试题
陕西
高一
期中
2019-11-11
218次
整体难度:
适中
考查范围:
物质结构与性质、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.Ne | B.Mg | C.S | D.C |
【知识点】 元素性质与原子结构的关系解读
| A.乳浊液 | B.溶液 | C.胶体 | D.悬浊液 |
| A.氧化物、化合物 | B.溶液、分散系 |
| C.含氧酸、酸 | D.化合物、电解质 |
【知识点】 物质的分类
| A.1 molH2O的质量为18g/mol |
| B.含有3.01×1023个氧原子的SO2分子的质量约为16g |
| C.CH4的摩尔质量为16g |
| D.标准状况下,1mol任何物质体积均为22.4L |
A.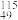 In原子核外有49个电子 In原子核外有49个电子 |
B.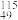 In原子核内有49个中子 In原子核内有49个中子 |
C.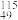 In原子核内质子数和中子数之和为115 In原子核内质子数和中子数之和为115 |
D.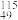 In是In元素的一种核素 In是In元素的一种核素 |
【知识点】 核素 原子的基本构成解读 原子中相关数值及其之间的相互关系解读
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.常温下,28gN2所含有的原子数目为2NA |
| B.标准状况下,22.4L的H2中所含分子数为NA |
| C.标准状况下,1molO2所占的体积约为22.4 L |
| D.24gMg与足量的盐酸完全反应转移的电子数为NA |
【知识点】 阿伏加德罗常数的求算解读 物质的量有关计算
A.H2 + Cl2  2HCl 2HCl | B.2HClO  2HCl+O2 2HCl+O2 |
| C.2NaI + Br2 = 2NaBr+ I2 | D.CaCl2 + Na2CO3=CaCO3↓+2NaCl |
【知识点】 氧化还原反应基本概念
 3Mn+2Al2O3,该反应的氧化剂是( )
3Mn+2Al2O3,该反应的氧化剂是( )| A.MnO2 | B.Al | C.Mn | D.Al2O3 |
| A.HCl→Cl2 | B.MnO4-→Mn2+ | C.KClO3→O2 | D.Fe→Fe2+ |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的应用
| A.2Fe2++I2=2Fe3++2I- | B.Br2+H2S=S+2HBr |
| C.2Fe3++2I-=2Fe2++I2 | D.Br2+2Fe2+=Fe3++2Br- |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
| A.两容器中气体的质量相等 | B.两容器中气体的分子数目相等 |
| C.两容器中气体的氧原子数目相等 | D.两容器中气体的密度相等 |
【知识点】 阿伏加德罗定律 物质的量的含义解读 阿伏加德罗定律的应用解读
| A.150mL 1mol·L-1的NaCl | B.100mL 1.5mol·L-1的CaCl2 |
| C.75mL 2mol·L-1的NH4Cl | D.150mL 2mol·L-1的KCl |
| A.应称取该碳酸钠晶体128.7 g |
| B.取 100 mL 该溶液,向其中加入100 mL 水,所得溶液浓度为0.5 mol/L |
| C.定容时俯视刻度线会引起配制溶液的浓度偏高 |
| D.定容、摇匀、静置后发现液面低于刻度线,应再补加少量水至刻度线 |
【知识点】 一定物质的量浓度的溶液的配制
| A.蒸发操作时,不能等到混合物中的水分完全蒸干后才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,选择的萃取剂的密度必须比水大 |
【知识点】 化学实验基础操作解读 物质分离、提纯的常见物理方法
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,一定有CO32- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C.加入氢氧化钠溶液并加热产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| D.加入硝酸银溶液产生白色沉淀,再加盐酸白色沉淀不消失,一定有Cl- |
| A.漂白粉被氧化了 |
| B.有色布条被空气中的氧气氧化了 |
| C.漂白粉跟空气中的CO2反应充分,生成了较多量的 HClO |
| D.漂白粉溶液蒸发掉部分水,其浓度增大 |
【知识点】 次氯酸及其性质解读 漂白粉和漂粉精 漂白粉的变质原因及检验解读
四、填空题 添加题型下试题
(1)硫酸铝的电离方程式:
(2)BaCO3与稀盐酸溶液反应的化学方程式:
(3)实验室制氯气的化学方程式:
(4)写出工业制漂白粉的化学方程式:
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用
(2)为了从氯化钾和二氧化锰的混合物中获得氯化钾,可先加足量的水溶解,过滤,将得到的滤液
(3)除去氧化钙中的碳酸钙,可用
(4)从溴水中提取溴单质,可用
(5)分离沸点相差较大的液体混合物,可用
(1)用双线桥标出电子转移的方向和数目
(2)该反应中,氧化剂是
Ⅱ.铜绿即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
(1)用单线桥标出电子转移的方向和数目
(2)该反应中的还原剂是
Ⅲ.氮化铝具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可以通过如下方式合成:Al2O3+N2+3C=2AlN+3CO
(1)用单线桥标出该反应中电子转移的方向和数目
(2)该反应中的还原剂是
五、解答题 添加题型下试题

回答下列问题:
(1)装置A中,仪器a的名称叫
(2)装置B的作用是
(3)当有少量Cl2通过后,观察到装置C中溶液变成
(4)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?为什么
(5)若要证明Cl2无漂白性,则必须在装置D之前加一个装有
(6)装置E的作用是
六、计算题 添加题型下试题
求:(1)生成Cl2在标况下的体积?
(2)求盐酸的浓度?
(3)如果恰好完全反应,求所需盐酸的体积?
【知识点】 化学方程式计算中物质的量的运用解读
试卷分析
试卷题型(共 23题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 元素性质与原子结构的关系 | |
| 2 | 0.65 | 胶体的定义及分类 | |
| 3 | 0.85 | 物质的分类 | |
| 4 | 0.85 | 摩尔质量的概念 22.4L/mol适用条件 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 5 | 0.85 | 核素 原子的基本构成 原子中相关数值及其之间的相互关系 | |
| 7 | 0.85 | 电离方程式 | |
| 8 | 0.65 | 阿伏加德罗常数的求算 物质的量有关计算 | |
| 9 | 0.85 | 氧化还原反应基本概念 | |
| 10 | 0.94 | 氧化还原反应的几组概念 氧化还原反应方程式的配平 氧化还原反应的规律 铝热反应 | |
| 11 | 0.85 | 氧化还原反应的几组概念 氧化还原反应的应用 | |
| 12 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 13 | 0.65 | 阿伏加德罗定律 物质的量的含义 阿伏加德罗定律的应用 | |
| 14 | 0.85 | 物质的量浓度 物质的量浓度概念、含义 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度计算-与溶质成分有关的计算 | |
| 15 | 0.65 | 一定物质的量浓度的溶液的配制 | |
| 16 | 0.65 | 化学实验基础操作 物质分离、提纯的常见物理方法 | |
| 17 | 0.65 | 硫酸根离子的检验 离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 18 | 0.65 | 次氯酸及其性质 漂白粉和漂粉精 漂白粉的变质原因及检验 | |
| 二、未知 | |||
| 6 | 0.85 | 氧化还原反应定义、本质及特征 | 未知 |
| 三、填空题 | |||
| 19 | 0.65 | 电离方程式 氯气的实验室制法 漂白粉和漂粉精的制备原理 | |
| 20 | 0.65 | 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 21 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 | |
| 四、解答题 | |||
| 22 | 0.65 | 氯气的化学性质 氯气的实验室制法 | 实验探究题 |
| 五、计算题 | |||
| 23 | 0.65 | 化学方程式计算中物质的量的运用 | |



