江西省奉新县第一中学2021届高三上学期第二次月考化学试题
江西
高三
阶段练习
2020-10-24
490次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、化学与STSE、有机化学基础
江西省奉新县第一中学2021届高三上学期第二次月考化学试题
江西
高三
阶段练习
2020-10-24
490次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、化学与STSE、有机化学基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 室温下,下列各组离子在溶液中能大量共存的是( )
| A.Fe3+、Na+、ClO-、SCN- | B.OH-、K+、Br-、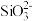 |
C.Ba2+、Al3+、 、 、 | D.Cl-、Mg2+、 、OH- 、OH- |
【知识点】 离子共存
您最近一年使用:0次
单选题
|
适中(0.65)
名校
2. 下列各组物质按照纯净物、混合物、强、弱电解质和非电解质顺序排列的是( )
| A.氯水,水煤气,硫酸,醋酸,干冰 |
| B.冰醋酸,福尔马林,硫酸钡,次氯酸,乙醇 |
| C.单甘油酯,混甘油酯,水玻璃,氢硫酸,三氧化硫 |
| D.胆矾,漂白粉,氯化钾,氢氟酸,氯气 |
您最近一年使用:0次
2019-09-07更新
|
532次组卷
|
5卷引用:陕西省咸阳市三原县南郊中学2020届第一次月考化学试题
单选题
|
适中(0.65)
名校
3. 下列试剂的保存方法正确的是( )
| A.少量金属钠保存在水中 |
| B.新制氯水存放在带玻璃塞的无色细口瓶中 |
| C.碳酸钠固体保存在带橡胶塞的广口瓶中 |
| D.浓硝酸保存在带橡胶塞的无色玻璃瓶中 |
您最近一年使用:0次
2019-11-03更新
|
156次组卷
|
3卷引用:江西省赣州市寻乌中学2020届高三上学期第一阶段考试化学试题
单选题
|
适中(0.65)
真题
名校
4. 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA |
| B.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
【知识点】 阿伏加德罗常数的应用解读
您最近一年使用:0次
2019-01-30更新
|
3078次组卷
|
23卷引用:2012年普通高等学校招生全国统一考试理综化学部分(四川卷)
2012年普通高等学校招生全国统一考试理综化学部分(四川卷)(已下线)2013届山西省忻州一中高三第一次月考化学试卷(已下线)2015届江西师大附中高三年级10月月考化学试卷2015届江苏常州市高三第一次调研试卷化学试卷2016届四川省彭州中学高三9月月考化学试卷2016届甘肃省天水市秦安县第二中学高三上第一次检测考试化学试卷2016届江西省丰城中学课改实验班高三上学期10月月考化学试卷2015-2016学年湖南省双峰一中高一下期中理科化学试卷2017届江西省上高二中高三上第二次月考化学试卷2016-2017学年辽宁省铁岭市清河高级中学高二下学期第一阶段考试化学试卷江西省南昌市第三中学2016-2017学年高一下学期期末考试化学试题广东省阳东广雅学校2018届高三上学期第一次月考化学试题湖南省衡阳县第一中学2018届高三上学期第二次月考化学试题河南省安阳市第三十六中学2018届高三上学期第一次月考化学试题浙江省杭州市学军中学2018届高三选考前适应性练习(2)化学试题安徽省滁州市定远县民族中学2017-2018学年高一下学期期末考试化学试题河南省安阳市第三实验中学2019届高三上学期11月月考化学试题陕西省榆林市第二中学2018-2019学年高二下学期期中考试化学试题江西省奉新县第一中学2021届高三上学期第二次月考化学试题广西梧州市2021届高三3月联考理科综合化学试题山西省晋中市新一双语学校2021-2022学年高三上学期8月月考化学试题(已下线)专题01 阿伏加德罗常数正误判断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)河南省郑州中学2023-2024学年高三上学期第二次月考化学试题
单选题
|
较易(0.85)
名校
5. 金属钾的冶炼可采用如下方法:2KFCaC2 CaF22K2C,下列有关说法合理的是
CaF22K2C,下列有关说法合理的是
 CaF22K2C,下列有关说法合理的是
CaF22K2C,下列有关说法合理的是| A.该反应的氧化剂是KF,氧化产物是K |
| B.该反应能说明C的还原性大于K |
| C.电解KF水溶液不可能制备金属钾 |
| D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2:1 |
您最近一年使用:0次
2020-07-29更新
|
232次组卷
|
10卷引用:2014届湖南省长沙市重点中学高三第四次月考化学试卷
(已下线)2014届湖南省长沙市重点中学高三第四次月考化学试卷2016届江西省九江市七校高三第一次联考化学试卷陕西省西安中学2016-2017学年高一(实验班)下学期期中考试化学试题【全国百强校】湖南省衡阳市第八中学2019届高三上学期第二次月考化学试题黑龙江省宾县一中2020届高三上学期第一次月考化学试题云南省南华县一中2019-2020学年高二上学期开学考试化学试题湖南省常德市芷兰实验学校2020届高三第二次月考化学试题2020届人教版高中化学高三专题基础复习专题3《金属及其化合物》测试卷湖南省长沙市雅礼中学2019-2020学年高二下学期期末考试化学试题江西省奉新县第一中学2021届高三上学期第二次月考化学试题
单选题
|
适中(0.65)
名校
6. 在给定条件下,下列选项所示物质间不满足每一步转化均能实现的是( )
A.N2(g) NO(g) NO(g) NaNO2(aq) NaNO2(aq) |
B.SiO2(s) Na2SiO3(aq) Na2SiO3(aq)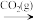 H2SiO3(s) H2SiO3(s) |
C.Al(s) NaAlO2(aq) NaAlO2(aq)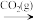 Al(OH)3(s) Al(OH)3(s) |
D.Fe2O3(s)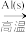 Fe(s) Fe(s) Fe(NO3)3(aq) Fe(NO3)3(aq) |
您最近一年使用:0次
2020-09-25更新
|
662次组卷
|
6卷引用:河北省唐山市2021届高三上学期第一次摸底考试化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 下列各组溶液,不需要其它试剂就可以鉴别出来的是( )
| A.AgNO3、NaCl、Na2SO4、NaI | B.Na2SO4、KNO3、(NH4)2SO4、MgCl2 |
| C.FeCl3、NaOH、NaCl、NaNO3 | D.NaCl、HCl、NaAlO2、NaHCO3 |
【知识点】 无机物的检验
您最近一年使用:0次
单选题
|
适中(0.65)
名校
8. 工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )
8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )
 8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )
8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )| A.反应①和②均为氧化还原反应 |
| B.反应①的氧化剂是O2,还原剂是FeO·Cr2O3 |
| C.高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 |
| D.反应①中每生成1 mol Na2CrO4时转移电子3 mol |
您最近一年使用:0次
2019-10-02更新
|
337次组卷
|
12卷引用:2013届湖北省孝感一中高三第一次阶段性考试化学试卷
(已下线)2013届湖北省孝感一中高三第一次阶段性考试化学试卷(已下线)2014届江西省师大附中高三上学期期中考试化学试卷(已下线)2014届江西省师大附中高三上学期期中考试化学试卷(已下线)2015届江西省上高二中高三上学期第二次月考化学试卷2015届上海市十三校高三第二次联考化学试卷辽宁师范大学附属中学2018届高三上学期期末考试化学试题【全国百强校】新疆生产建设兵团第二中学2017-2018学年高二下学期期末考试化学试题河北省大名县第一中学(清北班,一)2020届高三9月月考化学试题上海市复旦大学附中2017-2018学年高二上学期期中考试化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应江西省奉新县第一中学2021届高三上学期第二次月考化学试题陕西省汉中中学2021-2022学年高二下学期4月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 工业上制备高纯硅有多种方法,其中的一种工艺流程如下:
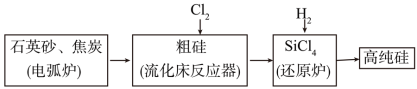
已知:流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等。下列说法正确的是

已知:流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等。下列说法正确的是
A.电弧炉中发生的反应为 |
| B.SiCl4进入还原炉之前需要经过蒸馏提纯 |
C.每生成 高纯硅,需要 高纯硅,需要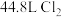 (标准状况) (标准状况) |
D.该工艺 的产率高,符合绿色化学要求 的产率高,符合绿色化学要求 |
您最近一年使用:0次
2022-04-05更新
|
835次组卷
|
28卷引用:湖北省黄冈市2019届高三上学期9月质量检测化学试题
湖北省黄冈市2019届高三上学期9月质量检测化学试题【全国市级联考】湖北省黄冈市2019届高三9月质量检测化学试题河北省承德一中2019届高三上学期第二次月考(期中)化学试题江西省宜春市上高二中2020届高三上学期第三次月考化学试题江西省上高县第二中学2020届高三上学期第三次月考化学试题会做实验2020届高三化学实验复习——过滤、蒸馏、冷凝、结晶、洗气的再练习 【选择突破】(已下线)第13讲 碳、硅及无机非金属材料(精练)——2021年高考化学一轮复习讲练测江西省奉新县第一中学2021届高三上学期第二次月考化学试题江西省南昌市新建一中2021届高三期中考试化学试题新疆北屯高级中学2021届高三上学期10月月考化学试题江苏省盐城中学2021届高三上学期第三次阶段性质量检测化学试题江西省南昌市第二中学2020-2021学年高一上学期第三次月考化学试题(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第09讲 无机非金属材料 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)云南省玉溪市江川区第二中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)重庆市实验中学校2021-2022学年高三上学期11月月考化学试题湖南省常德市桃源县第一中学2022届高三下学期第二次模拟化学试题(已下线)专题13 物质的反应和转化-2022年高考真题模拟题分项汇编(已下线)第14练 无机非金属材料-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题29 非金属及其化合物制备流程与实验探究(Si、N、P、As)-备战2023年高考化学一轮复习考点微专题超重点7 金属与非金属交界处的3种重要元素(已下线)第7讲 碳、硅及无机非金属材料黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题
单选题
|
适中(0.65)
名校
10. 下列有关化学用语的用法中,正确的是
A.BaCO3的电离方程式:BaCO3 Ba2++CO32— Ba2++CO32— |
| B.向沸水中滴加饱和氯化铁溶液得到红褐色液体的化学方程式:3H2O+FeCl3=3HCl+Fe(OH)3↓ |
| C.向酸性KI溶液中通入臭氧(O3)的离子方程式:2I—+O3+H2O==I2+O2+2OH— |
| D.向Ba(OH)2溶液中滴入 NaHSO4溶液至恰好完全沉淀时,反应的离子方程式Ba2++OH—+SO42—+H+==BaSO4↓+H2O |
您最近一年使用:0次
2019-09-03更新
|
262次组卷
|
5卷引用:安徽省皖江名校联盟2020届高三8月第一次联考化学试题
单选题
|
适中(0.65)
名校
解题方法
11. 8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示,下列说法正确的是


| A.温度为78℃时固体物质M的化学式为FeSO4•5H2O |
| B.温度为l59℃时固体物质N的化学式为FeSO4•3H2O |
C.在隔绝空气条件下,N得到P的化学方程式为 FeSO4 FeO+SO3↑ FeO+SO3↑ |
| D.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |
【知识点】 物质的量有关计算 亚铁盐 探究物质组成或测量物质的含量解读
您最近一年使用:0次
2016-12-09更新
|
247次组卷
|
6卷引用:2014高考名师推荐化学铁及其化合物主要性质
单选题
|
适中(0.65)
名校
解题方法
12. 中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是( )


| A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉 |
| B.选用合适的溶液,CO2也能用于做喷泉实验 |
| C.HCl、NH3均能用该装置做喷泉实验 |
| D.用NO2和N2O4的混合气体做喷泉实验,烧瓶中将充满稀硝酸 |
您最近一年使用:0次
2020-10-20更新
|
188次组卷
|
2卷引用:江西省奉新县第一中学2021届高三上学期第二次月考化学试题
单选题
|
适中(0.65)
名校
13. 下列实验方案、现象、得出的结论均正确的是( )
| 选项 | 实验及现象 | 结论 |
| A | 用玻璃棒蘸取某样品进行焰色反应时观察到黄色火焰 | 该样品含钠元素 |
| B | 向NaHCO3溶液中加入过量盐酸振荡、静置、有气泡产生 | 证明非金属性Cl>C |
| C | 向酸化的KMnO4溶液通入SO2,向反应后的溶液中加入BaCl2产生白色沉淀 | 证明SO2被氧化为SO42- |
| D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN,溶液颜色变红 | KI与FeCl3反应有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-08-28更新
|
3203次组卷
|
15卷引用:【全国校级联考】辽宁省六校协作体2019届高三上学期期初联考化学试题
【全国校级联考】辽宁省六校协作体2019届高三上学期期初联考化学试题河南省许昌高级中学2020届高三上学期第一次月考化学试题辽宁省抚顺市第十中学2018-2019学年高二下学期期中考试化学试题山东省济宁市2020届高三10月月考化学试卷山东省济宁市邹城第一中学2020届高三10月月考化学试题山东省莱阳市第一中学2020届高三10月月考化学试题河北省石家庄市行唐县三中2020届高三11月月考化学试题江西省南昌市新建县第一中学2020届高三上学期第二次月考化学试题甘肃省天水市一中2020届高三上学期第四次考试化学试题内蒙古包钢第一中学2020届高三上学期10月月考化学试题黑龙江省鹤岗市第一中学2021届高三上学期第一次月考(开学考试)化学试题江西省奉新县第一中学2021届高三上学期第二次月考化学试题湖南省邵东县第一中学2021届高三上学期第三次月考化学试题陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期8月月考化学试题
单选题
|
较易(0.85)
名校
14. 利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
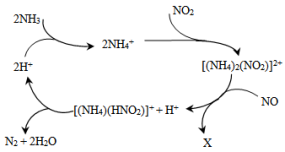
| A.X是N2O |
| B.汽车尾气中含有的氮氧化合物是由于汽油燃烧产生的 |
C.NH 中含有非极性共价键 中含有非极性共价键 |
D.上述历程的总反应为:2NH3+NO+NO2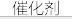 2N2+3H2O 2N2+3H2O |
您最近一年使用:0次
2021-03-17更新
|
338次组卷
|
12卷引用:江西省南昌市第二中学2020届高三第四次月考化学试题
江西省南昌市第二中学2020届高三第四次月考化学试题江西省顶级名校2020届高三第四次联考化学试题江西省南昌市新建县第一中学2020届高三上学期第二次月考化学试题新人教版必修2同步测试:5.2.1一氧化氮和二氧化氮河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题江西省奉新县第一中学2021届高三上学期第二次月考化学试题湖北省六校(恩施高中 郧阳中学 沙市中学 十堰一中 随州二中 襄阳三中)2021届高三11月联考化学试题专题7 第三单元综合拔高练-高中化学必修第二册苏教版2019北京市昌平区新学道临川学校2021届高三上学期期末考试化学试题吉林省东北师范大学附属中学2021届高三第五次模拟考试理科综合化学试题辽宁省沈阳市第一二〇中学2022-2023学年高一下学期期初质量监测化学试题(已下线)选择题7-12
单选题
|
适中(0.65)
名校
解题方法
15. 下列说法中正确的个数有( )
①由同一种元素组成的物质是单质 ②阴离子不含金属元素,阳离子含金属元素
③金属氧化物一定是碱性氧化物 ④碱性氧化物一定是金属氧化物 ⑤非金属氧化物一定是酸性氧化物 ⑥酸性氧化物一定是非金属氧化物 ⑦酸酐一定是氧化物 ⑧酸的元数不一定等于酸中的H原子数 ⑨ 无氧酸不一定是非金属的氢化物
①由同一种元素组成的物质是单质 ②阴离子不含金属元素,阳离子含金属元素
③金属氧化物一定是碱性氧化物 ④碱性氧化物一定是金属氧化物 ⑤非金属氧化物一定是酸性氧化物 ⑥酸性氧化物一定是非金属氧化物 ⑦酸酐一定是氧化物 ⑧酸的元数不一定等于酸中的H原子数 ⑨ 无氧酸不一定是非金属的氢化物
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
16. 将KClO3、I2各0.02mol加入12g 36.5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发).将反应后的溶液用冰水冷却,析出橙红色晶体A(A在常温下就有升华现象),过滤,将滤液蒸干,收集到KCl固体、8.7g液态水和极少量的A蒸气.则A的化学式可能是
| A.I2Cl6 | B.HClO | C.IClO | D.KIO3 |
【知识点】 基于氧化还原反应守恒规律的计算解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
名校
解题方法
17. 有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的。
为了鉴别上述化合物,分别完成以下实验,其结果是
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________ ,D________ 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为__________________________ 。
(3)C常用作净水剂,用离子方程式表示其净水原理:________________________ 。
(4)在A溶液中加入少量澄清石灰水,其离子方程式为___________________ 。
| 阳离子 | K+、Na+、Cu2+、Al3+ |
| 阴离子 | SO42-、HCO3-、NO3-、OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
(3)C常用作净水剂,用离子方程式表示其净水原理:
(4)在A溶液中加入少量澄清石灰水,其离子方程式为
您最近一年使用:0次
2017-06-26更新
|
252次组卷
|
2卷引用:苏教版2017届高三单元精练检测二化学试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
18. 氯化钴渗入水泥中可以制备彩色水泥(变色水泥)。以某废钴渣(主要成分为Co2O3,含少量Fe3O4、Al2O3和SiO2)制备氯化钴晶体的一种流程如下:

已知:在酸性条件下,氧化性Co3+>Cl2>H2O2>Fe3+。
请回答下列问题:
(1)滤渣A的主要成分是________ (填化学式);提高废钴渣溶解速率的措施宜采用__________________ (任写一点)。
(2)在滤液A中加入H2O2,H2O2作还原剂的离子方程式为__________________ 。
(3)从滤渣B中提取铁红的操作是将滤渣B溶于过量的________ 溶液(填化学式),________ ,洗涤、灼烧得到铁红。
(4)从环境保护角度分析,不用浓盐酸替代硫酸的原因是__________________ 。
(5)为了测定CoCl2·nH2O中结晶水数目进行如下实验:取18.4 g样品在一定条件下脱水得13.0 g CoCl2,则n=________ 。

已知:在酸性条件下,氧化性Co3+>Cl2>H2O2>Fe3+。
请回答下列问题:
(1)滤渣A的主要成分是
(2)在滤液A中加入H2O2,H2O2作还原剂的离子方程式为
(3)从滤渣B中提取铁红的操作是将滤渣B溶于过量的
(4)从环境保护角度分析,不用浓盐酸替代硫酸的原因是
(5)为了测定CoCl2·nH2O中结晶水数目进行如下实验:取18.4 g样品在一定条件下脱水得13.0 g CoCl2,则n=
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
名校
解题方法
19. 氯化亚砜(SOCl2)常用于医药、农药、染料工业,也可在有机合成工业中作氯化剂。已知:SOCl2的相关性质如下表所示:
现利用如图装置制备SOCl2。

请回答下列问题:
Ⅰ.制备SO2和Cl2。
(1)本实验选用装置甲制备SO2和Cl2,装置甲中仪器x的名称为_________ ;若以KMnO4和浓盐酸反应制备Cl2,反应的离子方程式为_____________ 。
Ⅱ.制备SOCl2。
以活性炭作为催化剂,SO2和C12可以和S粉在180~200℃时反应合成SOCl2,选用装置A、B、C、D进行制备(夹持、加热装置略去)。
(2)按气流从左到右的方向,装置A、B、C、D的连接顺序为______ (填仪器接口的字母编号)。
(3)试剂y为__________ (填选项字母,下同);试剂z为______________ 。
A.热水 B.乙醇 C.石蜡油 D.冰水
(4)装置A中U形管内发生反应的化学方程式为________________ 。
(5)装置C的作用为_____________ ;若装置A处通入的SO2和Cl2的物质的量之比为1:3,请设计实验验证装置C中生成的盐中含有 :
:_______________ 。
| 颜色、状态 | 熔点 | 沸点 | 腐蚀性 | 水解 |
| 无色或微黄液体 | -105℃ | 78℃ | 强 | 极易水解 |

请回答下列问题:
Ⅰ.制备SO2和Cl2。
(1)本实验选用装置甲制备SO2和Cl2,装置甲中仪器x的名称为
Ⅱ.制备SOCl2。
以活性炭作为催化剂,SO2和C12可以和S粉在180~200℃时反应合成SOCl2,选用装置A、B、C、D进行制备(夹持、加热装置略去)。
(2)按气流从左到右的方向,装置A、B、C、D的连接顺序为
(3)试剂y为
A.热水 B.乙醇 C.石蜡油 D.冰水
(4)装置A中U形管内发生反应的化学方程式为
(5)装置C的作用为
 :
:
您最近一年使用:0次
三、计算题 添加题型下试题
计算题
|
适中(0.65)
名校
解题方法
20. 取一定量的Fe、Cu的混合物粉末,平均分成A、B、C、D、E五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(惟一还原产物)的体积及所得剩余物的质量记录如下(所有体积均在标准状况下测定):
(1)A组实验后17.2 g剩余固体为___________ (均填写化学式)
(2)实验中每次所取混合物中铁的物质的量为________ mol。
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:____ ,物质的量之比是:___ 。
| 实验序号 | A | B | C | D | E |
| 硝酸溶液体积 | 100ml | 200 mL | 300 mL | 400 mL | 500 mL |
| 剩余固体的质量 | 17.2 g | 8g | 0 g | 0 g | 0 g |
| 气体体积 | 2.24 L | 4.48 L | 6.72L | 7.84 L | 7.84 L |
(1)A组实验后17.2 g剩余固体为
(2)实验中每次所取混合物中铁的物质的量为
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
名校
解题方法
21. 如图中的Ⅰ是某抗肿瘤药物的中间体,B的核磁共振氢谱有3组峰,C的分子式为C7H8O,D分子中有两个相同且处于相邻位置的含氧官能团,E的相对分子质量比D大34.5。

已知:RCHO+R1CH2CHO RCH=C(R1)CHO+H2O。
RCH=C(R1)CHO+H2O。
请回答下列问题:
(1)A的名称是______ ,B的结构简式为_________ ,D转化为E的反应类型是____________ 。
(2)I的分子式为________ 。
(3)写出E转化为F的化学方程式____________ 。
(4)X是G酸化后的产物,X有多种芳香族同分异构体,符合下列条件且能发生银镜反应的同分异构体有____ 种(不包括X),写出核磁共振氢谱有4组峰的物质的结构简式____________ 。
①遇FeCl3溶液发生显色反应 ②苯环上有两种类型的取代基
(5)参照上述流程,以乙醇为原料(其他无机试剂自选)可制取2﹣丁烯酸,写出相应的合成路线__________________ 。

已知:RCHO+R1CH2CHO
 RCH=C(R1)CHO+H2O。
RCH=C(R1)CHO+H2O。请回答下列问题:
(1)A的名称是
(2)I的分子式为
(3)写出E转化为F的化学方程式
(4)X是G酸化后的产物,X有多种芳香族同分异构体,符合下列条件且能发生银镜反应的同分异构体有
①遇FeCl3溶液发生显色反应 ②苯环上有两种类型的取代基
(5)参照上述流程,以乙醇为原料(其他无机试剂自选)可制取2﹣丁烯酸,写出相应的合成路线
【知识点】 有机物的合成 有机物的推断 根据题给物质选择合适合成路线解读
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础、化学与STSE、有机化学基础
试卷题型(共 21题)
题型
数量
单选题
16
解答题
4
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 离子共存 | |
| 2 | 0.65 | 树状分类法 分类方法的应用 无机物质的分类 非电解质、电解质物质类别判断 | |
| 3 | 0.65 | 氯水的性质 硝酸的强氧化性 钠单质的保存与用途 碳酸钠的俗称、物理性质及用途 | |
| 4 | 0.65 | 阿伏加德罗常数的应用 | |
| 5 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 电解原理的理解及判断 共价键与离子键的比较 | |
| 6 | 0.65 | 硝酸的强氧化性 硅酸与硅酸盐 铝与强碱溶液反应 与“铁三角”有关的推断 | |
| 7 | 0.65 | 无机物的检验 | |
| 8 | 0.65 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 9 | 0.65 | 硅的制备 二氧化硅的化学性质 绿色化学与可持续发展 | |
| 10 | 0.65 | 电离方程式 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 11 | 0.65 | 物质的量有关计算 亚铁盐 探究物质组成或测量物质的含量 | |
| 12 | 0.65 | 氨的喷泉实验 二氧化氮 酸性氧化物的通性 综合实验设计与评价 | |
| 13 | 0.65 | 二氧化硫 可逆反应及反应限度 常见阳离子的检验 化学实验方案的设计与评价 | |
| 14 | 0.85 | 氧化还原反应的应用 氧化还原反应方程式的书写与配平 共价键概念及判断 | |
| 15 | 0.65 | 单一分类法 树状分类法 分类方法的应用 | |
| 16 | 0.65 | 基于氧化还原反应守恒规律的计算 | |
| 二、解答题 | |||
| 17 | 0.65 | 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 | 无机推断题 |
| 18 | 0.65 | 含氧化铝的混合物的提纯 物质分离、提纯综合应用 探究物质组成或测量物质的含量 | 工业流程题 |
| 19 | 0.65 | 氯气的实验室制法 氯气与还原性化合物的反应 化学实验基础操作 常见阴离子的检验 | 实验探究题 |
| 21 | 0.65 | 有机物的合成 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |
| 三、计算题 | |||
| 20 | 0.65 | 硝酸的强氧化性 铁与强氧化性酸的反应 铜与强氧化性酸的反应 探究物质组成或测量物质的含量 | |



