四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题
四川
高二
期中
2019-12-22
259次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学
一、单选题 添加题型下试题
A.KOH(aq)+ H2SO4(aq)= H2SO4(aq)= K2SO4(aq)+H2O(l) △H=-11.46 kJ·mol-1 K2SO4(aq)+H2O(l) △H=-11.46 kJ·mol-1 |
| B.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l) △H=-11.46 kJ·mol-1 |
C.KOH(aq)+ H2SO4(aq)= H2SO4(aq)= K2SO4(aq)+H2O(l) △H=-57.3 kJ·mol-1 K2SO4(aq)+H2O(l) △H=-57.3 kJ·mol-1 |
| D.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l) △H=-114.6 kJ·mol-1 |
二、未知 添加题型下试题
A.C(s)+ O2(g)=CO(g) △H=-393.5kJ/mol O2(g)=CO(g) △H=-393.5kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l) △H=+571.6kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ/mol |
D. C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) △H=-1400 kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) △H=-1400 kJ/mol |
三、单选题 添加题型下试题
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=+131.3 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ/mol
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ/mol
下列有关说法正确的是( )
| A.水煤气只能用作燃料 |
| B.水煤气是一种二次能源,比煤直接燃烧污染小 |
| C.等质量的CO和H2完全燃烧时,前者放热多 |
| D.由反应③可以确定H2的燃烧热为241.8 kJ/mol |
【知识点】 燃烧热

| A.化学能 | B.生物质能 | C.热能 | D.电能 |
【知识点】 能量的相互转化
| A.2912 kJ | B.2953 kJ | C.3236 kJ | D.3867 kJ |
【知识点】 化学反应热的计算
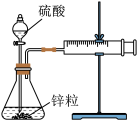
| A.用锌粒来表示10 s内该反应的速率为0.013 g/s |
| B.忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol/(L·s) |
| C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应的速率为0.01 mol/(L·s) |
| D.用H2来表示10 s内该反应的速率为0.000 2 mol/s |
 2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1;④v(D)=0.45 mol·L-1·s-1该反应进行的快慢顺序为( )
2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1;④v(D)=0.45 mol·L-1·s-1该反应进行的快慢顺序为( )| A.④>②=③>① | B.④>②>③>① |
| C.①>②=③>④ | D.①>②>③>④ |
【知识点】 化学反应速率与化学计量数之间的关系解读
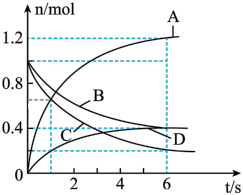
| A.该反应的化学方程式为3B+4D⇌6A+2C |
| B.反应进行到1 s时,v(A)=v(C) |
| C.反应从开始到6 s的时间内,B的平均反应速率为0.05 mol·L-1·s-1 |
| D.反应进行到6 s时,各物质的反应速率相等 |
| A.用HCl和CaCl2表示的反应速率数值不同,但所表示的意义相同 |
| B.不能用CaCO3的浓度变化来表示反应速率,但可用水来表示 |
| C.用H2O和CO2表示的化学反应速率相同 |
| D.用CaCl2浓度的减小表示其反应速率 |
【知识点】 化学反应速率的定量表示方法解读
四、未知 添加题型下试题
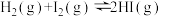
 ,下列说法正确的是
,下列说法正确的是A.保持容器容积不变,向其中加入 ,反应速率一定加快 ,反应速率一定加快 |
B.保持容器容积不变,向其中加入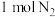 ( ( 不参加反应),反应速率一定加快 不参加反应),反应速率一定加快 |
C.保持容器内气体压强不变,向其中加入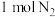 ( ( 不参加反应),反应速率一定加快 不参加反应),反应速率一定加快 |
D.保持容器内气体压强不变,向其中加入 和 和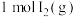 ,反应速率一定加快 ,反应速率一定加快 |
五、单选题 添加题型下试题
甲:在500℃时,SO2和O2各10mol反应
乙:在500℃时,用V2O5作催化剂,10molSO2和5molO2反应
丙:在450℃时,8molSO2和5molO2反应
丁:在500℃时,8molSO2和5molO2反应
| A.甲、乙、丙、丁 |
| B.乙、甲、丁、丙 |
| C.乙、甲、丙、丁 |
| D.丁、丙、乙、甲 |
A.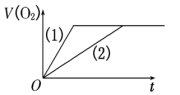 | B. | C.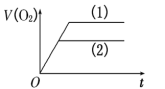 | D. |
【知识点】 催化剂对化学反应速率的影响解读
六、未知 添加题型下试题
 CaCl2+H2O+CO2↑,下列措施中可使生成CO2的速率加快的是(不考虑CaCO3与盐酸接触面积改变的影响)( )
CaCl2+H2O+CO2↑,下列措施中可使生成CO2的速率加快的是(不考虑CaCO3与盐酸接触面积改变的影响)( )| A.加大CaCO3的量 | B.加大盐酸的量 |
| C.加大盐酸的浓度 | D.减小CaCl2的浓度 |
【知识点】 影响化学反应速率的外因 浓度对化学反应速率的影响解读
七、单选题 添加题型下试题
 2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )
2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )| A.等于5s | B.等于10s | C.小于10s | D.大于10s |
 SO3(g)+NO(g) ΔH=-41.8kJ·mol-1。将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
SO3(g)+NO(g) ΔH=-41.8kJ·mol-1。将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是| A.体系压强保持不变 | B.混合气体颜色保持不变 |
| C.SO3和NO的体积比保持不变 | D.每消耗1molSO3的同时生成1molNO2 |
【知识点】 化学平衡状态的判断方法解读
 2NH3(g)已达到平衡状态的是( )
2NH3(g)已达到平衡状态的是( )| A.1个N≡N键断裂的同时,有3个H—H键断裂 |
| B.1个N≡N键断裂的同时,有3个H—H键形成 |
| C.3个H—H键断裂的同时,有6个N—H键形成 |
| D.1个N≡N键断裂的同时,有6个N—H键形成 |
【知识点】 化学平衡状态 化学平衡状态本质及特征解读 化学平衡状态的判断方法解读
 xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是
xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是| A.x=1 |
| B.B的转化率为50% |
| C.2min内A的反应速率为0.3mol·L-1·min-1 |
| D.若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态 |
 2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )
2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )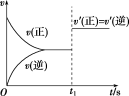
| A.t1时刻,增大了X的浓度 |
| B.t1时刻,升高了体系温度 |
| C.t1时刻,缩小了容器体积 |
| D.t1时刻,使用了催化剂 |
【知识点】 外界条件对化学平衡影响的图像解读
 N2(g)+2CO2(g)ΔH=-746.4kJ•mol-1。平衡后,为提高该反应的速率和NO的转化率,采取措施最合理的是
N2(g)+2CO2(g)ΔH=-746.4kJ•mol-1。平衡后,为提高该反应的速率和NO的转化率,采取措施最合理的是| A.加催化剂同时升高温度 |
| B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 |
| D.降低温度同时增大压强 |
【知识点】 化学平衡的移动及其影响因素 温度对化学平衡移动的影响解读
| A.熔融MgCl2、熔融NaOH | B.液氨、石灰水 |
| C.石墨、食醋 | D.稀硫酸、蔗糖 |
【知识点】 物质水溶液的导电性解读 强电解质和弱电解质的判断
| A.碳酸钙难溶于水,放入水中溶液不导电,且碳酸钙在960 ℃时分解,不存在熔融状态导电的性质,故CaCO3是非电解质 |
| B.NH3溶于水后得到的水溶液能导电,所以NH3是电解质 |
| C.BaSO4难溶于水,但溶于水的那一部分能够完全电离,故BaSO4是强电解质 |
| D.NaCl是电解质,所以NaCl固体能导电 |
【知识点】 电解质、非电解质概念解读 强电解质与弱电解质解读
八、填空题 添加题型下试题
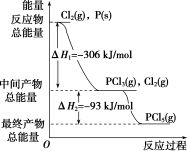
根据如图回答下列问题:
(1)P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式是
(2)PCl5(g)分解成PCl3(g)和Cl2(g)的热化学方程式是
(3)P(s)和Cl2(g)分两步反应生成1 mol PCl5(g)的ΔH3=
(4)已知1mol白磷变成1mol红磷放出18.39KJ的热量和下列两个热化学方程式:
4P(白磷,s)+5O2(g)=2P2O5(s) ΔH1,
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2。
则ΔH1和ΔH2的关系正确的是
A.ΔH1=ΔH2 B.ΔH1>ΔH2 C.ΔH1<ΔH2 D.无法确定
九、解答题 添加题型下试题
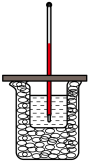
中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃用品是
(2)实验中改用60 mL 0.50 mol/L盐酸与60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
(3)实验中改用6.94 mL 15 mol/L硫酸溶液跟60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所求中和热
(4)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①3.3 ℃、②3.5 ℃、③4.5 ℃,则最终代入计算式的温差平均值为
(5)请利用上(4)小题的结论,计算该实验测得的中和反应反应热ΔH=
(6)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和反应反应热为ΔH1,则ΔH1与原题中ΔH的关系为ΔH1
【知识点】 中和热的测定与误差分析解读 中和热的计算解读
十、填空题 添加题型下试题
 2NH3(g) ΔH=-92.2 kJ·mol-1。
2NH3(g) ΔH=-92.2 kJ·mol-1。(1)一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,正、逆反应速率与时间的关系如图所示,其中t4、t5、t7时刻所对应改变的实验条件分别是t2

(2)在一定条件下,将2 mol N2与5 mol H2混合于一个10 L的密闭容器中,反应情况如图所示:

①5 min内的平均反应速率v(NH3)=
②达到平衡时NH3的百分含量为
(1)H2SO4:
(2)Fe(OH)3:
(3)NH3·H2O:
(4)Na2CO3:
(5)KHCO3:
(6)Al(OH)3的酸式电离:
【知识点】 电离方程式解读 弱电解质的电离方程式解读
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 中和热 中和热概念 | |
| 3 | 0.65 | 燃烧热 | |
| 4 | 0.65 | 能量的相互转化 | |
| 5 | 0.85 | 化学反应热的计算 | |
| 6 | 0.65 | 化学反应的速率 化学反应速率的定量表示方法 化学反应速率计算 测定某些反应的反应速率 | |
| 7 | 0.65 | 化学反应速率与化学计量数之间的关系 | |
| 8 | 0.65 | 化学反应的速率 化学反应速率计算 化学反应速率与化学计量数之间的关系 化学平衡图像分析 | |
| 9 | 0.85 | 化学反应速率的定量表示方法 | |
| 12 | 0.65 | 化学反应速率计算 外因对化学反应速率影响的综合分析 化学反应速率与化学平衡的综合应用 | |
| 13 | 0.85 | 催化剂对化学反应速率的影响 | |
| 15 | 0.85 | 化学反应速率计算 | |
| 16 | 0.85 | 化学平衡状态的判断方法 | |
| 17 | 0.85 | 化学平衡状态 化学平衡状态本质及特征 化学平衡状态的判断方法 | |
| 18 | 0.4 | 化学反应速率计算 化学平衡状态的判断方法 转化率的相关计算及判断 | |
| 19 | 0.65 | 外界条件对化学平衡影响的图像 | |
| 20 | 0.65 | 化学平衡的移动及其影响因素 温度对化学平衡移动的影响 | |
| 21 | 0.65 | 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 22 | 0.65 | 电解质、非电解质概念 强电解质与弱电解质 | |
| 二、未知 | |||
| 2 | 0.65 | 热化学方程式 燃烧热 | 未知 |
| 10 | 0.94 | 化学反应的速率 | 未知 |
| 11 | 0.85 | 影响化学反应速率的因素 浓度对化学反应速率的影响 压强对化学反应速率的影响 | 未知 |
| 14 | 0.85 | 影响化学反应速率的外因 浓度对化学反应速率的影响 | 未知 |
| 三、填空题 | |||
| 23 | 0.65 | 焓变 盖斯定律与热化学方程式 根据△H=生成物的总能量之和-反应物的总能量之和进行计算 | |
| 25 | 0.65 | 化学反应速率计算 化学平衡的有关计算 化学平衡图像分析 化学反应速率与化学平衡的综合应用 | |
| 26 | 0.65 | 电离方程式 弱电解质的电离方程式 | |
| 四、解答题 | |||
| 24 | 0.65 | 中和热的测定与误差分析 中和热的计算 | 实验探究题 |



