2016-2017学年辽宁省重点高中协作校高二上学期期中化学卷
辽宁
高二
期中
2017-07-27
418次
整体难度:
较易
考查范围:
认识化学科学、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.铜、石墨均能导电,所以它们均是电解质 |
| B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 |
| C.液态HCl、固体NaCl均不能导电,所以HCl、NaCl均是非电解质 |
| D.蔗糖、酒精在水溶液或熔融状态下均不能导电,所以它们均是非电解质 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.发生中和反应时所需NaOH的量前者大于后者 |
| B.溶液pH前者小于后者 |
| C.已电离出的H+的物质的量前者大于后者 |
| D.所含CH3COOH的物质的量前者大于后者 |
【知识点】 水的电离及溶液的酸碱性
A.1:10:10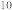 :10 :10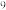 | B.1:5:5 10 10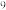 :5 :5 108 108 |
C.1:20:10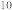 :10 :10 | D.1:10:10 :10 :10 |
| A.用干燥的pH试纸测定新制氯水的pH |
| B.若25.00 mL滴定管中液面的位置在刻度为3.00mL处,则滴定管中液体的体积一定大于22.00mL |
| C.中和滴定实验中,洗净后的锥形瓶一定要用待测液润洗2-3次 |
| D.用玻璃棒蘸取溶液滴在表面皿上的已润湿pH试纸上测其pH,一定有误差 |
【知识点】 测定溶液pH的方法解读 酸碱中和滴定实验基本操作及步骤解读

| A.水电离出的氢离子浓度:a > b |
| B.盐酸的物质的量浓度为0.0100 mol·L-1 |
| C.当指示剂由红色变为无色时,达滴定终点 |
| D.当滴加NaOH溶液10.00 mL时,该混合液的pH= l+lg3 |
【知识点】 水的电离及溶液的酸碱性
| A.新制氯水中加入固体NaOH:c(Na+) = c(Cl-) + c(ClO-) + c(OH‑) |
| B.pH = 8.3的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-) > c(H2CO3) |
| C.pH = 11的氨水与pH = 3的盐酸等体积混合:c(Cl-) = c(NH4+) > c(OH‑) = c(H+) |
| D.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+) – 2c(OH-) = c(CH3COO-) – c(CH3COOH) |
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
| A.①②③ | B.②③④ | C.①④⑤ | D.①②③④⑤ |
【知识点】 盐类水解的应用
1.①②③显酸性,④显碱性
2.c(NH4+):④<①<③<②
3.溶液的pH:①<②<④
4.②溶液中:c (NH4+) +c (H+)="c" (SO42-)+c (OH-)
| A.1项 | B.2项 | C.3项 | D.4项 |
【知识点】 盐类的水解
二、未知 添加题型下试题
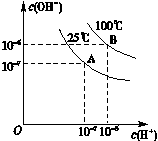
| A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液等体积混合时恰好中和,所得溶液的pH等于7 |
| B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl溶液等体积混合,所得溶液的pH等于7 |
| C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L醋酸等体积混合后恰好中和,所得溶液pH等于7 |
| D.25 ℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7 |
【知识点】 水的电离及溶液的酸碱性
三、单选题 添加题型下试题
 )在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是
)在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是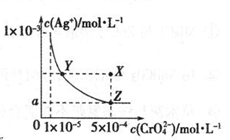
A.向饱和 溶液中加入固体K2CrO4能使溶液由Y点变为X点 溶液中加入固体K2CrO4能使溶液由Y点变为X点 |
| B.T℃时,在Y点和Z点,Ag2CrO4的Ksp相等 |
C.T℃时, 的 Ksp数值为 1×10-11 的 Ksp数值为 1×10-11 |
D.图中 |
【知识点】 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积规则及其应用解读
| A.10mL 0.lmol/L 氨水与 l0mL 0.lmol/L 盐酸混合 c(Cl-) > c(NH4+) > c(OH-) > c(H+) |
| B.10mL 0.lmol/L NH4Cl溶液与 5mL 0.2 mol/L NaOH溶液混合c(NH4+) >c(Cl-)>c(OH-) >c(H+) |
| C.l0mL 0.lmol/LCH3COOH溶液与5mL 0.2mol/L NaOH 溶液混合, c(Na+) = c(CH3COO-) > c(OH-) = c(H+) |
| D.10mL 0.5mol/L CH3COONa 溶液与5mL lmol/L 盐酸混合c(Cl-) = c(Na+) > c(H+) > c(OH-) |
【知识点】 盐类的水解

| A.0.5% | B.1.5% | C.0.1% | D.1% |
【知识点】 弱电解质的电离平衡
A.HB-水解方程式:HB-+H2O H3O++ B2- H3O++ B2- |
| B.溶液中离子浓度大小为:c(Na+) > c(HB-)> c(B2-) > c(OH-) > c(H+) |
| C.NaHB的存在促进了水的电离 |
| D.相同物质的量浓度溶液的pH值:NaHB > Na2B |
【知识点】 盐类的水解
| A.4—甲基一3—乙基戊烷 | B.2,2—二氯乙烷 |
| C.2,2—二甲基一1—丁烯 | D.3,3—二甲基一1一丁烯 |
【知识点】 有机物的命名
| A.分子式均满足CnH2n+2的两种烃不一定是同系物 |
| B.可单独用溴水或酸性KMnO4溶液除去乙烷中的乙烯 |
| C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同 |
| D.乙烯使溴水和酸性KMnO4溶液褪色的原理相同 |
| A.1—丁烯 | B.1—丁炔 | C.2—丁炔 | D.2—丁烯 |
【知识点】 简单有机物同分异构体书写及辨识解读 炔烃的加成解读
 则其单体的名称为
则其单体的名称为| A.2,4—二甲基—2—己烯 | B.2,4—二甲基-1,3-己二烯 |
| C.乙烯和2-甲基-1,3-戊二烯 | D.乙烯和2-甲基-1,3-丁二烯 |
【知识点】 加聚物的单体、链节及聚合度的确定解读
四、填空题 添加题型下试题
(1)NH4NO3的水溶液呈
(2)某温度下纯水中的C(H+ )= 2×10-7mol/L,则此时溶液中的C(OH-)=
【知识点】 水的电离及溶液的酸碱性

(1)①反应类型
②反应类型
(2)现有如下有机物:
①CH3—CH3②CH2=CH2 ③CH3CH2C
 CH
CH④CH3C
 CCH3⑤C2H6⑥CH3CH=CH2
CCH3⑤C2H6⑥CH3CH=CH2一定互为同系物的是
(3)人造羊毛的主要成分是聚丙烯腈(丙烯腈:CH2=CH—CN),试写出以乙炔、HCN为原料,两步反应合成聚丙烯腈的化学方程式。
①
②
【知识点】 合成有机高分子的基本方法
五、解答题 添加题型下试题
(1)配制待测液:称取6.0 g固体烧碱样品(杂质不与酸反应)配制成250 mL溶液。
(2)滴定:
①用
②向锥形瓶中加入几滴甲基橙,用0.2010 mol •L-1的标准硫酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,滴定终点时的现象为
(3)数据处理
| 实验次序编号 | 硫酸溶液体积V/mL | 氢氧化钠溶液体积V/mL |
| 1 | 19.90 | 15.00 |
| 2 | 20.10 | 15.00 |
| 3 | 22.00 | 15.00 |
| 4 | 20.00 | 15.00 |
(4)—定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制盐酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是
A.实验中所用到的滴定管、容量瓶,在使用前均需要验漏
B.如果实验中需用80 mL的稀盐酸标准溶液,配制时应选用100mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀盐酸,则测得的NaOH溶液的浓度将偏小
E.配制标准溶液时,定容时俯视读数,则导致滴定时测得的NaOH溶液的浓度偏大
F.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏小
G.锥形瓶用蒸馏水洗净后,有少量蒸馏水残留,则导致实验结果偏小
H.滴定前滴定管尖嘴有气泡,滴定后气泡消失,则导致实验结果偏大
I.在滴定过程中,不慎将数滴酸液滴在锥形瓶外,则导致实验结果偏大

其中第①步存在平衡:2 CrO42-(黄色)+2H+
 Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO4•7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s)
 Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。
【知识点】 沉淀溶解平衡
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 2 | 0.85 | 盐类的水解 | |
| 3 | 0.94 | 水的电离及溶液的酸碱性 | |
| 4 | 0.65 | 水的离子积常数 影响水电离的因素 水溶液中水的电离程度及的计算 盐类水解规律 | |
| 5 | 0.94 | 测定溶液pH的方法 酸碱中和滴定实验基本操作及步骤 | |
| 6 | 0.94 | 水的电离及溶液的酸碱性 | |
| 7 | 0.85 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 8 | 0.85 | 盐类水解的应用 | |
| 9 | 0.64 | 盐类的水解 | |
| 11 | 0.65 | 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积规则及其应用 | |
| 12 | 0.94 | 盐类的水解 | |
| 13 | 0.85 | 弱电解质的电离平衡 | |
| 14 | 0.94 | 盐类的水解 | |
| 15 | 0.65 | 甲烷的取代反应 烷烃的取代反应 | |
| 16 | 0.94 | 有机物的命名 | |
| 17 | 0.65 | 炔烃的加成 | |
| 18 | 0.64 | 烃 有机物的分类 | |
| 19 | 0.94 | 简单有机物同分异构体书写及辨识 炔烃的加成 | |
| 20 | 0.85 | 加聚物的单体、链节及聚合度的确定 | |
| 二、未知 | |||
| 10 | 0.4 | 水的电离及溶液的酸碱性 | 未知 |
| 三、填空题 | |||
| 21 | 0.94 | 水的电离及溶液的酸碱性 | |
| 22 | 0.94 | 合成有机高分子的基本方法 | |
| 四、解答题 | |||
| 23 | 0.85 | 酸碱中和滴定实验基本操作及步骤 酸碱中和滴定的误差分析 | 实验探究题 |
| 24 | 0.85 | 沉淀溶解平衡 | 实验探究题 |

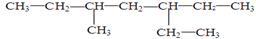 则该炔烃可能具有的结构有
则该炔烃可能具有的结构有

