湖南省武冈市第二中学2018-2019学年高一上学期期中考试化学试题
湖南
高一
期中
2018-11-30
378次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、化学反应原理、常见无机物及其应用
一、单选题 添加题型下试题
| A.被玻璃割伤手,先取出伤口里的碎玻璃片,再用过氧化氢溶液擦洗,然后敷药包扎 |
| B.实验桌上因酒精灯打翻而着火时应立即用水扑灭 |
| C.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上3%的稀盐酸 |
| D.浓酸对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多水冲洗,再涂上稀硼酸溶液 |
【知识点】 仪器使用与实验安全
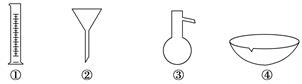
| A.过滤 | B.蒸馏 | C.蒸发 | D.分液 |
【知识点】 物质分离、提纯的常见物理方法
| A.在常温、常压下,11.2L N2含有的分子数为0.5NA |
| B.将80 g NaOH溶于1L水中,所得溶液的物质的量浓度为2mol/L |
| C.标准状况下,18g H2O的体积是22.4L |
| D.标准状况下,20mL NH3与60mL O2所含分子个数比为1:3 |
| A.1mol OH-含有的电子数为9NA |
| B.含0.01 mol FeCl3的饱和溶液滴入沸腾的水中,制得的氢氧化铁胶体粒子数为0.01NA |
| C.常温常压下,NO2和N2O4的混合物23g中含有NA个氧原子 |
| D.标准状况下,22.4 L乙醇(酒精)中含有NA个乙醇分子 |
| A.将5.85gNaCl 固体溶于IL水中可配成0.1mol/L的NaCl 溶液 |
| B.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果 |
| C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线 |
| D.称量时,将固体NaCl 直接放在天平左盘上 |
| A.氢氧化镁和稀盐酸反应 | B.Ba(OH)2溶液滴入稀硫酸中 |
| C.澄清石灰水和稀硝酸反应 | D.氢氧化钠和稀醋酸反应 |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.46 | B.28 | C.44 | D.64 |
| A.转移溶液后未洗涤烧杯和玻璃棒就直接定容 |
| B.在容量瓶中进行定容时俯视刻度线 |
| C.带游码的天平称24gNaOH时误用了“左码右物”方法 |
| D.所用NaOH已经潮解 |
| A.稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| B.氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-=BaSO4↓ |
| C.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| D.NaHSO4溶液中加入Ba(OH)2溶液后恰好显中性Ba2++2OH-+2H++ SO42-=BaSO4↓+2H2O |
【知识点】 离子反应的发生及书写
| A.KMnO4→O2 | B.CO2→CO | C.Br-→Br2 | D.Fe2O3→Fe |
【知识点】 氧化还原反应基本概念 常见氧化剂与还原剂解读 氧化还原反应的应用
| A.氧化剂 | B.还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.Fe3+>Cu2+>Fe2+ | B.Cu2+>Fe3+>Fe2+ | C.Fe3+>Fe2+>Cu2+ | D.Fe2+>Cu2+>Fe3+ |
【知识点】 氧化性、还原性强弱的比较解读
| A.强碱性溶液中:K+、Al3+、Cl-、SO42— |
| B.在无色透明的溶液中:K+、Cu2+、NO3—、SO42— |
| C.含有0.1 mol·L−1 Ca2+的溶液中:Na+、K+、CO32—、Cl- |
| D.室温下,pH=1的溶液中:Na+、Fe3+、NO3—、SO42— |
【知识点】 离子反应的发生及书写
| A.1:1 | B.3:8 | C.2:3 | D.8:3 |
【知识点】 氧化还原反应有关计算 与氧化剂、还原剂有关的计算解读
| A.0.1mol | B.0.3mol |
| C.0.5 mol | D.0.15mol |
【知识点】 物质的量有关计算
二、填空题 添加题型下试题
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O、Br2。
①已知KBrO3在反应中得到电子,则该反应的氧化产物是
②0.2 mol KBrO3在反应中得到
(3)在2Na + Cl2 == 2NaCl的反应中,当有2.3 g Na发生反应时,转移了

(1)两种物质混合能发生反应且都是电解质的是
(2)分类标准代号A表示
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:
(4)用洁净的烧杯取25 mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热得红褐色胶体,该反应的化学方程式为:
三、解答题 添加题型下试题
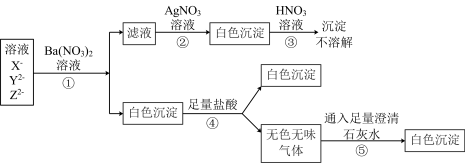
(1)判断X-、Y2-、Z2-分别为
(2)写出④、⑤步反应的离子方程式。
④
⑤
【知识点】 离子反应的发生及书写 无机综合推断 常见无机物的制备解读 离子的检验
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为
(2)配制该硫酸溶液应选用容量瓶的规格为
(3)配制时,该同学的操作顺序如下,请将操作步骤 B、D 补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L 的浓硫酸150mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果步骤C中的硫酸溶液未冷却就转移到容量瓶并定容,对所配溶液浓度有何影响?
试卷分析
试卷题型(共 23题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 仪器使用与实验安全 | |
| 2 | 0.85 | 化学实验基础 仪器使用与实验安全 | |
| 3 | 0.85 | 分散系概念及其分类 胶体的定义及分类 | |
| 4 | 0.85 | 物质分离、提纯的常见物理方法 | |
| 5 | 0.85 | 胶体 分散系概念及其分类 胶体的定义及分类 | |
| 6 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合气体物质与NA相关推算 | |
| 7 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 8 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度溶液的综合考查 | |
| 9 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 10 | 0.65 | 气体摩尔体积 阿伏加德罗定律的应用 物质的量有关计算 根据n=m/M进行相关计算 | |
| 11 | 0.65 | 仪器使用与实验安全 配制一定物质的量浓度的溶液实验的误差分析 | |
| 12 | 0.4 | 离子反应的发生及书写 | |
| 13 | 0.65 | 氧化还原反应基本概念 常见氧化剂与还原剂 氧化还原反应的应用 | |
| 14 | 0.85 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 15 | 0.65 | 氧化性、还原性强弱的比较 | |
| 16 | 0.94 | 离子反应的发生及书写 | |
| 17 | 0.65 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 18 | 0.94 | 物质的量有关计算 | |
| 二、填空题 | |||
| 19 | 0.65 | 电解质与非电解质 非电解质、电解质物质类别判断 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 20 | 0.65 | 摩尔质量 摩尔质量与相对原子质量区别与联系 氧化还原反应的应用 氧化还原反应的规律 | |
| 21 | 0.65 | 无机物质的分类 胶体的制备 电解质与非电解质 离子方程式的书写 | |
| 三、解答题 | |||
| 22 | 0.65 | 离子反应的发生及书写 无机综合推断 常见无机物的制备 离子的检验 | 无机推断题 |
| 23 | 0.65 | 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |