云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题
云南
高三
开学考试
2019-09-27
222次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、化学与STSE、物质结构与性质、有机化学基础、化学实验基础
云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题
云南
高三
开学考试
2019-09-27
222次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、化学与STSE、物质结构与性质、有机化学基础、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列有关说法不正确的是( )
| A.a=4 | B.Y的化学式为Fe2O3 |
| C.S2O32-是还原剂 | D.每32gO2参加反应,转移电子的物质的量为4mol |
【知识点】 氧化还原反应的规律解读 与氧化剂、还原剂有关的计算解读
您最近一年使用:0次
2016-09-01更新
|
256次组卷
|
6卷引用:2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷
单选题
|
较易(0.85)
2. 下列说法正确的是
| A.强氧化剂与强还原剂不一定能发生氧化还原反应 |
| B.含最高价元素的化合物一定只表现强氧化性 |
| C.阳离子只有氧化性,阴离子只有还原性 |
| D.发生化学反应时,失电子越多的金属原子,还原能力越强 |
您最近一年使用:0次
单选题
|
适中(0.65)
3. 下列说法错误的是
| A.电解饱和食盐水可制取烧碱、氯气、氢气 |
| B.从海水中可提取镁、溴、碘等物质 |
| C.粗铜(含少量Zn、Fe、Pt等)电解精炼后,溶液中金属阳离子只有Fe2+、Zn2+ |
| D.在镀件上镀铜,镀件作阴极 |
您最近一年使用:0次
2016-12-09更新
|
252次组卷
|
4卷引用:2015届福建省宁德市高三上学期期末化学试卷
单选题
|
容易(0.94)
真题
名校
4. “保护环境”是我国的基本国策。下列做法不应该提倡的是
| A.采取低碳、节俭的生活方式 | B.按照规定对生活废弃物进行分类放置 |
| C.深入农村和社区宣传环保知识 | D.经常使用一次性筷子、纸杯、塑料袋等 |
您最近一年使用:0次
2019-01-30更新
|
1351次组卷
|
15卷引用:2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)
2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)2016届山东省枣庄市第二中学高三9月阶段性学情检测化学试题2016届江苏省东海县石榴高级中学高三上学期第一次月考化学试卷2015-2016学年江苏省扬州市高二下学期模拟考试必修(一)化学试卷江苏省启东中学2017-2018学年高一(创新班)上学期期初考试化学试题【校级联考】江苏省七校联盟2018-2019学年高二上学期期中联考化学试题云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题河南省鹤壁市高级中学2019-2020学年高一11月月考化学试题贵州省六盘水市第七中学2019-2020学年高一上学期第一次月考化学试题(已下线)专题一 化学与STSE(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训吉林省长春市东北师大附中2020届高中毕业班四月份教学质量监测卷理科综合化学部分江苏省连云港市智贤中学2021届高三9月月考化学试题江苏省棋盘中学2021届高三下学期新高考第二次模拟化学试题宁夏固原市隆德县中学教育集团2022-2023学年高三上学期期中考试化学试题陕西省西安市周至县第四中学2022-2023学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
5. 对下列物质溶于水时破坏的作用力描述错误的是
| A.氯化钠,破坏了离子键 | B.氯化氢,破坏了共价键 |
| C.蔗糖,破坏了分子间作用力 | D.二氧化碳,没有破坏作用力 |
您最近一年使用:0次
2019-09-26更新
|
465次组卷
|
8卷引用:云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题
云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题贵州省黎平第二中学2019-2020学年高三上学期期末考试化学试题贵州省罗甸县第一中学2019-2020学年高三上学期期末考试理综化学试题上海市杨浦区2015届高三上学期学业质量调研化学试题鲁科版2019选择性必修2阶段性综合评估测试卷(一)(已下线)课时27 微粒间作用力-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第11练 化学键-2023年高考化学一轮复习小题多维练(全国通用)
单选题
|
适中(0.65)
名校
7. 下列各组物质,具有相同的最简式,但既不属于同分异构体又不属于同系物的是
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯
| A.①②⑤ | B.①②③ | C.①④⑤ | D.①②③⑤ |
【知识点】 同系物的判断解读 同分异构现象、同分异构体的概念解读
您最近一年使用:0次
2019-09-26更新
|
307次组卷
|
2卷引用:云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
8. 欲降低废水中重金属元素铬的毒性,可将Cr2O 转化为Cr(OH)3沉淀除去。已知该条件下:
转化为Cr(OH)3沉淀除去。已知该条件下:
(1)某含铬废水处理的主要流程如图所示:
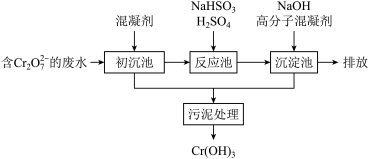
①初沉池中加入的混凝剂是K2SO4·Al2(SO4)3·2H2O,其作用为(用离子方程式表示)____ 。
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+===2Cr3++3SO42-+4H2O。根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是_____ 、____ 。证明Cr3+沉淀完全的方法是____ 。
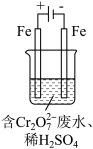
(2)工业可用电解法来处理含Cr2O 废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是_____ ,得到的金属阳离子在阴极区可沉淀完全。用电解法处理该溶液中0.01molCr2O72-时,至少得到沉淀的质量是____ g。
 转化为Cr(OH)3沉淀除去。已知该条件下:
转化为Cr(OH)3沉淀除去。已知该条件下:| 离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cr3+ | 6.0 | 8.0 |
(1)某含铬废水处理的主要流程如图所示:

①初沉池中加入的混凝剂是K2SO4·Al2(SO4)3·2H2O,其作用为(用离子方程式表示)
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+===2Cr3++3SO42-+4H2O。根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是
(2)工业可用电解法来处理含Cr2O
 废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是
您最近一年使用:0次
2019-09-19更新
|
205次组卷
|
4卷引用:云南省陇川县一中2020届高三上学期开学考试化学试题
解答题-工业流程题
|
适中(0.65)
名校
9. 活性ZnO在橡胶、塑料、涂料工业有重要应用,工业上用含锌物料(含FeO、CuO等杂质)制取活性ZnO的流程如图所示:

(1)上述流程中,浸出时用的是60% H2SO4(密度是1.5 g/cm3),则该H2SO4的物质的量浓度为______________ (保留两位小数) 。
(2)上述流程H2SO4浸出后溶液中Fe3+的浓度为0.04 mol·L-1,控制滤液的pH,加入H2O2后产生大量红褐色沉淀。
①粗略测定溶液pH的实验操作是___________________________________________ 。
②已知:常温下Fe(OH)3的Ksp=4.0×10-38。滤液的pH至少为________ 时,溶液中Fe3+开始沉淀。
(3)A溶液中主要含有的溶质是______________ ,验证溶质所含阳离子的方法是_____________ 。
(4)制备ZnO所焙烧的物质是含结晶水的碱式碳酸锌。取碱式碳酸锌6.82g,溶于HCl生成CO2 448 mL(标准状况下),溶解过程消耗HCl 0.12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式_________________ 。

(1)上述流程中,浸出时用的是60% H2SO4(密度是1.5 g/cm3),则该H2SO4的物质的量浓度为
(2)上述流程H2SO4浸出后溶液中Fe3+的浓度为0.04 mol·L-1,控制滤液的pH,加入H2O2后产生大量红褐色沉淀。
①粗略测定溶液pH的实验操作是
②已知:常温下Fe(OH)3的Ksp=4.0×10-38。滤液的pH至少为
(3)A溶液中主要含有的溶质是
(4)制备ZnO所焙烧的物质是含结晶水的碱式碳酸锌。取碱式碳酸锌6.82g,溶于HCl生成CO2 448 mL(标准状况下),溶解过程消耗HCl 0.12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式
您最近一年使用:0次
2019-09-26更新
|
254次组卷
|
5卷引用:云南省凤庆县一中2020届高三上学期开学考试理综化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
10. 按下图装置进行实验,并回答下列问题:
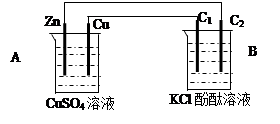
(1)判断装置的名称:A池为___________ ;B池为______________ ;
(2)锌极为________ 极,电极反应式为___________________________________ ;铜极为________ 极,电极反应式为___________________________________ ;石墨棒C1为______ 极,电极反应式为__________________________________ ;石墨棒C2附近发生的实验现象为______________________________________ ;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________ (变大、不变或变小)了________ g,CuSO4溶液的质量_________ (增加、不变或减少)_________ g。
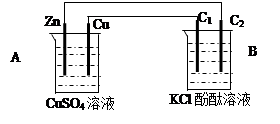
(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化
您最近一年使用:0次
2014-07-16更新
|
782次组卷
|
11卷引用:2010年江苏省江都中学高一第二学期期末考试化学试题
(已下线)2010年江苏省江都中学高一第二学期期末考试化学试题(已下线)2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷2015-2016学年河北省容城中学高二上学期第一次月考化学试卷云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题(已下线)考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》贵州省惠水县第一高级中学2019-2020学年高三上学期期末考试化学试题宁夏回族自治区中卫市中宁县中宁中学2019-2020学年高二下学期阶段测试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解福建省仙游县郊尾中学2020届高三上学期期中考试化学试题
四、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
解题方法
11. [化学—选修5:有机化学基础]
高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:Ⅰ.RCOOR′+ R′′18OH RCO18O R′′+ R′OH(R、R′、R′′代表烃基);
RCO18O R′′+ R′OH(R、R′、R′′代表烃基);
Ⅱ. (R、R′代表烃基);
(R、R′代表烃基);
(1)①的反应类型是________ 。
(2)②的化学方程式为________ 。
(3)PMMA单体的官能团名称是________ 、________ 。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________ 。
(5)G的结构简式为________ 。
(6)下列说法正确的是________ (填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d.1 mol 与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是________ 。
(8)写出由PET单体制备PET聚酯(化学式为C10nH8nO4n 或C10n+2H8n+6O4n+2)并生成B的化学方程式________________________________________________ 。
高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:Ⅰ.RCOOR′+ R′′18OH
 RCO18O R′′+ R′OH(R、R′、R′′代表烃基);
RCO18O R′′+ R′OH(R、R′、R′′代表烃基);Ⅱ.
 (R、R′代表烃基);
(R、R′代表烃基);(1)①的反应类型是
(2)②的化学方程式为
(3)PMMA单体的官能团名称是
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为
(5)G的结构简式为
(6)下列说法正确的是
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d.1 mol
 与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是
(8)写出由PET单体制备PET聚酯(化学式为C10nH8nO4n 或C10n+2H8n+6O4n+2)并生成B的化学方程式
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
12. 下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:

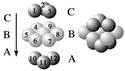
图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________ ,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为__________________________________ 。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________ ,H3BO3晶体中B原子个数与极性键个数比为____________ 。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________ 理论。
(4)三种晶体中熔点最低的是________ (填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为____________________________________________________________ 。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为_______________________________________ 。


图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用
(4)三种晶体中熔点最低的是
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为
您最近一年使用:0次
2018-09-26更新
|
449次组卷
|
16卷引用:云南省玉溪市通海县第二中学2019届高三9月月考化学试题
云南省玉溪市通海县第二中学2019届高三9月月考化学试题云南省西畴县第二中学2020届高三上学期开学考试化学试题云南省文山壮族苗族自治州砚山县第二中学2020届高三上学期开学考试化学试题云南省文山州马关县实验高中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省宾川县三中2020届高三上学期开学考试化学试题云南省盈江县一中2020届高三上学期开学考试化学试题云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题云南省马关县第二中学2019-2020学年高三上学期期末考试理综化学试题贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题贵州省黔南布依族苗族自治州贵定县第二中学2019-2020学年高三上学期期末考试化学试题云南省玉溪市新平县一中2019-2020学年高三上学期1月月考理综化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题云南省景东彝族自治县第一中学2021-2022学年高三下学期3月份考试化学试题云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题云南省广南县第一中学2021-2022学年高三下学期3月考试理综化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、化学反应原理、化学与STSE、物质结构与性质、有机化学基础、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
3
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 2 | 0.85 | 氧化还原反应基本概念 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 3 | 0.65 | 电解原理的应用 氯碱工业 电镀 铜的电解精炼 | |
| 4 | 0.94 | 固体废弃物的处理 “白色污染”危害及防治 能源的充分利用 绿色化学与可持续发展 | |
| 5 | 0.65 | 化学键与物质类别关系的判断 分子间作用力 化学键与分子间作用力 | |
| 6 | 0.85 | 金属的电化学腐蚀与防护 | |
| 7 | 0.65 | 同系物的判断 同分异构现象、同分异构体的概念 | |
| 二、解答题 | |||
| 8 | 0.65 | 离子反应的发生及书写 氧化还原反应方程式的配平 电化学计算 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 常见无机物的制备 物质含量的测定 物质制备的探究 | 工业流程题 |
| 11 | 0.65 | 常见官能团名称、组成及结构 卤代烃的性质 缩聚反应 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 10 | 0.65 | 原电池正负极判断 原电池电极反应式书写 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | |
| 12 | 0.65 | 化学键概念理解及判断 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 晶体的类型与物质熔点、硬度、导电性的关系 | |



