合成甲基橙( ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为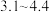 )的实验步骤如下:
)的实验步骤如下:
①在一支试管中加入 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),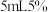 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和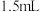 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在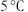 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。
②在试管中将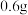 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入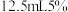 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。
③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。
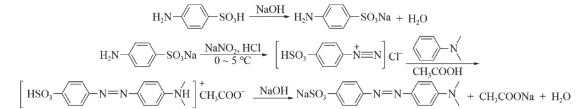
根据上述实验原理,下列说法错误的是
 ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为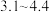 )的实验步骤如下:
)的实验步骤如下:①在一支试管中加入
 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),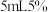 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和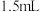 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在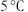 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。②在试管中将
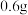 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入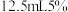 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。

根据上述实验原理,下列说法错误的是
| A.实验中得到的N,N-二甲基苯胺需要在蒸馏后才能使用 |
| B.使用乙醚洗涤的目的是为了除去产物中残留的乙醇和水 |
| C.重结晶操作时需要加入过量水使甲基橙溶解 |
| D.N,N-二甲基苯胺的蒸馏应当在通风橱中进行 |
更新时间:2024-02-19 17:33:53
|
【知识点】 物质分离、提纯综合应用解读
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】高锰酸钾在工业中广泛用作氧化剂。以软锰矿(主要成分是 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示: 生成。
生成。
②20℃时各物质的溶解度如下表。
下列说法错误的是
 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示: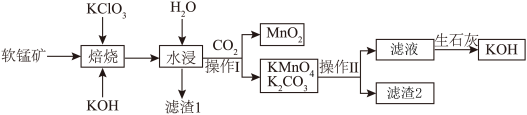
 生成。
生成。 ②20℃时各物质的溶解度如下表。
| 物质 |  |  |  |
| 溶解度/g | 6.38 | 111 | 11.1 |
A.“焙烧”时,主要反应的化学方程式为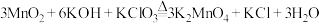 |
B.通入 时,理论上生成的 时,理论上生成的 和 和 的物质的量之比为 的物质的量之比为 |
C.若“焙烧”时加入的 过量,则制得的 过量,则制得的 中混有含 中混有含 元素的杂质 元素的杂质 |
D.操作Ⅱ为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】纳米材料Cu2O在光电领域有广泛应用。以硫酸厂的废渣(主要成分是CuO,含少量的Fe3O4、Fe2O3、SiO2、Al2O3等)为原料制备Cu2O的流程如图所示。已知:“还原”中氧化产物对环境友好。
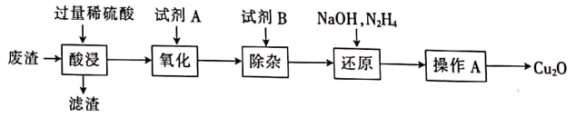
下列判断正确的是

下列判断正确的是
| A.“酸浸”时发生了氧化还原反应 |
| B.“除杂”得到的滤渣的主要成分是Fe2O3和Al2O3 |
| C.试剂A可能是H2O2 |
| D.制备14.4g Cu2O至少需要0.8g N2H4 |
您最近一年使用:0次


 Cu2++S+2H2O
Cu2++S+2H2O

