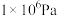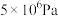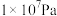工业制备硫酸的生产过程及相关信息如下。下列有关说法正确的是
温度/℃ | 不同压强下接触室中 | |
|
| |
450 | 99.2 | 99.7 |
550 | 94.9 | 97.7 |
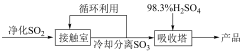
工艺流程 |
| |
A.循环利用的物质是 |
B. 为放热反应 为放热反应 |
C.吸收塔中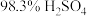 表现强氧化性 表现强氧化性 |
D.实际生产中,接触室中应采用温度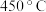 ,压强 ,压强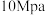 |
更新时间:2024-03-03 08:59:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验装置不能 达到实验目的的是
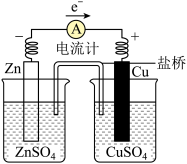 | 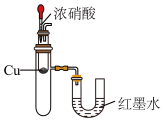 |  | 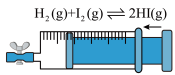 |
| A.探究铜锌原电池的工作原理 | B.验证Cu与浓硝酸反应的热量变化 | C.探究生铁在不同条件下的电化学腐蚀 | D.根据颜色变化探究压强对平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】在体积恒定的密闭容器中,一定量的SO2与1.100molO2在催化剂作用下加热到600℃发生反应:2SO2 + O2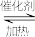 2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
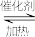 2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是| A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡 |
| B.降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| C.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为161.980g |
| D.达到平衡时,SO2的转化率为90% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体而被除去。在1L恒容密闭容器中充入1molCO和0.8molNO,发生反应2NO(g)+2CO(g)=N2(g)+2CO2(g) △H<0,测得平衡时NO的体积分数与温度、压强的关系如图所示,下列说法正确的是


| A.温度:T2<T1 |
| B.平衡常数:Kb=Kd<Ka=Kc |
C.反应速率: (d)= (d)= (c) (c) |
D.T1时,测得CO的平衡转化率为40%,则T1时反应的平衡常数为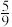 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氨催化氧化是工业制硝酸的重要反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2,平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是
4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2,平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是
 4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2,平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是
4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2,平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是| A.反应过程中分离出H2O(g),正反应速率增大 |
| B.反应达到平衡时,相同时间内消耗NH3和NO的物质的量相等 |
| C.平衡时向容器中继续通入O2,平衡正向移动,平衡常数增大 |
| D.其他条件不变,起始时投入2molNH3、2.5molO2,平衡时NH3的转化率小于60% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对已经达到化学平衡的反应: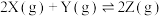 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是
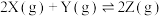 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】近年,科学家研究了乙醇催化合成乙酸乙酯的新方法: ,在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
,在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是

 ,在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
,在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
| A.反应温度不宜超过300℃ |
| B.该反应属于消去反应 |
| C.在催化剂作用下,乙醛是反应历程中的中间产物 |
| D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】近年,科学家研究了乙醇催化合成乙酸乙酯的新方法: 2C2H5OH(g)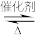 CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
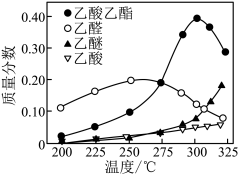
 CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
CH3COOC2H5(g)+2H2(g),在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是
| A.反应温度不宜超过300°C |
| B.在催化剂作用下,乙醛是反应历程中的中间产物 |
| C.提高催化剂的活性和选择性,减少乙醚、乙酸等副产物是工艺的关键 |
| D.该反应属于加成反应 |
您最近一年使用:0次

 的平衡转化率/
的平衡转化率/



 ,
,