某化学兴趣小组的同学欲除去固态氯化钠中混有的氯化钙。请根据如下实验方案回答相关问题:

(1)操作①所需主要玻璃仪器有_________________________
(2)反应①中加入略过量的A物质的目的是______________________ ;判断A已过量的实验操作方法是_______________________________________________ ;反应①的化学反应方程式为___________________________________________________ 。
(3)操作②的名称为__________________ ;反应②的离子方程式______________________ 。
(4)实验时称取样品质量为185.0g,经过操作①后,经洗涤、干燥后测得沉淀质量为50.0g,则样品中NaCl的质量百分数为_________________________ 。(保留到小数点后第一位)

(1)操作①所需主要玻璃仪器有
(2)反应①中加入略过量的A物质的目的是
(3)操作②的名称为
(4)实验时称取样品质量为185.0g,经过操作①后,经洗涤、干燥后测得沉淀质量为50.0g,则样品中NaCl的质量百分数为
更新时间:2017-11-14 15:09:39
|
【知识点】 物质分离、提纯综合应用解读
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】钒钛系 催化剂主要包含
催化剂主要包含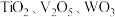 。从废
。从废 催化剂中回收
催化剂中回收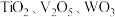 的某种工艺部分流程如下:
的某种工艺部分流程如下:

(1)“碱浸”选择高温的目的是
 元素可以形成多种配合物,在配合物
元素可以形成多种配合物,在配合物 中,提供孤电子对的是
中,提供孤电子对的是(2)钛酸钠
 ,则将其化学式写成氧化物的形式为
,则将其化学式写成氧化物的形式为 转化为
转化为 的化学方程式为
的化学方程式为(3)钒钨溶液中钨元素以
 的形式存在,调节
的形式存在,调节 为2~3,溶液中的
为2~3,溶液中的 会转化为
会转化为 ,再经萃取、反萃取等过程可制得
,再经萃取、反萃取等过程可制得 。写出
。写出 转化为
转化为 的离子方程式
的离子方程式(4)为测定废催化剂中
 的含量,现进行如下实验:准确称取
的含量,现进行如下实验:准确称取 废催化剂样品于烧杯中,加入足量质量分数为50%的硫酸,加热,冷却后将溶液移入
废催化剂样品于烧杯中,加入足量质量分数为50%的硫酸,加热,冷却后将溶液移入 容量瓶中,加水定容。准确量取
容量瓶中,加水定容。准确量取 溶液于锥形瓶中,滴加2~3滴指示剂,用浓度为
溶液于锥形瓶中,滴加2~3滴指示剂,用浓度为 的
的 标准溶液进行滴定,恰好完全反应时消耗标准溶液的体积为
标准溶液进行滴定,恰好完全反应时消耗标准溶液的体积为 。实验过程中,V元素最终转化为
。实验过程中,V元素最终转化为 ,计算废催化剂中
,计算废催化剂中 的含量为
的含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】我国是干电池的生产和消费大国。某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:

已知:经过反应Ⅰ后,所有金属元素均以离子形式存在。
回答下列问题:
(1)碱性锌锰干电池是以锌粉为负极,二氧化锰为正极,氢氧化钾溶液为电解质。电池总反应为2MnO2+Zn+2KOH=2MnOOH+K2ZnO2,请写出电池的正极反应式__________ 。
(2)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应化学方程式________________ 。
(3)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,请写出该反应的离子方程式______ 。
(4)反应Ⅲ中X可以是______ 。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(5)已知:H2S的电离常数K1=1.0×10−7,K2=7.0×10−15。0.1 mol/L NaHS的pH___ 7(填“>”“=”或“<”)。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L−1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=________ 。[已知:Ksp(MnS)=1.4×10−15]

已知:经过反应Ⅰ后,所有金属元素均以离子形式存在。
回答下列问题:
(1)碱性锌锰干电池是以锌粉为负极,二氧化锰为正极,氢氧化钾溶液为电解质。电池总反应为2MnO2+Zn+2KOH=2MnOOH+K2ZnO2,请写出电池的正极反应式
(2)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应化学方程式
(3)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,请写出该反应的离子方程式
(4)反应Ⅲ中X可以是
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(5)已知:H2S的电离常数K1=1.0×10−7,K2=7.0×10−15。0.1 mol/L NaHS的pH
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L−1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】Ⅰ、铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
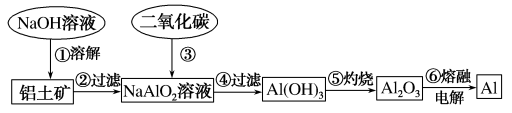
(1)请用离子方程式表示以上工艺流程中第①步反应:_______ 。
(2)写出以上工艺流程中第③步反应的化学方程式:_______ 。
(3)若第①步加入的是盐酸,则发生反应的离子方程式为_______ 。
Ⅱ、下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。
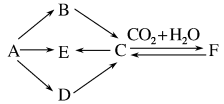
(4)写出下列物质的化学式:B_______ , C_______ , E_______ , F_______ 。
(5)写出下列各步反应的化学方程式:
C→E_______ ;
F→C_______ 。

(1)请用离子方程式表示以上工艺流程中第①步反应:
(2)写出以上工艺流程中第③步反应的化学方程式:
(3)若第①步加入的是盐酸,则发生反应的离子方程式为
Ⅱ、下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。

(4)写出下列物质的化学式:B
(5)写出下列各步反应的化学方程式:
C→E
F→C
您最近一年使用:0次



