某同学欲用浓H2SO4配制980mL 0.1mol·L-1的稀H2SO4。
(1)需要98%密度为1.84g·cm-3的浓硫酸______ mL。
(2)配制时,必须使用的仪器有______ (填代号),还缺少的仪器是______ 、______ 。
①烧杯;②10mL量筒;③20mL量筒;④托盘天平(带砝码);⑤玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是____________ 、___________ 。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”、“偏低”、“不影响”)。
①用量筒量取98%的硫酸时俯视________ 。
②如果加水超过了刻度线,取出水使液面恰好到刻度线________ 。
③容量瓶没有干燥________ 。
(1)需要98%密度为1.84g·cm-3的浓硫酸
(2)配制时,必须使用的仪器有
①烧杯;②10mL量筒;③20mL量筒;④托盘天平(带砝码);⑤玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”、“偏低”、“不影响”)。
①用量筒量取98%的硫酸时俯视
②如果加水超过了刻度线,取出水使液面恰好到刻度线
③容量瓶没有干燥
14-15高一上·内蒙古巴彦淖尔·期中 查看更多[5]
(已下线)广东省深圳市深圳中学2019-2020学年高一上学期期中考试化学试题山东省济宁市微山县第一中学2018-2019学年高一上学期10月月考化学试题江西省吉安县第三中学2019届高三上学期10月月考化学试题重庆市南开中学2018-2019学年高一上学期第一次月考化学试题2014-2015内蒙古巴彦淖尔市一中高一上学期期中考试化学试卷
更新时间:2018-09-23 22:57:44
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】“84消毒液”是一种以NaClO为主的高效含氯消毒剂,可用于灭活新型冠状病毒。某“84消毒液”瓶体部分标签如图所示,请回答下列问题:

(1)用 表示该“84消毒液”中NaClO的物质的量浓度,则
表示该“84消毒液”中NaClO的物质的量浓度,则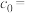
_______ 。
(2)某化学实验小组参阅该品牌“84消毒液”的标签,欲用NaClO固体配制240mL含NaClO浓度为 的消毒液。
的消毒液。
①配制此溶液需称量NaClO固体的质量为_______ g。
②在配制过程中,如图所示的仪器中不需要使用的是_______ (填字母),除玻璃棒外还缺少的玻璃仪器是_______ 。
A. B.
B. C.
C. D.
D.
③容量瓶上标有_______ (填字母)。
A.温度、容积、刻度线 B.温度、容积、压强
C.浓度、压强 D.浓度、温度、刻度线
④使用容量瓶前必须进行的一步操作是_______ 。
⑤下列操作会使所配制的溶液浓度偏高的是_______ (填字母)。
A.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
B.定容时,俯视容量瓶刻度线
C.利用实验室久置的NaClO固体来配制溶液
D.转移溶液时未洗涤烧杯和玻璃棒
E.容量瓶事先用NaClO溶液润洗一遍

(1)用
 表示该“84消毒液”中NaClO的物质的量浓度,则
表示该“84消毒液”中NaClO的物质的量浓度,则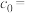
(2)某化学实验小组参阅该品牌“84消毒液”的标签,欲用NaClO固体配制240mL含NaClO浓度为
 的消毒液。
的消毒液。①配制此溶液需称量NaClO固体的质量为
②在配制过程中,如图所示的仪器中不需要使用的是
A.
 B.
B. C.
C. D.
D.
③容量瓶上标有
A.温度、容积、刻度线 B.温度、容积、压强
C.浓度、压强 D.浓度、温度、刻度线
④使用容量瓶前必须进行的一步操作是
⑤下列操作会使所配制的溶液浓度偏高的是
A.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
B.定容时,俯视容量瓶刻度线
C.利用实验室久置的NaClO固体来配制溶液
D.转移溶液时未洗涤烧杯和玻璃棒
E.容量瓶事先用NaClO溶液润洗一遍
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用质量分数为36.5%的浓盐酸(密度为1.16g•cm-3)配制成1mol•L-1的稀盐酸。现实验室需这种盐酸220mL,试回答下列问题:
(1)配制稀盐酸时,应选用________ mL的容量瓶。
(2)经计算需要________ mL浓盐酸,在量取时宜选用量筒________ (填序号)。
A.5mL B.10mL C.25mL D.50mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面距容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是________ (填序号)。
(4)在上述配制过程中,用刚刚用蒸馏水洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度会________ (填“偏高”“偏低”或“无影响”)。若容量瓶用蒸馏水洗涤后残留有少量的水,其配制的稀盐酸浓度会________ (填“偏高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁和玻璃棒或未将洗涤液注入容量瓶,则配制的稀盐酸浓度会________ (填“偏高”“偏低”或“无影响”)。
(1)配制稀盐酸时,应选用
(2)经计算需要
A.5mL B.10mL C.25mL D.50mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面距容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(4)在上述配制过程中,用刚刚用蒸馏水洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度会
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某同学在实验室中称取20 g NaOH固体,配制500 mL 1 mol·L-1的氢氧化钠溶液。
(1)该同学准备的实验用品有:托盘天平(带砝码)、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有__________ 、_____________ 、_______________ 。
(2)下列有关实验操作,正确的是__________ 。
A.称量氢氧化钠固体时,应该放在称量纸上称量
B.某同学将称量的氢氧化钠固体溶解并冷却至室温,然后转移到容量瓶中
C.某同学在定容时,不小心加水超过刻度线,又将多余的液体吸出直至刻度线
D.某同学在溶解、转移完氢氧化钠溶液后,将溶解用的仪器洗涤2~3次,并将洗涤液转移到容量瓶中
(3)玻璃棒在该实验中的作用有①___________ ,②_________ 。
(4)若实验室遇到下列情况,对氢氧化钠溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”):
①转移时,有少量的溶液洒落出容量瓶_______________________ 。
②定容时,容量瓶中事先有洁净的蒸馏水,所配溶液的浓度____________________ 。
(1)该同学准备的实验用品有:托盘天平(带砝码)、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有
(2)下列有关实验操作,正确的是
A.称量氢氧化钠固体时,应该放在称量纸上称量
B.某同学将称量的氢氧化钠固体溶解并冷却至室温,然后转移到容量瓶中
C.某同学在定容时,不小心加水超过刻度线,又将多余的液体吸出直至刻度线
D.某同学在溶解、转移完氢氧化钠溶液后,将溶解用的仪器洗涤2~3次,并将洗涤液转移到容量瓶中
(3)玻璃棒在该实验中的作用有①
(4)若实验室遇到下列情况,对氢氧化钠溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”):
①转移时,有少量的溶液洒落出容量瓶
②定容时,容量瓶中事先有洁净的蒸馏水,所配溶液的浓度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室用NaOH固体配制480mL 1.0 氢氧化钠溶液。
氢氧化钠溶液。
(1)配制上述溶液,需要称取NaOH固体_________ g。
(2)配制上述溶液除需要天平、药匙、玻璃棒、胶头滴管外,还需要的仪器有_________ 、_________ 。
(3)下列关于250ml容量瓶的操作,正确的是_________。
(4)实验过程中,玻璃棒的作用有_________ 、_________ 。
(5)写出下列操作对所配氯化钠溶液浓度的影响(填“偏高”“偏低”或“无影响”)
Ⅰ.转移溶液后,未洗涤小烧杯和玻璃棒;_________ 。
Ⅱ.定容时,加水超过了刻度线,吸出一部分水;_________ 。
 氢氧化钠溶液。
氢氧化钠溶液。(1)配制上述溶液,需要称取NaOH固体
(2)配制上述溶液除需要天平、药匙、玻璃棒、胶头滴管外,还需要的仪器有
(3)下列关于250ml容量瓶的操作,正确的是_________。
A. | B. | C. | D. |
(5)写出下列操作对所配氯化钠溶液浓度的影响(填“偏高”“偏低”或“无影响”)
Ⅰ.转移溶液后,未洗涤小烧杯和玻璃棒;
Ⅱ.定容时,加水超过了刻度线,吸出一部分水;
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】纯碱是生活中常用的去油污洗涤剂。某同学欲用碳酸钠晶体(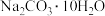 )配制
)配制 的纯碱溶液。请回答下列问题:
的纯碱溶液。请回答下列问题:
(1)计算所需要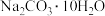 的质量为
的质量为________ g。
(2)取该溶液20mL稀释到100mL后的溶液中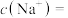
__________  。
。
(3)完成上述实验,除需要如图所示的仪器外,还需要的玻璃仪器是_________ 。

(4)下列实验操作会使所配制溶液浓度偏低的是__________ (填标号)。
A.容量瓶内有水,未经过干燥处理
B.定容时,仰视刻度线
C.转移溶液后的烧杯和玻璃棒未洗涤
D.定容后上下颠倒容量瓶几次,发现溶液的凹液面最低点低于刻度线,再补加水到刻度线
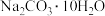 )配制
)配制 的纯碱溶液。请回答下列问题:
的纯碱溶液。请回答下列问题:(1)计算所需要
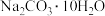 的质量为
的质量为(2)取该溶液20mL稀释到100mL后的溶液中
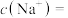
 。
。(3)完成上述实验,除需要如图所示的仪器外,还需要的玻璃仪器是

(4)下列实验操作会使所配制溶液浓度偏低的是
A.容量瓶内有水,未经过干燥处理
B.定容时,仰视刻度线
C.转移溶液后的烧杯和玻璃棒未洗涤
D.定容后上下颠倒容量瓶几次,发现溶液的凹液面最低点低于刻度线,再补加水到刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学实验室需要480mL,0.5mol/L的稀硫酸,现欲用98%的浓硫酸(ρ=1.84g/cm3)配制,配制步骤包括:①计算所用浓硫酸的体积②转移③定容、上下颠倒摇匀④量取一定体积的浓硫酸⑤洗涤并转移⑥稀释并冷却至室温⑦轻摇混匀。完成下列问题:
(1)正确的操作顺序为(填入序号)________ 。选用的主要仪器有:量筒、烧杯、玻璃棒、________ 、________ 。
(2)应量取浓硫酸的体积为________ ;量取浓硫酸所用的量筒的规格是________ (从下列中选用,填字母 A.10 mL B.25 mL C.50 mL D.100 mL);第⑥步中稀释实验的操作方法是________ 。
(3)下列关于容量瓶的使用方法中,正确的是________ 。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是________ 。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
(1)正确的操作顺序为(填入序号)
(2)应量取浓硫酸的体积为
(3)下列关于容量瓶的使用方法中,正确的是
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某兴趣小组利用废旧电池的铜帽(铜锌总含量约99%)制备了CuSO4·5H2O样品,制备流程如下:

(1)“溶解II”过程中,发生反应的离子方程式为________ 。
(2)“溶解II”过程中应控制反应温度,温度不能过高的原因是________ 。
(3)为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00mL。实验过程中发生的反应如下:2Cu2++4I-=2CuI↓+I2; 2 +I2=
+I2= +2I-。
+2I-。
①配制250mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有_____ 。
②计算出样品中CuSO4·5H2O的质量分数_____ 。(写出计算过程)

(1)“溶解II”过程中,发生反应的离子方程式为
(2)“溶解II”过程中应控制反应温度,温度不能过高的原因是
(3)为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00mL。实验过程中发生的反应如下:2Cu2++4I-=2CuI↓+I2; 2
 +I2=
+I2= +2I-。
+2I-。①配制250mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有
②计算出样品中CuSO4·5H2O的质量分数
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用18.4 mol·L-1的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒、②烧瓶、③烧杯、④胶头滴管、⑤量筒、⑥容量瓶、⑦托盘天平。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)________ 。
(2)经计算,需量取浓H2SO4________ mL。现有①10 mL、②50 mL、③100 mL三种规格的量筒,你选用的量筒是________ (写序号)。
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到______ mL的容量瓶中。
(4)在配制过程中,其他操作都准确,下列操作中能引起误差偏高的有________ (填代号)。
①定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
②转移前,容量瓶中含有少量蒸馏水
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线
(5)在下图的配制过程示意图中,正确的是(填写序号)_______ 。
A.称量
B.溶解
C.转移
D.定容
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)
(2)经计算,需量取浓H2SO4
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到
(4)在配制过程中,其他操作都准确,下列操作中能引起误差偏高的有
①定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
②转移前,容量瓶中含有少量蒸馏水
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线
(5)在下图的配制过程示意图中,正确的是(填写序号)
A.称量

B.溶解

C.转移

D.定容

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学实验室需要480mL,0.5mol/L的稀硫酸,现欲用98%的浓硫酸(ρ=1.84g/cm3)配制,配制步骤包括:①计算所用浓硫酸的体积②转移③定容、上下颠倒摇匀④量取一定体积的浓硫酸⑤洗涤并转移⑥稀释并冷却至室温⑦轻摇混匀。完成下列问题:
(1)正确的操作顺序为(填入序号)________ 。选用的主要仪器有:量筒、烧杯、玻璃棒、________ 、________ 。
(2)应量取浓硫酸的体积为________ ;量取浓硫酸所用的量筒的规格是________ (从下列中选用,填字母 A.10 mL B.25 mL C.50 mL D.100 mL);第⑥步中稀释实验的操作方法是________ 。
(3)下列关于容量瓶的使用方法中,正确的是________ 。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是________ 。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
(1)正确的操作顺序为(填入序号)
(2)应量取浓硫酸的体积为
(3)下列关于容量瓶的使用方法中,正确的是
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.用量筒量取浓硫酸时仰视刻度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】小组同学探究 的性质及工业制法。
的性质及工业制法。
(1)用 固体配制
固体配制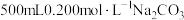 溶液。
溶液。
i.用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、___________ 。
ii.计算需要 固体的质量是
固体的质量是___________ g。
iii.下列主要操作步骤的正确顺序是___________ (填字母)。
a.称取一定质量的碳酸钠固体,放入烧杯中,加入适量蒸馏水溶解;
b.向容量瓶中加水至液面离容量瓶刻度线下1-2cm,改用胶头滴管向容量瓶中加入蒸馏水至凹液面与刻度线相切;
c.将溶液转移到500mL容量瓶中;
d.盖好瓶塞,反复翻转,摇匀;
e.用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
iv.下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究 与盐酸的反应。向
与盐酸的反应。向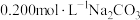 溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: 、
、___________ 。
(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。通过“联合制碱法”得到的纯碱产品中往往含少量 ,为测定产品中
,为测定产品中 的质量分数,进行如下操作:
的质量分数,进行如下操作:
①称取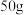 样品放入烧杯内加水溶解。
样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,经过滤、___________ 等操作,称量沉淀的质量为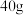 。则样品中
。则样品中 的质量分数为
的质量分数为___________ 。
 的性质及工业制法。
的性质及工业制法。(1)用
 固体配制
固体配制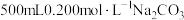 溶液。
溶液。i.用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、
ii.计算需要
 固体的质量是
固体的质量是iii.下列主要操作步骤的正确顺序是
a.称取一定质量的碳酸钠固体,放入烧杯中,加入适量蒸馏水溶解;
b.向容量瓶中加水至液面离容量瓶刻度线下1-2cm,改用胶头滴管向容量瓶中加入蒸馏水至凹液面与刻度线相切;
c.将溶液转移到500mL容量瓶中;
d.盖好瓶塞,反复翻转,摇匀;
e.用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
iv.下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
(2)探究
 与盐酸的反应。向
与盐酸的反应。向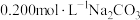 溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:
溶液中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为: 、
、(3)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。通过“联合制碱法”得到的纯碱产品中往往含少量
 ,为测定产品中
,为测定产品中 的质量分数,进行如下操作:
的质量分数,进行如下操作:①称取
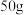 样品放入烧杯内加水溶解。
样品放入烧杯内加水溶解。②加入过量的氯化钙溶液充分反应,经过滤、
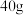 。则样品中
。则样品中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室需要450mL 0.1mol·L-1NaOH溶液。根据溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_______ (填序号),配制上述溶液需用到_______ mL的容量瓶。根据计算用托盘天平称取NaOH的质量为_______ g。

(2)下列操作中,正确的是_______ (填字母)。

(3)在配制NaOH溶液的过程中,下列情况对NaOH溶液物质的量浓度有何影响(填“偏大”“偏小”或“无影响”)。
①未经冷却趁热将溶液注入容量瓶中定容:_______ 。
②定容时仰视观察液面:_______ 。
③移液时不小心将部分溶液洒出:_______ 。
(1)如图所示的仪器中配制溶液肯定不需要的是

(2)下列操作中,正确的是

(3)在配制NaOH溶液的过程中,下列情况对NaOH溶液物质的量浓度有何影响(填“偏大”“偏小”或“无影响”)。
①未经冷却趁热将溶液注入容量瓶中定容:
②定容时仰视观察液面:
③移液时不小心将部分溶液洒出:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】如图是硫酸试剂瓶标签上的内容:
(1)该硫酸的物质的量浓度是____________ mol/L。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要460 mL 0.5 mol/L稀硫酸,则需要取____________ mL的该浓硫酸。
(3)将蒸馏水注入容量瓶,当液面离容量瓶刻度线1~2 cm时,__________________ 。
(4)配制溶液有如下(未按顺序排列):a.溶解;b.摇匀;c.洗涤;d.冷却;e.称量;f.将溶液移至容量瓶;g.定容等操作。其中摇匀的前一步操作是___________ (填写字母) 。
(5)下列配制过程示意图中,有不正确的是(填写序号):__________________ 。

(6)配制0.5 mol/L稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高的是_____ 。
A.用量筒量取浓硫酸时仰视读数
B.未经冷却将溶液注入容量瓶中
C.摇匀后液面低于刻度线,再滴加蒸馏水
D.未洗涤烧杯和玻璃棒
| 硫酸:化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g·cm-3 质量分数:98% |
(1)该硫酸的物质的量浓度是
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要460 mL 0.5 mol/L稀硫酸,则需要取
(3)将蒸馏水注入容量瓶,当液面离容量瓶刻度线1~2 cm时,
(4)配制溶液有如下(未按顺序排列):a.溶解;b.摇匀;c.洗涤;d.冷却;e.称量;f.将溶液移至容量瓶;g.定容等操作。其中摇匀的前一步操作是
(5)下列配制过程示意图中,有不正确的是(填写序号):

(6)配制0.5 mol/L稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高的是
A.用量筒量取浓硫酸时仰视读数
B.未经冷却将溶液注入容量瓶中
C.摇匀后液面低于刻度线,再滴加蒸馏水
D.未洗涤烧杯和玻璃棒
您最近一年使用:0次



