名校
1 . 完成下列问题。
(1)重铬酸钾(K2Cr2O7为橙色,K2CrO4为黄色)溶液存在着如下平衡: +H2O⇌2
+H2O⇌2 +2H+。
+2H+。
①若平衡体系的pH=2,则溶液显______ 色。
②能说明该反应达平衡状态的是_______ 。
a.溶液呈酸性 b.溶液的颜色不变
c.2v( )=v(
)=v( ) d.
) d. 和
和 的浓度相同
的浓度相同
(2)25℃时,2NO2(g)⇌N2O4(g) △H=-56.9kJ/mol。
①该反应的化学平衡常数表达式_____ 。
②其它条件不变,缩小容器体积,达到新平衡,此过程的现象:______ 。
③其它条件不变,将该体系升温至100℃,此过程的现象:_______
(3)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂。
①用离子方程式表示净水的原因:______ 。
②明矾溶液中滴加Ba(OH)2溶液至 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH____ 7(填“>”“=”或“<”,下同)。
③明矾溶液中离子浓度由大到小的顺序:_______ 。
(1)重铬酸钾(K2Cr2O7为橙色,K2CrO4为黄色)溶液存在着如下平衡:
 +H2O⇌2
+H2O⇌2 +2H+。
+2H+。①若平衡体系的pH=2,则溶液显
②能说明该反应达平衡状态的是
a.溶液呈酸性 b.溶液的颜色不变
c.2v(
 )=v(
)=v( ) d.
) d. 和
和 的浓度相同
的浓度相同(2)25℃时,2NO2(g)⇌N2O4(g) △H=-56.9kJ/mol。
①该反应的化学平衡常数表达式
②其它条件不变,缩小容器体积,达到新平衡,此过程的现象:
③其它条件不变,将该体系升温至100℃,此过程的现象:
(3)明矾[KAl(SO4)2·12H2O]是一种常用的净水剂。
①用离子方程式表示净水的原因:
②明矾溶液中滴加Ba(OH)2溶液至
 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH③明矾溶液中离子浓度由大到小的顺序:
您最近一年使用:0次
名校
解题方法
2 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,从氧化还原反应的角度探究它们的性质。
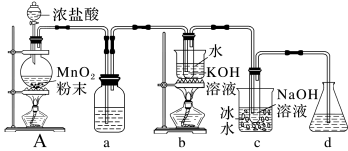
回答下列问题:
(1)A中盛放MnO2粉末的仪器名称是___________ ,A中发生化学反应的方程式是___________ ;
(2)a中盛放的是饱和食盐水,其作用是___________ ;
(3)b中采用的加热方式是___________ ,A中产生的气体与c中NaOH反应的离子方程式___________ ;
(4)d的作用是___________ ;
(5)A中产生气体与b中的KOH反应产生KClO3、KCl和 H2O的方程式___________ 。

回答下列问题:
(1)A中盛放MnO2粉末的仪器名称是
(2)a中盛放的是饱和食盐水,其作用是
(3)b中采用的加热方式是
(4)d的作用是
(5)A中产生气体与b中的KOH反应产生KClO3、KCl和 H2O的方程式
您最近一年使用:0次
名校
3 . (1)填写关于物质的量计算的四个恒等式:n=______ =______ =______ =_______ 。
(2)已知下列四个反应:
A.2Na+2H2O=2NaOH+H2↑ B.2F2+2H2O=4HF+O2
C.Cl2+H2O=HCl+HClO D.C+H2O(g) CO+H2
CO+H2
试从氧化还原的角度,回答下列问题:
①水只作氧化剂的是________ ;
②水只作还原剂的是________ ;
③水既不作氧化剂又不作还原剂的是________ 。
(3) KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为KClO3+HCl(浓)=KCl+ClO2↑+Cl2↑+H2O。
①请配平上述化学方程式_____ 。
②产生0.1molCl2,则转移的电子的物质的量为______ mol。
(2)已知下列四个反应:
A.2Na+2H2O=2NaOH+H2↑ B.2F2+2H2O=4HF+O2
C.Cl2+H2O=HCl+HClO D.C+H2O(g)
 CO+H2
CO+H2试从氧化还原的角度,回答下列问题:
①水只作氧化剂的是
②水只作还原剂的是
③水既不作氧化剂又不作还原剂的是
(3) KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为KClO3+HCl(浓)=KCl+ClO2↑+Cl2↑+H2O。
①请配平上述化学方程式
②产生0.1molCl2,则转移的电子的物质的量为
您最近一年使用:0次
2020-09-29更新
|
74次组卷
|
2卷引用:西藏自治区拉萨市拉萨中学2020-2021学年高二第一次月考理综化学试题
解题方法
4 . 本题为《化学与生活(选修1)》选做题。
(1)资源必须要合理使用。
水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是______(填字母代号)
(2)矿泉水瓶不能随意丢弃.根据垃圾分类方法,矿泉水瓶属于_____________ (填“可回收物”或“可堆肥垃圾”);
(3)在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向大气的排放,减小环境污染。在催化转化器中,CO和NO发生反应.请完成该反应的化学主程式_____________ 。
(4)保护环境、爱护地球已成为人们的共同呼声。
我们常在公共场所见到下列标志,其中属于回收标志的是__________

(5)2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是____________。
(6)化学与生活关系密切。现有下列四种物质:
A.蛋白质 B.亚硝酸盐 C.维生素C D.油脂
①__________ 是重要的体内能源;
②__________ 广泛存在于新鲜水果和绿色蔬菜中,有酸性和还原性,又称为抗坏血酸;
(7)材料是人类赖以生存和发展的重要物质基础
试管、烧杯和烧瓶等化学仪器的主要材质是__________;
(8) “辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料。生铁和钢成分上的主要差别是_________;
(9)钢铁在潮湿空气中易发生吸氧腐蚀,负极反应式为__________ 。
(1)资源必须要合理使用。
水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是______(填字母代号)
| A.科学合理使用农药 | B.任意排放化工厂废水 | C.处理生活污水,达标排放 |
(3)在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向大气的排放,减小环境污染。在催化转化器中,CO和NO发生反应.请完成该反应的化学主程式
(4)保护环境、爱护地球已成为人们的共同呼声。
我们常在公共场所见到下列标志,其中属于回收标志的是

(5)2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是____________。
| A.吸烟会对室内和公共场所造成污染 |
| B.吸入焦油、尼古丁及颗粒物可导致多种病变 |
| C.N2、CO2、CO尼古丁和都属于室内空气污染物 |
A.蛋白质 B.亚硝酸盐 C.维生素C D.油脂
①
②
(7)材料是人类赖以生存和发展的重要物质基础
试管、烧杯和烧瓶等化学仪器的主要材质是__________;
| A.玻璃 | B.陶瓷 | C.水泥 |
| A.碳的含量不同 |
| B.磷、硫的含量不同 |
| C.镍、铬等金属含量不同 |
您最近一年使用:0次
2019-01-30更新
|
80次组卷
|
2卷引用:2015-2016学年西藏日喀则一中高二6月月考化学试卷
10-11高二·西藏拉萨·阶段练习
5 . (Ⅰ)配平下列氧化还原反应方程式:
(i)____ Cu2S+____ HNO3===____ Cu(NO3)2+____ NO↑+____ H2SO4+____ H2O
(ii)____ NO3-+____ Zn+____ OH-+____ H2O===____ NH3↑+____ Zn(OH)4-
(Ⅱ)某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:
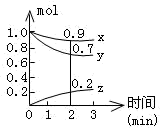
(1)计算反应开始2min内的vx=__________ ,vy=_____________ ,vz=__________ 。
(2)容器内的反应物是______________ 。
(3)写出该反应的化学方程式__________________ 。
(i)
(ii)
(Ⅱ)某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:

(1)计算反应开始2min内的vx=
(2)容器内的反应物是
(3)写出该反应的化学方程式
您最近一年使用:0次



