解题方法
1 . 下列物质的颜色变化与氧化还原反应无关的是
| A.浓硝酸久置后颜色变黄 |
B.将 溶液加热,溶液由蓝色变为绿色 溶液加热,溶液由蓝色变为绿色 |
C.将 粉末露置在空气中,固体由淡黄色变为白色 粉末露置在空气中,固体由淡黄色变为白色 |
D.向 酸性溶液中加入乙醇,溶液由橙色变为绿色 酸性溶液中加入乙醇,溶液由橙色变为绿色 |
您最近一年使用:0次
2 . 某化学兴趣小组同学按图示装置进行实验,产生足量的气体通入c中,最终出现浑浊。下列所选物质组合符合要求的是
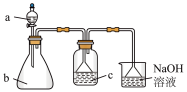
| 选项 | a中试剂 | b中试剂 | c中试剂 | |
| A | 浓硫酸 | 浓盐酸 | 饱和食盐水 | |
| B | 浓硫酸 | Cu |  溶液 溶液 | |
| C | 稀盐酸 | 大理石 |  溶液 溶液 | |
| D | 浓硫酸 | 亚硫酸钠 |  溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列描述的事实不符合“量变引起质变”的哲学观点的是
| A.配制银氨溶液时,向硝酸银溶液中滴入氨水至生成的沉淀恰好溶解 |
| B.向AlCl3溶液中逐滴滴加NaOH溶液至生成的沉淀溶解 |
| C.向稀硝酸中逐渐加入铁粉,溶液由无色变为黄色,然后变为浅绿色 |
| D.用NaOH溶液吸收NO2时,NO2既是氧化剂又是还原剂 |
您最近一年使用:0次
4 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
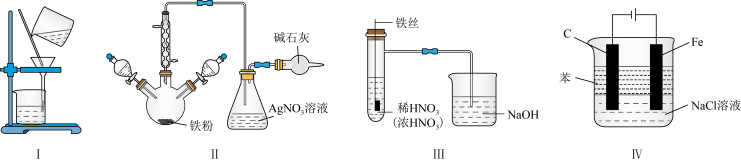
| A.用装置Ⅰ除去苯中的三溴苯酚 |
| B.用装置Ⅱ证明苯与溴发生取代反应 |
| C.用装置Ⅲ证明不同浓度硝酸还原产物可为NO、NO2 |
| D.用装置Ⅳ制备并较长时间观察到Fe(OH)2 |
您最近一年使用:0次
2024-05-31更新
|
141次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
5 . “探究与创新能力”是化学的关键能力。下列各项中“操作或现象”能达到预期“实验目的”的是
| 选项 | 实验目的 | 操作或现象 |
| A | 制作简单原电池 | 将铁钉和铜丝用导线连接并插入FeCl3 溶液中即可形成原电池 |
| B | 验证碳能与浓硝酸反应 | 向浓硝酸中插入红热的碳,产生红棕色气体 |
| C | 鉴别溴蒸气和NO2 | 分别通入AgNO3 溶液中,产生浅黄色沉淀的是溴蒸气 |
| D | 向某溶液中加入足量稀硝酸,无明显现象,再加入 Ba(NO3)2 溶液,出现白色沉淀 | 溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列有关氮及其化合物的说法错误的是
| A.氮气是工业合成氨的原料 | B.氨遇氯化氢产生白烟 |
| C.铵盐受热易分解 | D.稀硝酸与铁反应产生氢气 |
您最近一年使用:0次
解题方法
7 . I、回答下列问题
(1)以太阳能为热源,利用纳米级 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为___________ (填名称);过程I的化学方程式为___________ ;反应中生成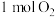 ,则同时生成
,则同时生成
___________ L(标准状况下)。
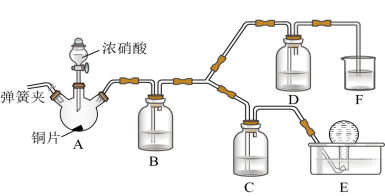
(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为___________ 。
②装置A中发生反应的化学方程式为___________ ;装置B的作用为___________ 。
③装置D中的现象为___________ ;C中盛放的试剂为___________ 。
(3)在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
(1)以太阳能为热源,利用纳米级
 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为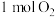 ,则同时生成
,则同时生成

(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
(3)在碱性条件下,
 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 亚硝酰氯NOCl常用于合成洗涤剂及合成中间体,某学习小组在实验室利用 反应制备NOCl,设计如图实验装置(夹持装置略去)。
反应制备NOCl,设计如图实验装置(夹持装置略去)。
①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应 。
。
回答下列问题:
(1)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?________ (填“合理”或“不合理”),试说明原因:_______________ .
(2)实验时,应先在三颈烧瓶内通入__________ (填“ ”或“NO”),另一种气体可以通入的标志是
”或“NO”),另一种气体可以通入的标志是______________________________ .
(3)实验中用NaOH溶液进行尾气处理。①无水 的作用是
的作用是_________________ 。②尾气处理时,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与_________ (填化学式)同时通入NaOH溶液中。
 反应制备NOCl,设计如图实验装置(夹持装置略去)。
反应制备NOCl,设计如图实验装置(夹持装置略去)。
①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应
 。
。回答下列问题:
(1)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?
(2)实验时,应先在三颈烧瓶内通入
 ”或“NO”),另一种气体可以通入的标志是
”或“NO”),另一种气体可以通入的标志是(3)实验中用NaOH溶液进行尾气处理。①无水
 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式正确的是
A. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
B.向 稀溶液中加入盐酸: 稀溶液中加入盐酸: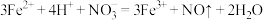 |
C.用 溶液吸收废气中的 溶液吸收废气中的 : :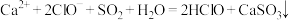 |
D.用热的NaOH溶液溶解S: |
您最近一年使用:0次
解题方法
10 . 氮氧化物(NOx)是大气污染物之一,处理工业废气中的NOx对于环境保护具有重要的意义。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。_______ ;装置B内的试剂是______ 。
②装置D中发生反应的离子方程式是_______ ,铜丝可抽动的优点是________ 。
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为______ 。
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):_____ ,c(NaOH)=_____ 。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。

②装置D中发生反应的离子方程式是
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O。
用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):

您最近一年使用:0次



