1 . 宏观辨识与微观探析是化学学科重要的学科素养。回答下列问题:
Ⅰ.已知某无色水样中只含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:
①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是__________ (填离子符号,下同),可能存在的离子是__________ ,一定不存在的离子是__________ 。
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是__________ 。
Ⅱ.现有 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
(3)溶液A、B、C、D中的溶质依次为__________ 、__________ 、__________ 、__________ (填化学式)。
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为__________ (填化学式)。
Ⅰ.已知某无色水样中只含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是
Ⅱ.现有
 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的
 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。②向①中反应后的四支试管中,分别依次加入足量
 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。(3)溶液A、B、C、D中的溶质依次为
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为
您最近一年使用:0次
2 . 下列对于铵盐的描述都正确的是
①绝大多数都溶于水 ②都是白色或无色晶体 ③都有刺激性气味 ④加热后都有氮气放出
⑤与碱混合后加热都有氨气放出 ⑥都能使石蕊试纸变蓝
①绝大多数都溶于水 ②都是白色或无色晶体 ③都有刺激性气味 ④加热后都有氮气放出
⑤与碱混合后加热都有氨气放出 ⑥都能使石蕊试纸变蓝
| A.全部 | B.①②⑤⑥ | C.①②⑤ | D.③④⑤ |
您最近一年使用:0次
名校
解题方法
3 . 下列反应的离子方程式不正确的是
A.向 溶液中缓慢滴加 溶液中缓慢滴加 溶液: 溶液: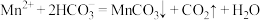 |
B.向苯酚钠溶液中通入少量二氧化碳: |
C.向 溶液中加入足量 溶液中加入足量 溶液: 溶液: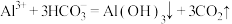 |
D.向 溶液中加入过量 溶液中加入过量 溶液: 溶液: |
您最近一年使用:0次
4 . 含氮物质的分类与相应化合价的关系如图所示。下列说法不正确的是

A. ③与 ③与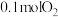 完全反应后生成④的分子数小于 完全反应后生成④的分子数小于 |
| B.②的氧化或还原均可实现氮的固定 |
| C.⑤的浓溶液可以溶解金和铂 |
D.⑥中加入浓 溶液并加热可产生① 溶液并加热可产生① |
您最近一年使用:0次
2024-05-24更新
|
126次组卷
|
2卷引用:广东省部分学校2024届高三下学期5月份大联考化学试题
名校
5 . 下列物质中既能与稀硫酸反应产生气体,又能与氢氧化钠溶液(允许加热)反应产生气体的是:①Al ② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
| A.①⑤⑥ | B.①③⑤⑥ | C.①③⑤⑥⑦ | D.①②③④⑤⑥⑦ |
您最近一年使用:0次
名校
6 . 下列各组离子在指定条件下可能大量共存的是
A.0.1  溶液: 溶液: 、 、 、 、 、 、 |
B.能使甲基橙变红的溶液中: 、 、 、 、 、 、 |
C.水电离出的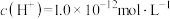 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.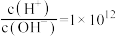 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-05-23更新
|
68次组卷
|
2卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(五)
7 . 现有一包由 、
、 、
、 、
、 、
、 和
和 中的三种物质组成的混合物,通过如下实验确定其组成,则混合物的成分可能是
中的三种物质组成的混合物,通过如下实验确定其组成,则混合物的成分可能是
 、
、 、
、 、
、 、
、 和
和 中的三种物质组成的混合物,通过如下实验确定其组成,则混合物的成分可能是
中的三种物质组成的混合物,通过如下实验确定其组成,则混合物的成分可能是步骤 | 操作及现象 |
① | 取少量粉末溶于水,产生白色沉淀,放出有刺激性气味的气体 |
② | 过滤,得到白色固体和透明溶液 |
③ | 取②中固体,加入足量 溶液,固体全部溶解 溶液,固体全部溶解 |
A. 、 、 和 和 | B. 、 、 和 和 |
C. 、 、 和 和 | D. 、 、 和 和 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.铵盐都能与碱反应,不能与酸反应 |
| B.铵盐受热分解一定都会产生NH3 |
C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为 +OH- =NH3↑+H2O +OH- =NH3↑+H2O |
| D.可以用NaOH溶液鉴别Na2SO4、NH4NO3、KCl、(NH4)2SO4四种溶液 |
您最近一年使用:0次
解题方法
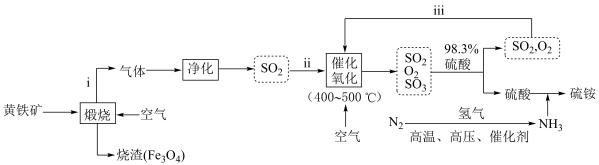
9 . 硫酸铵[(NH4)2SO4]俗称硫铵、肥田粉。模拟以黄铁矿(主要成分为FeS2)为原料制备硫酸铵的一种流程如图所示:
(1)步骤ⅲ的目的是____________ 。
(2)“煅烧”过程中发生反应的化学方程式为_____________ ;在该反应中,36.0gFeS2完全反应时转移______ mol电子。
(3)合成氨反应中,1molN2和4molH2在催化剂、高温、高压作用下合成NH3的物质的量_______ (填“>”“<”或“=”)2mol。
(4)如果直接用水吸收SO3,会形成大量“酸雾”,污染环境。由此推知,SO3和H2O的反应是_____ (填“吸”或“放”)热反应。
(5)利用Fe3O4可以制备高纯度铁红,其步骤如下:
步骤1:用足量稀硫酸溶解Fe3O4。
步骤2:向溶液中加入足量双氧水,氧化亚铁离子。
步骤3:加入过量NaOH溶液,过滤﹑洗涤、灼烧。
步骤2中氧化亚铁离子的离子方程式为_________________ 。
(6)测定硫酸铵产品纯度(假设杂质不参加反应):取Wg硫酸铵产品于试管中,向其中加入足量NaOH溶液,共热;产生的气体用V1mLc1mol/L盐酸吸收,得到吸收液;再向吸收液中滴加V2mLc2mol/LNaOH溶液恰好完全中和过量的盐酸。该产品中(NH4)2SO4的质量分数为________ (用含c1、V1、c2、V2、W的代数式表示)。
(1)步骤ⅲ的目的是
(2)“煅烧”过程中发生反应的化学方程式为
(3)合成氨反应中,1molN2和4molH2在催化剂、高温、高压作用下合成NH3的物质的量
(4)如果直接用水吸收SO3,会形成大量“酸雾”,污染环境。由此推知,SO3和H2O的反应是
(5)利用Fe3O4可以制备高纯度铁红,其步骤如下:
步骤1:用足量稀硫酸溶解Fe3O4。
步骤2:向溶液中加入足量双氧水,氧化亚铁离子。
步骤3:加入过量NaOH溶液,过滤﹑洗涤、灼烧。
步骤2中氧化亚铁离子的离子方程式为
(6)测定硫酸铵产品纯度(假设杂质不参加反应):取Wg硫酸铵产品于试管中,向其中加入足量NaOH溶液,共热;产生的气体用V1mLc1mol/L盐酸吸收,得到吸收液;再向吸收液中滴加V2mLc2mol/LNaOH溶液恰好完全中和过量的盐酸。该产品中(NH4)2SO4的质量分数为
您最近一年使用:0次
解题方法
10 . 某溶液呈酸性,可能含有: 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:
Ⅰ.取少量溶液,向其中加入过量 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。
Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。
(1)上述6种离子中,该溶液肯定存在的为____________ ,肯定不存在 的为______ ,不能 确定是否存在的为______ 。
(2)请设计实验检验原溶液中是否存在 ,写出操作方法、现象及结论
,写出操作方法、现象及结论___________ 。
(3)生成无色气体 的离子方程式为
的离子方程式为____________ 。
(4)步骤Ⅱ中发生反应的离子方程式为___________________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种。对其进行如下实验:
中的若干种。对其进行如下实验:Ⅰ.取少量溶液,向其中加入过量
 ,生成白色沉淀
,生成白色沉淀 和无色气体
和无色气体 ,该无色气体在空气中变为红棕色。
,该无色气体在空气中变为红棕色。Ⅱ.将Ⅰ中所得溶液滤去沉淀后,加入过量浓
 溶液,生成无色气体,最终得到红棕色沉淀
溶液,生成无色气体,最终得到红棕色沉淀 。
。(1)上述6种离子中,该溶液肯定存在的为
(2)请设计实验检验原溶液中是否存在
 ,写出操作方法、现象及结论
,写出操作方法、现象及结论(3)生成无色气体
 的离子方程式为
的离子方程式为(4)步骤Ⅱ中发生反应的离子方程式为
您最近一年使用:0次



