1 . 下列叙述错误的是
A.分子组成上相差n个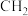 的有机物一定互为同系物 的有机物一定互为同系物 |
| B.水泥生产过程中加入适量石膏可调节水泥硬化速率 |
C.向 溶液中滴加稀硫酸,溶液变浑浊,说明非金属性: 溶液中滴加稀硫酸,溶液变浑浊,说明非金属性: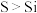 |
| D.石墨稀电阻率低,可用于生产超级电容器 |
您最近一年使用:0次
名校
2 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向 溶液中加入浓盐酸,产生的气体使紫色石蕊变红 溶液中加入浓盐酸,产生的气体使紫色石蕊变红 |  为酸性氧化物 为酸性氧化物 |
| B | 向CO还原 所得到的产物中加入稀盐酸,滴加KSCN溶液,溶液颜色不变红 所得到的产物中加入稀盐酸,滴加KSCN溶液,溶液颜色不变红 |  全部被还原 全部被还原 |
| C |  和KOH的混合溶液中加入铝粉并加热,管口湿润的红色石蕊试纸变蓝色 和KOH的混合溶液中加入铝粉并加热,管口湿润的红色石蕊试纸变蓝色 |  能被铝粉还原为 能被铝粉还原为 |
| D | 向 溶液中滴加盐酸,溶液变浑浊 溶液中滴加盐酸,溶液变浑浊 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列各组离子能在溶液中大量共存的是
A.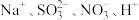 | B.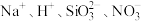 |
C. | D.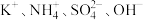 |
您最近一年使用:0次
4 . 无机非金属材料与人类社会的发展与进步息息相关,硅元素更是无机非金属材料的主角,地壳质量的90%以上是二氧化硅和硅酸盐。回答下列问题:
(1)硅元素在元素周期中的位置____________ 。
(2)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是_________ (填序号)。
①玻璃;②陶瓷;③石英玻璃;④硅芯片;⑤光导纤维;⑥水泥;⑦砖瓦
(3)盛装碱液的试剂瓶用橡胶塞而不用玻璃塞的原因是请用离子方程式来解释原因__________ 。
(4)实验室制取硅酸的方法是向硅酸钠溶液中加入稀盐酸,化学方程式为__________ 。
(5)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=___________ 。
(1)硅元素在元素周期中的位置
(2)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃;②陶瓷;③石英玻璃;④硅芯片;⑤光导纤维;⑥水泥;⑦砖瓦
(3)盛装碱液的试剂瓶用橡胶塞而不用玻璃塞的原因是请用离子方程式来解释原因
(4)实验室制取硅酸的方法是向硅酸钠溶液中加入稀盐酸,化学方程式为
(5)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=
您最近一年使用:0次
解题方法
5 . 下列离子方程式书写错误的是
A.SO2通入过量KOH中:2OH-+SO2= SO +H2O +H2O |
B.铜与足量稀硝酸反应:3Cu+8H++2NO =3Cu2++4H2O+2NO↑ =3Cu2++4H2O+2NO↑ |
C.向Na2SiO3溶液中滴加盐酸:SiO +2H+=H2SiO3↓ +2H+=H2SiO3↓ |
| D.FeS2与硫酸反应:FeS2+2H+= Fe2++H2S↑ |
您最近一年使用:0次
名校
6 . 普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,它是以纯碱、石灰石和石英砂(主要成分为SiO2)为原料,经混合,粉碎,在玻璃窑中熔融,发生复杂的物理变化和化学变化制得的。下列说法正确的是
| A.沸点:SiO2<Na2CO3 |
| B.SiO2的VSEPR模型与空间结构均为平面三角形 |
| C.Na2SiO3和CaCO3分别与足量的稀盐酸反应,反应后均无新的沉淀产生 |
| D.0.1 mol SiO2的质量为6 g |
您最近一年使用:0次
7 . 硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是________ 。
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为_______________ 。
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):_________________ 。
(4)当前制备高纯硅的主要生产过程示意图如下:_________________ 。
②高纯硅的用途:_____________ 。(写出一种)
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是_______________ 。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):
(4)当前制备高纯硅的主要生产过程示意图如下:

②高纯硅的用途:
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是
您最近一年使用:0次
8 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。请写出
)和硅酸盐的形式存在。请写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式___________ 。
(2)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:___________ 。
ⅱ.流程①焦炭体现了___________ (填“氧化性”或“还原性”)。
(3)氮化硅是一种新型陶瓷材料,可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得 ,请用单线桥表示该反应电子转移的方向与数目
,请用单线桥表示该反应电子转移的方向与数目___________ 。
(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,写出水玻璃和盐酸反应的离子方程式___________ 。
(5)关于硅及其相关化合物的叙述正确的是___________。
(1)硅元素在自然界中通常以石英石(
 )和硅酸盐的形式存在。请写出
)和硅酸盐的形式存在。请写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式(2)高纯硅单质可由石英砂(主要成分是
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示: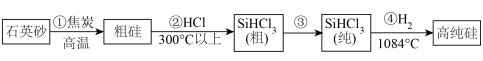
ⅱ.流程①焦炭体现了
(3)氮化硅是一种新型陶瓷材料,可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得
 ,请用单线桥表示该反应电子转移的方向与数目
,请用单线桥表示该反应电子转移的方向与数目(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,写出水玻璃和盐酸反应的离子方程式
(5)关于硅及其相关化合物的叙述正确的是___________。
A.已知 与 与 在同一主族,由于 在同一主族,由于 ,用类比法得知 ,用类比法得知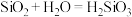 |
B.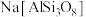 用氧化物形式表示为 用氧化物形式表示为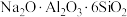 |
| C.硅元素在金属元素与非金属元素的分界线处,因此单质硅具有弱导电性,一般可用于作为半导体材料 |
| D.高温熔融纯碱时可选用石英玻璃坩埚 |
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写正确的是
A.向硫酸铜溶液中滴入氨水: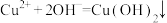 |
B.金属锌与浓硫酸共热: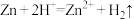 |
C.向硅酸钠溶液中通入少量 : : |
D.氧化钠与水反应: |
您最近一年使用:0次
10 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 90%以上。
(1)可用于制作计算机芯片的是___________ (填化学式,下同)可用于制作太阳能电池的是___________ ,光导纤维的主要成分是___________ 。
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:___________ 。
(4)高纯度单晶硅可以按下列方法制备: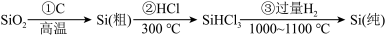
写出步骤①的化学方程式:___________ 。
(1)可用于制作计算机芯片的是
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(4)高纯度单晶硅可以按下列方法制备:
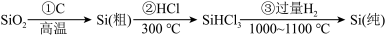
写出步骤①的化学方程式:
您最近一年使用:0次



