名校
解题方法
1 . 一些活泼金属也可作还原剂。下列金属不能通过铝热反应原理制取的是
| A.钠 | B.铁 | C.铜 | D.锌 |
您最近一年使用:0次
名校
解题方法
2 . 合理、高效利用金属矿物。将金属从其化合物中还原出来用于生产和制造各种金属材料,利用金属活动性的不同,可以采用不同的冶炼方法。
(1)以 为原料冶炼
为原料冶炼 ,冶炼方法是
,冶炼方法是_______ ,下列能用该方法制得的金属是_______ (填字母)。
A. B.
B. C.
C.
(2)明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(已知炉甘石的主要成分为碳酸锌)。下列说法不正确的是_______(填字母)。
(3)铝热法是冶炼金属的方法之一(如下图),写出铝热法炼铁的化学方程式_______ 。引发铝热反应的实验操作是_______ 。

(4)金属镁的冶炼有多种方法,其中一种以白云石(主要成分为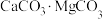 )为原料,经高温煅烧生成氧化物
)为原料,经高温煅烧生成氧化物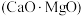 ,氧化物在还原炉中经
,氧化物在还原炉中经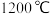 真空条件下用硅铁(硅铁含硅量达
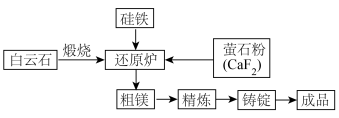
真空条件下用硅铁(硅铁含硅量达 )还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
)还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
①萤石粉作为活性剂,可增强冶炼过程中的打渣能力,用电子式表示 的形成过程
的形成过程_______ 。
②写出还原炉中高温下发生置换反应的化学方程式_______ 。
(1)以
 为原料冶炼
为原料冶炼 ,冶炼方法是
,冶炼方法是A.
 B.
B. C.
C.
(2)明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(已知炉甘石的主要成分为碳酸锌)。下列说法不正确的是_______(填字母)。
| A.煤炭中起作用的主要元素是碳 |
| B.该冶炼锌的方法属于热还原法 |
| C.倭铅是指金属锌和铅的混合物 |
D.冶炼 的反应方程式为 的反应方程式为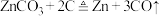 |
(3)铝热法是冶炼金属的方法之一(如下图),写出铝热法炼铁的化学方程式

(4)金属镁的冶炼有多种方法,其中一种以白云石(主要成分为
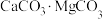 )为原料,经高温煅烧生成氧化物
)为原料,经高温煅烧生成氧化物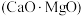 ,氧化物在还原炉中经
,氧化物在还原炉中经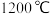 真空条件下用硅铁(硅铁含硅量达
真空条件下用硅铁(硅铁含硅量达 )还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
)还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
①萤石粉作为活性剂,可增强冶炼过程中的打渣能力,用电子式表示
 的形成过程
的形成过程②写出还原炉中高温下发生置换反应的化学方程式
您最近一年使用:0次
名校
3 . 物质集合 中含有常见物质
中含有常见物质 、
、 、
、 、
、 、
、 、
、 、
、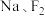 。这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
。这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
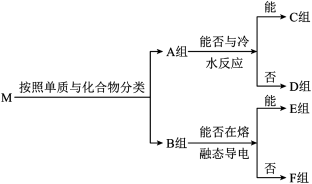
(1)B组物质中属于非电解质的为___________ 。
(2)C组物质中能与水反应生成还原性气体的化学方程式为___________ 。
(3)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:___________ 。
(4)请写出 组中的酸性氧化物与酸性
组中的酸性氧化物与酸性 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(5)在密闭容器中,将 组中的两种物质充分加热后排出气体,经测定,所得固体为纯净物,该纯净物的化学式为
组中的两种物质充分加热后排出气体,经测定,所得固体为纯净物,该纯净物的化学式为___________ 。
 中含有常见物质
中含有常见物质 、
、 、
、 、
、 、
、 、
、 、
、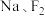 。这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
。这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
(1)B组物质中属于非电解质的为
(2)C组物质中能与水反应生成还原性气体的化学方程式为
(3)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:
(4)请写出
 组中的酸性氧化物与酸性
组中的酸性氧化物与酸性 溶液反应的离子方程式:
溶液反应的离子方程式:(5)在密闭容器中,将
 组中的两种物质充分加热后排出气体,经测定,所得固体为纯净物,该纯净物的化学式为
组中的两种物质充分加热后排出气体,经测定,所得固体为纯净物,该纯净物的化学式为
您最近一年使用:0次
名校
解题方法
4 . 下列方程式与所给事实不相符的是
| A.白醋可除去水壶中的水垢:2H++CaCO3=Ca2++CO2↑+H2O |
| B.湿润的淀粉碘化钾试纸遇氯气变蓝:Cl2+2I-=2Cl-+I2 |
C.铝粉和氧化铁组成的铝热剂用于焊接钢轨:2Al+Fe2O3 Al2O3+2Fe Al2O3+2Fe |
D.在煤中添加石灰石,降低尾气中SO2浓度:2CaCO3+2SO2+O2 2CaSO4+2CO2 2CaSO4+2CO2 |
您最近一年使用:0次
2024-01-05更新
|
164次组卷
|
2卷引用:北京市中国人民大学附属中学2021-2022学年高一下学期期末考试化学试题
名校
5 . 填空。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量___________ ,请用离子方程式表示除杂原理___________ 。
(2)下列属于氮的固定的是___________ (填序号)。
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①___________ ,③___________ 。
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:___________ 。
(4)检验 的离子方程式:
的离子方程式:___________ 。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量
(2)下列属于氮的固定的是
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:
(4)检验
 的离子方程式:
的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 根据如图所示的转化关系判断,下列说法正确的是(反应条件已略去)


A.生成等质量 时,①和②反应消耗 时,①和②反应消耗 |
B.反应③和④消耗等量的Al时,生成的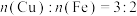 |
| C.反应③中氧化剂与还原剂的物质的量之比为2∶3 |
D.反应⑤的离子方程式为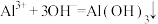 |
您最近一年使用:0次
2023-11-29更新
|
149次组卷
|
8卷引用:山西省怀仁市2021-2022学年期末调研高一上学期期末调研化学试题
7 . 铝是地壳中含量最多的金属元素,在自然界主要以化合态的形式存在于铝土矿中。铝土矿的主要成分是 ,此外还含有少量
,此外还含有少量 、
、 等杂质,如图是工业冶炼铝的流程:
等杂质,如图是工业冶炼铝的流程:
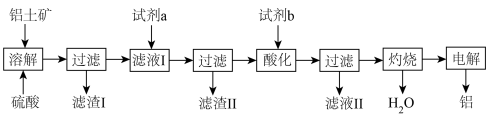
回答下列问题:
(1)为加速流程中的溶解,可采用的措施是___________ 。(答出1点即可)
(2)实际工业操作中,流程图中的试剂a和试剂b必须过量,试剂a为___________ ,试剂b为___________ 。
(3)若将溶解过程中的硫酸换成氢氧化钠并相应改变试剂a和试剂b亦可完成此流程,当用NaOH溶解铝土矿时滤渣Ⅰ的成分是___________ (写化学式,下同),滤渣Ⅱ的成分是___________ 。
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨,铝热剂高温下发生反应的化学方程式为___________ 。
(5)一次生产中,铝土矿中氧化铝的含量为50%,电解过程中的转化率为85%,其他操作过程没有铝的损失,那么2.00 t铝土矿可冶炼出金属铝___________ t。
 ,此外还含有少量
,此外还含有少量 、
、 等杂质,如图是工业冶炼铝的流程:
等杂质,如图是工业冶炼铝的流程:
回答下列问题:
(1)为加速流程中的溶解,可采用的措施是
(2)实际工业操作中,流程图中的试剂a和试剂b必须过量,试剂a为
(3)若将溶解过程中的硫酸换成氢氧化钠并相应改变试剂a和试剂b亦可完成此流程,当用NaOH溶解铝土矿时滤渣Ⅰ的成分是
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨,铝热剂高温下发生反应的化学方程式为
(5)一次生产中,铝土矿中氧化铝的含量为50%,电解过程中的转化率为85%,其他操作过程没有铝的损失,那么2.00 t铝土矿可冶炼出金属铝
您最近一年使用:0次
8 . 下列反应过程中的能量变化与图一致的是
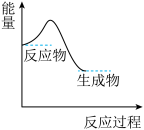

A.2H2O 2H2↑ + O2↑ 2H2↑ + O2↑ |
| B.在加热条件下氢气还原氧化铜 |
| C.胆矾受热分解 |
| D.铝热反应 |
您最近一年使用:0次
解题方法
9 . 化学创造美好生活。下列生产活动中,没有运用相应化学原理的是
选项 | 生产活动 | 化学原理 |
A | 利用冰箱储存食物 | 通过降低温度来减缓食物腐败速率 |
B | 利用氢氟酸刻蚀石英制作工艺品 | HF可与 发生反应 发生反应 |
C | 用铝热剂焊接钢铁 | 铝的金属活动性强于铁,反应放出大量热 |
D | 食用油脂为人体提供能量 | 油脂燃烧生成 和 和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 铁及其化合物在工业上用途广泛。部分含铁物质的分类与相应铁元素的化合价关系如图所示。回答下列问题:

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途______ 。
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为______ ,设计实验证明腐蚀后的废液中含有b的阳离子:______ 。
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的______ 性;在加热条件下二者可剧烈反应,c与足量浓硝酸在加热条件下反应的化学方程式为______ 。
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为______ 。若要制备0.2mol ,理论上需要
,理论上需要______ gNaClO。

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、
 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为 ,理论上需要
,理论上需要
您最近一年使用:0次



