“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。
(1)甲烷分子具有________________ 结构,其结构式是_________________ 。
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式________________________ ,该反应属于____________ (填反应类型)。
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:
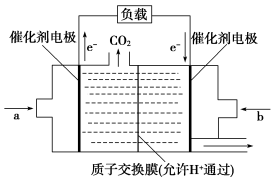
若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为________________________________ ;该电池工作过程中,H+的移动方向为从________ 到________ (填“左”或“右”)。
(1)甲烷分子具有
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:

若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为
更新时间:2020-07-07 14:49:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Ⅰ.在1×105Pa、298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能(已知氨分子中有三个等价的氮氢共价键):
(1)根据上表中的数据判断工业合成氨的反应是___________ (填“吸热”或“放热”)反应。
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为___________ kJ。
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小关系为___________ 。
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
Ⅱ.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是CH4-8e-+10OH-=CO +7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
+7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
(1)通入CH4的电极为___________ 极,发生___________ 反应。
(2)若将该电池中的燃料改为氢气,其正极反应式为O2+4e-+2H2O=4OH-,则其负极反应式为___________ 。
| 共价键 | H—H | N≡N | N—H |
| 键能(kJ·mol-1) | 436 | 945 | 391 |
(1)根据上表中的数据判断工业合成氨的反应是
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小关系为
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
Ⅱ.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是CH4-8e-+10OH-=CO
 +7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
+7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:(1)通入CH4的电极为
(2)若将该电池中的燃料改为氢气,其正极反应式为O2+4e-+2H2O=4OH-,则其负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是_______ (填“氧化”或“还原”)反应。
②写出NiO电极的电极反应式:___________________________________ 。
(2)下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:

请回答:①甲烷燃料电池负极反应式是_______________________________________ 。
②当线路中有0.1 mol电子通过时,________ (填“a”或“b”)极增重________ g。

①Pt电极上发生的是
②写出NiO电极的电极反应式:
(2)下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:

请回答:①甲烷燃料电池负极反应式是
②当线路中有0.1 mol电子通过时,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.已知常温下,AgCl的Ksp=1.8×10-10,AgBr的Ksp=4.9×10-13。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-)_________ (填“变大”、“变小”或“不变”,下同);
②若改加更多的AgCl固体,则c(Ag+)_________ ;
③若改加更多的KBr固体,则c(Ag+)_________ ,c(Cl-)_________ ;
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中正确的是___________________ ;
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,Ksp一定增大
B.两种难溶盐电解质,其中Ksp小的溶解度也一定小
C.难溶盐电解质的Ksp与温度有关
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变
Ⅱ.最近有人制造了一种燃料电池使汽油氧化直接产生电流,其中一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。回答下列问题:
(1)以辛烷为汽油的代表物,则这个电池放电时必发生反应的化学方程式是_______________ 。
(2)这个电池负极的电极反应式为C8H18+ 25O2--50e-==8CO2+ 9H2O,正极的电极反应式为______ 。固体电解质里O2-的移动方向是____ ,向外电路释放电子的电极是_______ 。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-)
②若改加更多的AgCl固体,则c(Ag+)
③若改加更多的KBr固体,则c(Ag+)
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中正确的是
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,Ksp一定增大
B.两种难溶盐电解质,其中Ksp小的溶解度也一定小
C.难溶盐电解质的Ksp与温度有关
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变
Ⅱ.最近有人制造了一种燃料电池使汽油氧化直接产生电流,其中一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。回答下列问题:
(1)以辛烷为汽油的代表物,则这个电池放电时必发生反应的化学方程式是
(2)这个电池负极的电极反应式为C8H18+ 25O2--50e-==8CO2+ 9H2O,正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲烷的分子结构模型如图所示:

根据甲烷的分子结构模型,回答问题:
(1)甲烷的电子式是__ ,其含义是__ 。
(2)甲烷的结构式是__ ,其含义是_ 。
(3)甲烷分子的空间构型是__ 。
(4)更能真实反映甲烷分子结构模型的是__ 。

根据甲烷的分子结构模型,回答问题:
(1)甲烷的电子式是
(2)甲烷的结构式是
(3)甲烷分子的空间构型是
(4)更能真实反映甲烷分子结构模型的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)某物质只含C、H、O三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
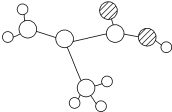
该分子中共平面的原子数最多为___________ (已知羧基的四个原子可以共平面)。
(2)甲烷与氯气的体积比为1∶1,光照条件下在如图所示的装置中反应,则得到的产物为
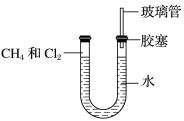
(3)甲烷最简单的同系物与氯气光照条件下反应,其生成物的化学式最多可能有
(4)经过几个小时的反应后,U形管右端的液面变化是
(5)下列事实中能证明甲烷分子是以碳原子为中心的正四面体结构的是
(1)某物质只含C、H、O三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。

该分子中共平面的原子数最多为
(2)甲烷与氯气的体积比为1∶1,光照条件下在如图所示的装置中反应,则得到的产物为

A. 、HCl 、HCl | B. 、HCl 、HCl |
C. 、 、 | D. 、 、 、 、 、 、 、 、 |
| A.5 | B.7 | C.9 | D.10 |
| A.升高 | B.降低 | C.不变 | D.无法确定 |
A. 只代表一种物质 只代表一种物质 | B. 只代表一种物质 只代表一种物质 |
C. 只代表一种物质 只代表一种物质 | D. 只代表一种物质 只代表一种物质 |
您最近一年使用:0次
【推荐1】(1)海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
①写出氯化镁的电子式__________________________
②重水的摩尔质量为____________________________
③写出金属镁的工业冶炼方程式_____________________ 
④海水淡化的常见方法有电渗析法、离子交换法、_________________
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是____________________________
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是________ (填选项)
A.沸点低 B.沸点高 C.易挥发 D.难挥发
③甲烷与氯气光照下反应生成产物共________ 种
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是__________________________
四、解答题
①写出氯化镁的电子式
②重水的摩尔质量为
③写出金属镁的工业冶炼方程式

④海水淡化的常见方法有电渗析法、离子交换法、
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是
A.沸点低 B.沸点高 C.易挥发 D.难挥发
③甲烷与氯气光照下反应生成产物共
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是
四、解答题
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题。
(1)甲烷与氯气的体积比为1∶1,光照条件下在如图所示的装置中反应,则得到的产物为___________ (填字母,下同)。

A. 、
、
B. 、
、
C. 、
、
D. 、
、 、
、 、
、 、
、
(2)甲烷最简单的同系物与氯气光照条件下反应,其生成物的化学式最多可能有___________ 种。
A.5 B.9 C.10 D.7
(3)经过几个小时的反应后,U形管右端的液面变化是___________ 。
A.升高 B.降低 C.不变 D.无法确定
(1)甲烷与氯气的体积比为1∶1,光照条件下在如图所示的装置中反应,则得到的产物为

A.
 、
、
B.
 、
、
C.
 、
、
D.
 、
、 、
、 、
、 、
、
(2)甲烷最简单的同系物与氯气光照条件下反应,其生成物的化学式最多可能有
A.5 B.9 C.10 D.7
(3)经过几个小时的反应后,U形管右端的液面变化是
A.升高 B.降低 C.不变 D.无法确定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
I.现有A、B、C、D四种烃,其结构模型如图:

(1)等质量的以上物质完全燃烧时耗去O2的量最多的是____ ;(填分子式,下同),生成CO2的量最多的是____ 。
(2)将1molA和适量的Cl2混合后光照,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为____ mol。
(3)将一定量的A和Cl2混合,光照条件下反应。请写出生成具有正四面体构型的有机产物的化学方程式:____ 。
(4)请你根据甲烷分子的结构推测,有机物D分子中的所有碳原子____ (填“一定”“可能”或“一定不”)在同一平面内。
II.电池在我们的生活中有着重要的应用,请回答下列问题:
(5)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH-向B电极定向移动,则B极的电极反应式为____ 。当消耗甲烷的体积为33.6L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为____ 。
(6)潜艇中使用的液氨液氧燃料电池工作原理如图所示:
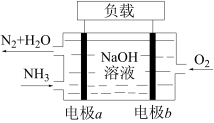
电极a名称是____ (填“正极”或“负极”),其电极反应为____ 。
I.现有A、B、C、D四种烃,其结构模型如图:

(1)等质量的以上物质完全燃烧时耗去O2的量最多的是
(2)将1molA和适量的Cl2混合后光照,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为
(3)将一定量的A和Cl2混合,光照条件下反应。请写出生成具有正四面体构型的有机产物的化学方程式:
(4)请你根据甲烷分子的结构推测,有机物D分子中的所有碳原子
II.电池在我们的生活中有着重要的应用,请回答下列问题:
(5)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH-向B电极定向移动,则B极的电极反应式为
(6)潜艇中使用的液氨液氧燃料电池工作原理如图所示:

电极a名称是
您最近一年使用:0次




