央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊进入患者腹中。明胶是水溶性蛋白质混合物,溶于水形成胶体。由工业明胶制成的胶囊往往含有超标的重金属Cr,从而对人体造成伤害。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是______ 价。已知铬的化合物常见有Cr2(SO4)3和NaCrO2,则Cr2O3属于______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”)。区别明胶的水溶液和K2SO4溶液的方法是_____ ,明胶的水溶液和K2SO4溶液共同具备的性质是______ (填序号)
a.都不稳定,密封放置沉淀 b.两者均有丁达尔现象 c.分散质粒子可通过滤纸
(2)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方式:_______ 。
②(CN)2和NaOH溶液反应的离子方程式:______ 。
(3)已知H2O2是二元弱酸、请写出H2O2与NaOH溶液反应生成酸式盐的化学式________ 。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
a.都不稳定,密封放置沉淀 b.两者均有丁达尔现象 c.分散质粒子可通过滤纸
(2)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方式:
②(CN)2和NaOH溶液反应的离子方程式:
(3)已知H2O2是二元弱酸、请写出H2O2与NaOH溶液反应生成酸式盐的化学式
20-21高三上·河南平顶山·阶段练习 查看更多[2]
更新时间:2020-09-08 16:11:02
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请对下列化合物:①NaCl、②HCl、③CaCl2、④CuO、⑤H2O、⑥Fe2O3进行分类:
(1)依据通常状况下物质的____ 为标准分类,属于固体的是_____ (填序号,下同),属于液体的是_____ 。
(2)依据以物质的____ 为标准分类,属于酸的是____ (填序号,下同),属于盐的是____ ,属于氧化物的是_____ 。
(1)依据通常状况下物质的
(2)依据以物质的
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代的。某化学兴趣小组对下列四组物质进行研究:
A.HCl、H2SO4、H2CO3、HNO3
B.Na2CO3、NaNO3、AgNO3、Ba(NO3)2
C.FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe(OH)3胶体
D.NaOH、KOH、Ba(OH)2、Fe2O3
(1)填写下列空白:
(2)写出(1)表中“不属于该类别的物质”发生反应的化学方程式。
A+B→气体:____ ;A+D:____ 。
(3)写出下列反应的离子方程式
①稀H2SO4与NaHCO3溶液的离子方程式:____ 。
②CuSO4溶液和Ba(OH)2溶液混合,其离子方程式为____ 。
③Fe和稀盐酸反应的离子方程式____ 。
④写出氢氧化钠溶液与碳酸氢钠溶液的离子方程式:____ 。
A.HCl、H2SO4、H2CO3、HNO3
B.Na2CO3、NaNO3、AgNO3、Ba(NO3)2
C.FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe(OH)3胶体
D.NaOH、KOH、Ba(OH)2、Fe2O3
(1)填写下列空白:
| A组 | B组 | C组 | D组 | |
| 分类标准 | 含氧酸 | ② | 分散系 | ④ |
| 不属于该类别的物质 | ① | Na2CO3 | ③ | Fe2O3 |
(2)写出(1)表中“不属于该类别的物质”发生反应的化学方程式。
A+B→气体:
(3)写出下列反应的离子方程式
①稀H2SO4与NaHCO3溶液的离子方程式:
②CuSO4溶液和Ba(OH)2溶液混合,其离子方程式为
③Fe和稀盐酸反应的离子方程式
④写出氢氧化钠溶液与碳酸氢钠溶液的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.化合物可以分为电解质和非电解质;根据电解质在水溶液中电离的程度,又可以分为强电解质和弱电解质。反应前有离子参加或反应后有离子生成的反应称为离子反应。
(1)下列物质中既属于无机物,又属于碱的是___________
(2)下列物质中,导电性能最差的是___________
(3)下列物质中,属于电解质的是___________
(4)下列各组离子反应可用 表示的是___________
表示的是___________
(5)某化学兴趣小组在课外活动中,对某碱性 、无色溶液 进行了多次检测,其中四次检测结果如下表所示:
组长一眼看出检测结果中第___________ 次和第___________ 次检测结果肯定不正确。
Ⅱ.某学习小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。
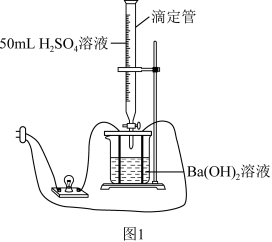
(6)溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察灯泡的亮度,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。反应的离子方程式为___________ 。
(7)整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图2中的___________ (填“a”、“b”、“c”或“d”序号)曲线表示。

(8)已知: 难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为:
难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为: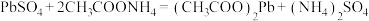 。试分析该复分解反应发生的原因
。试分析该复分解反应发生的原因___________ 。
(1)下列物质中既属于无机物,又属于碱的是___________
A. | B. | C. | D. |
(2)下列物质中,导电性能最差的是___________
| A.熔融的氢氧化钠 | B.石墨棒 | C.盐酸溶液 | D.固态氯化钾 |
(3)下列物质中,属于电解质的是___________
A. | B. | C. | D.NaOH溶液 |
(4)下列各组离子反应可用
 表示的是___________
表示的是___________| A.氢氧化钡和硫酸 | B.氢氧化铁和盐酸 | C.硝酸和氢氧化钠 | D.碳酸氢钠和氢氧化钠 |
(5)某化学兴趣小组在课外活动中,对某
| 检测次数 | 溶液中检测出的离子 |
| 第一次 |  、 、 、 、 、 、 |
| 第二次 |  、 、 、 、 、 、 |
| 第三次 |  、 、 、 、 、 、 |
| 第四次 |  、 、 、 、 、 、 |
Ⅱ.某学习小组为证实
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。
(6)溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察灯泡的亮度,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。反应的离子方程式为
(7)整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图2中的

(8)已知:
 难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为:
难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为: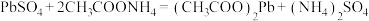 。试分析该复分解反应发生的原因
。试分析该复分解反应发生的原因
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某课外活动小组进行 胶体的制备实验并检验其性质。
胶体的制备实验并检验其性质。
(1)向煮沸的蒸馏水中逐滴加入饱和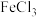 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体,制取
胶体,制取 胶体的离子方程式为
胶体的离子方程式为_______ 。
(2)向所得 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为_______ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式_______ 。
(3)欲除去 胶体中混有的NaCl,操作名称是
胶体中混有的NaCl,操作名称是_______ 。
(4) 胶体区别于
胶体区别于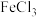 溶液最本质的特征是_______。
溶液最本质的特征是_______。
 胶体的制备实验并检验其性质。
胶体的制备实验并检验其性质。(1)向煮沸的蒸馏水中逐滴加入饱和
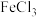 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体,制取
胶体,制取 胶体的离子方程式为
胶体的离子方程式为(2)向所得
 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为(3)欲除去
 胶体中混有的NaCl,操作名称是
胶体中混有的NaCl,操作名称是(4)
 胶体区别于
胶体区别于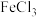 溶液最本质的特征是_______。
溶液最本质的特征是_______。A. 胶体粒子的直径在1~100nm之间 胶体粒子的直径在1~100nm之间 | B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 | D. 胶体的分散质能透过滤纸 胶体的分散质能透过滤纸 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在生产生活中有十分广泛的应用。铁的部分化合物的相互转化关系如框图所示,请回答相关问题。
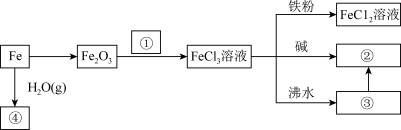
(1)图中①②③代表的物质所属不同分散系,③代表的物质所属的分散系名称是_______ ;
(2)写出生成④的化学反应方程式_______ ;
(3)写出 与①反应的离子方程式
与①反应的离子方程式_______ 。
(4)已知: 与铁粉反应生成
与铁粉反应生成 ,该反应中的氧化剂是
,该反应中的氧化剂是_______ 。若要实现 转化为
转化为 ,可以选用稀硫酸酸化的
,可以选用稀硫酸酸化的 溶液,请写出该反应的离子方程式
溶液,请写出该反应的离子方程式_______ 。

(1)图中①②③代表的物质所属不同分散系,③代表的物质所属的分散系名称是
(2)写出生成④的化学反应方程式
(3)写出
 与①反应的离子方程式
与①反应的离子方程式(4)已知:
 与铁粉反应生成
与铁粉反应生成 ,该反应中的氧化剂是
,该反应中的氧化剂是 转化为
转化为 ,可以选用稀硫酸酸化的
,可以选用稀硫酸酸化的 溶液,请写出该反应的离子方程式
溶液,请写出该反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是______________ (填序号)。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:________________ 。
(3)怎样证明制得的物质是胶体?请简述操作过程:__________________ 。
(4)取少量制得的胶体加入试管中,再加入少量(NH4)2SO4溶液,观察到的现象是__________ , 这种现象称为胶体的________________ 。
(5)Fe(OH)3胶体能稳定存在的主要原因是________ (填序号)。
A. 胶粒直径小于1nm B. 胶粒带正电荷
C. 胶粒作布朗运动 D . 胶粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________ (填序号)。
A. Fe(OH)3胶体粒子的直径在1~100nm之间
B. Fe(OH)3胶体具有丁达尔效应
C. Fe(OH)3胶体是均一的分散系
D. Fe(OH)3胶体的分散质粒子能透过滤纸
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:
(3)怎样证明制得的物质是胶体?请简述操作过程:
(4)取少量制得的胶体加入试管中,再加入少量(NH4)2SO4溶液,观察到的现象是
(5)Fe(OH)3胶体能稳定存在的主要原因是
A. 胶粒直径小于1nm B. 胶粒带正电荷
C. 胶粒作布朗运动 D . 胶粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A. Fe(OH)3胶体粒子的直径在1~100nm之间
B. Fe(OH)3胶体具有丁达尔效应
C. Fe(OH)3胶体是均一的分散系
D. Fe(OH)3胶体的分散质粒子能透过滤纸
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列填空:
现有物质①铜、②干冰、③盐酸、④液态硫酸、⑤蔗糖、⑥ 固体、⑦红褐色的氢氧化铁胶体、⑧熔融的
固体、⑦红褐色的氢氧化铁胶体、⑧熔融的 。
。
(1)属于分散系的是___________ (填写序号,下同);能够导电的是___________ ;写出属于酸式盐的物质溶于水后的电离方程式:___________
(2)⑦区别于其他分散系的本质特征为___________ ,利用___________ 效应可区分胶体和溶液。
(3) 溶液和⑥的溶液反应的离子方程式为
溶液和⑥的溶液反应的离子方程式为___________ 。
现有物质①铜、②干冰、③盐酸、④液态硫酸、⑤蔗糖、⑥
 固体、⑦红褐色的氢氧化铁胶体、⑧熔融的
固体、⑦红褐色的氢氧化铁胶体、⑧熔融的 。
。(1)属于分散系的是
(2)⑦区别于其他分散系的本质特征为
(3)
 溶液和⑥的溶液反应的离子方程式为
溶液和⑥的溶液反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式______ 。
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是______ (填字母序号)。
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为______ 。
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+ 2KI = 2FeCl2+ I2+2KI,在上式上用双线桥法标出该反应电子转移的方向和数目_____ 。向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为______ 色,再将混合液倒入______ (填仪器名称)中,将两层液体分离。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+ 2KI = 2FeCl2+ I2+2KI,在上式上用双线桥法标出该反应电子转移的方向和数目
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤Ba(OH)2,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4,⑨碳酸钙,⑩乙醇
(1)上述物质中属于电解质的有_______ ,属于非电解质的有_____ (填序号)。
(2)向⑥中逐渐滴加④的溶液,看到的现象是_______ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为____ 。
(4)⑧在水中的电离方程式为________ 。
(5)⑨和⑦混合,反应的离子方程式为_____ 。
(1)上述物质中属于电解质的有
(2)向⑥中逐渐滴加④的溶液,看到的现象是
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(4)⑧在水中的电离方程式为
(5)⑨和⑦混合,反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】IBr、ICl等称之为卤素互化物,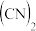 、
、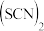 、
、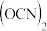 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应
,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。
 溴化碘
溴化碘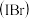 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为___ 。
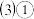 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_______________ 。
 下列物质中,也可以使该溶液红色褪去的是
下列物质中,也可以使该溶液红色褪去的是 _________ 。
A.新制氯水 碘水
碘水 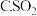
 盐酸
盐酸
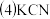 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为_______________ 。
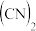 、
、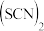 、
、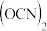 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。 氯化碘
氯化碘 能与水发生反应:
能与水发生反应: ,该反应
,该反应 填“是”或“不是”
填“是”或“不是” 氧化还原反应。
氧化还原反应。 溴化碘
溴化碘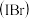 具有强氧化性,能与
具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为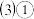 已知某些离子的还原性强弱顺序为
已知某些离子的还原性强弱顺序为 。现将几滴KSCN溶液滴入到含少量
。现将几滴KSCN溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象 下列物质中,也可以使该溶液红色褪去的是
下列物质中,也可以使该溶液红色褪去的是 A.新制氯水
 碘水
碘水 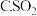
 盐酸
盐酸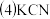 为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将
为剧毒物质,处理含有KCN的废水常用的方法是:在碱性条件下用NaClO溶液将 氧化为
氧化为 和一种单质气体,该反应的离子方程式为
和一种单质气体,该反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】氰 的结构简式为
的结构简式为 ,其化学性质与卤素
,其化学性质与卤素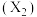 很相似,化学上称之为拟卤素,其氧化性介于
很相似,化学上称之为拟卤素,其氧化性介于 和
和 之间。
之间。
(1)写出 的电子式:
的电子式:_______ 。
(2)写出 在常温下与烧碱溶液反应的化学方程式:
在常温下与烧碱溶液反应的化学方程式:_______ 。
(3)在 的混合溶液中通入少量氯气,发生反应的离子方程式为
的混合溶液中通入少量氯气,发生反应的离子方程式为_______ 。
 的结构简式为
的结构简式为 ,其化学性质与卤素
,其化学性质与卤素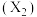 很相似,化学上称之为拟卤素,其氧化性介于
很相似,化学上称之为拟卤素,其氧化性介于 和
和 之间。
之间。(1)写出
 的电子式:
的电子式:(2)写出
 在常温下与烧碱溶液反应的化学方程式:
在常温下与烧碱溶液反应的化学方程式:(3)在
 的混合溶液中通入少量氯气,发生反应的离子方程式为
的混合溶液中通入少量氯气,发生反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列填空:
(1)画出 O2﹣结构示意图:_____ ,某种核素质量数 37,中子数 20,其原子符号:_____
(2)现有以下物质:①NaCl溶液;②液态HCl;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;
⑥液氨;⑦冰醋酸;⑧石墨.
其中:属于电解质且能导电的是_____
(3)氰(CN)2 的化学性质和卤素(X2,如 Cl2)很相似,化学上称为拟卤素.试写出(CN)2与水反应的化学方程式:_____
(4)钠是一种非常活泼的金属,能与水反应,若把一小块钠投入 CuSO4 溶液中,会产生蓝色沉淀,试写出 该反应的化学方程式_____ .
(1)画出 O2﹣结构示意图:
(2)现有以下物质:①NaCl溶液;②液态HCl;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;
⑥液氨;⑦冰醋酸;⑧石墨.
其中:属于电解质且能导电的是
(3)氰(CN)2 的化学性质和卤素(X2,如 Cl2)很相似,化学上称为拟卤素.试写出(CN)2与水反应的化学方程式:
(4)钠是一种非常活泼的金属,能与水反应,若把一小块钠投入 CuSO4 溶液中,会产生蓝色沉淀,试写出 该反应的化学方程式
您最近半年使用:0次



