请回答下列问题:
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi—O键。某些化学键键能数据如下:
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方程式:___ 。
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:___ 。
(1)已知1molSi固体中有2molSi—Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi—O键。某些化学键键能数据如下:
| 化学键 | Si—O | Si—Si | O=O |
| 键能(kJ·mol-1) | 460 | 176 | 498 |
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方程式:
(2)肼(N2H4)通常作为火箭的燃料。已知3.2g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式:
更新时间:2020-12-05 14:07:25
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】依据叙述,写出下列反应的热化学方程式。
(1)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有4NA个电子转移时,放出450 kJ的热量。其热化学方程式为______________________ 。
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、395 kJ、940 kJ,则N2与H2反应生成NH3的热化学方程式为____________________________ 。
(3)钛(Ti)被称为继铁、铝之后的第三金属,已知由金红石(TiO2)制取单质Ti,涉及的步骤为:
已知:①C(s)+O2(g) CO2(g); ΔH=-395.5 kJ·mol-1
CO2(g); ΔH=-395.5 kJ·mol-1
②2CO(g)+O2(g) 2CO2(g); ΔH=-560 kJ·mol-1
2CO2(g); ΔH=-560 kJ·mol-1
③TiO2(s)+2Cl2(g)+2C(s) TiCl4(s)+2CO(g)的ΔH=―80kJ/mol
TiCl4(s)+2CO(g)的ΔH=―80kJ/mol
则TiO2(s)与Cl2(g)反应的热化学方程式为______________________________ 。
(1)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有4NA个电子转移时,放出450 kJ的热量。其热化学方程式为
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、395 kJ、940 kJ,则N2与H2反应生成NH3的热化学方程式为
(3)钛(Ti)被称为继铁、铝之后的第三金属,已知由金红石(TiO2)制取单质Ti,涉及的步骤为:

已知:①C(s)+O2(g)
 CO2(g); ΔH=-395.5 kJ·mol-1
CO2(g); ΔH=-395.5 kJ·mol-1②2CO(g)+O2(g)
 2CO2(g); ΔH=-560 kJ·mol-1
2CO2(g); ΔH=-560 kJ·mol-1③TiO2(s)+2Cl2(g)+2C(s)
 TiCl4(s)+2CO(g)的ΔH=―80kJ/mol
TiCl4(s)+2CO(g)的ΔH=―80kJ/mol则TiO2(s)与Cl2(g)反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为______________ ;
②该反应的热化学方程式为________________________________ ;
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=____________ kJ·mol-1;
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
(3)倒入NaOH溶液的正确操作是_______________ (从下列选出)。
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_________ (从下列选出)
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=______________ (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是:___________ 。(任意写出一点)
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为
②该反应的热化学方程式为
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
(3)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(4)使硫酸与NaOH溶液混合均匀的正确操作是
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒搅拌棒轻轻地搅动
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
| 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | |||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】热值是指一定条件下单位质量的物质完全燃烧所放出的热量。已知H2(g)、CO(g)和CH3OH(l)的热值分别为143 kJ· g-1、10 kJ·g-1和23 kJ·g-1。请回答下列问题:
(1)写出CO燃烧反应的热化学方程式为__________________________________________ 。
(2)表示甲醇燃烧热的热化学方程式为__________________________________________ 。
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________________________ 。
(4)白磷与氧可发生如下反应:P4(g)+5O2(g) P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热
P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热_____________ 。
(1)写出CO燃烧反应的热化学方程式为
(2)表示甲醇燃烧热的热化学方程式为
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(4)白磷与氧可发生如下反应:P4(g)+5O2(g)
 P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热
P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一个化学反应,我们不但要关心物质变化,还要研究能量变化和反应快慢。
(1)下面是一个由天然气和水反应制备氢气的反应,其方程式为:CH4(g)+ 2H2O(g) CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为
CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为______ 反应(填“吸热”或“放热”),

若已知,破坏1mol化学键需要吸收的热量如下表所示:则该反应吸收或放出热量为______ kJ (用含a b c d字母的代数式表示)。
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为________ ;X为__________ 。若反应经2min达到平衡,平衡时C的浓度______ 0.8mol/L(填“大于”,“小于”或“等于”)。若已知达平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0。请用p0、p来表示达平衡时反应物A的转化率为__________ 。
(1)下面是一个由天然气和水反应制备氢气的反应,其方程式为:CH4(g)+ 2H2O(g)
 CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为
CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为
若已知,破坏1mol化学键需要吸收的热量如下表所示:则该反应吸收或放出热量为
化学键 | C—H | O—H | C=O | H—H |
吸收热量(kJ/mol) | a | b | c | d |
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式___________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为___________ 。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 减排能有效降低温室效应,同时
减排能有效降低温室效应,同时 也是一种重要的资源,因此
也是一种重要的资源,因此 捕集与转化技术研究备受关注。
捕集与转化技术研究备受关注。
Ⅰ. 催化加氢制甲醇
催化加氢制甲醇
(1)已知:

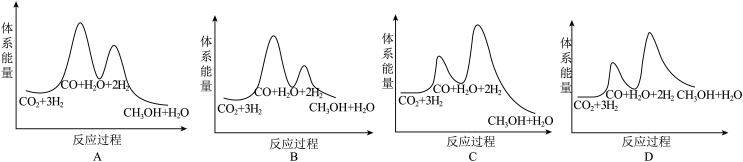
则 催化加氢制甲醇的热化学方程式为
催化加氢制甲醇的热化学方程式为_________ 。若反应①为慢反应,下列图中能体现上述能量变化的是_________ 。
Ⅱ.离子液体聚合物捕集
(2)已知离子液体聚合物在不同温度和不同 流速下,
流速下, 吸附容量随时间的变化如图1和图2.结合图1和图2分析:
吸附容量随时间的变化如图1和图2.结合图1和图2分析:

①离子液体聚合物捕集 的反应为
的反应为_________ (填“吸热”或“放热”)反应。
②离子液体聚合物捕集 的有利条件为
的有利条件为___________ 。
Ⅲ.研究建立的一种二氧化碳新循环体系
(3)过程Ⅰ的原理: ,根据下表数据回答:
,根据下表数据回答:
①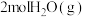 完全分解需
完全分解需_________ (填“放出”或“吸收”)能量_________  。
。
②能正确表示该过程能量变化的示意图是_________ 。
A.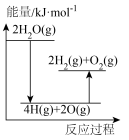 B.
B.
C.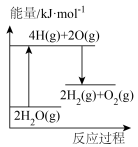 D.
D.
 减排能有效降低温室效应,同时
减排能有效降低温室效应,同时 也是一种重要的资源,因此
也是一种重要的资源,因此 捕集与转化技术研究备受关注。
捕集与转化技术研究备受关注。Ⅰ.
 催化加氢制甲醇
催化加氢制甲醇(1)已知:


则
 催化加氢制甲醇的热化学方程式为
催化加氢制甲醇的热化学方程式为
Ⅱ.离子液体聚合物捕集

(2)已知离子液体聚合物在不同温度和不同
 流速下,
流速下, 吸附容量随时间的变化如图1和图2.结合图1和图2分析:
吸附容量随时间的变化如图1和图2.结合图1和图2分析:
①离子液体聚合物捕集
 的反应为
的反应为②离子液体聚合物捕集
 的有利条件为
的有利条件为Ⅲ.研究建立的一种二氧化碳新循环体系
(3)过程Ⅰ的原理:
 ,根据下表数据回答:
,根据下表数据回答:| 化学键 |  |  |  |
键能 | 436 | 496 | 463 |
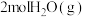 完全分解需
完全分解需 。
。②能正确表示该过程能量变化的示意图是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次



