(1)下列物质:①Fe ② Br2 ③Na2O ④CO ⑤CO2 ⑥SO3 ⑦NH3 ⑧H2S ⑨HCl ⑩H2SO4 ⑪Ba(OH)2 ⑫NaCl ⑬蔗糖 ⑭NaCl溶液。属于电解质的是___________ , 属于非电解质的是 ___________ ,能导电的是___________ 。
(2)写出下列物质在水中的电离方程式或离子方程式: NaHSO4 :___________ , H2SO4 :___________ , H2SO4+ Fe:___________ , Ba(OH)2 + H2SO4:___________ 。
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现___________ ,原因:___________ ,随后___________ ,原因(用离子方程式表示) ___________ 。
(2)写出下列物质在水中的电离方程式或离子方程式: NaHSO4 :
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现
更新时间:2020-12-16 21:40:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】为了认识和研究的方便,对于数以万计的物质,人们常根据物质的组成、结构和性质或用途进行分类,运用分类法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。就下列所列物质,按要求回答问题:①食盐②食醋③氯化钠固体④BaSO4固体⑤纯CH3COOH⑥KHSO4⑦Ba(OH)2⑧熔融Na2O⑨CO2⑩次氯酸HClO⑪乙醇⑫HNO3⑬CuSO4•5H2O⑭Cu(NO3)2溶液⑮Cu⑯Fe(OH)3胶体。
(1)以上物质能导电的有____ (填序号),以上物质属于强电解质的有____ (填序号),以上物质属于一元酸的有____ (填序号)。
(2)写出⑥在熔融状态的电离方程式:____ 。
(3)写出NaHCO3在水溶液条件下的电离方程式:____ 。
(4)上述物质有两种物质在水溶液中发生反应,其中离子方程式为H++OH-=H2O,则该反应的化学方程式为____ 。
(5)实验室制备⑯的方法是____ ,发生的反应方程式____ ,鉴别制备成功的最简单的方法是____ 。
(1)以上物质能导电的有
(2)写出⑥在熔融状态的电离方程式:
(3)写出NaHCO3在水溶液条件下的电离方程式:
(4)上述物质有两种物质在水溶液中发生反应,其中离子方程式为H++OH-=H2O,则该反应的化学方程式为
(5)实验室制备⑯的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答以下问题:
(1)下列描述的分别是胶体的性质或现象,按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔现象 D.胶体的稳定性
①用激光鉴别胶体和溶液,利用的胶体性质是____ (填字母)。
②工厂采用高压静电除尘,利用的胶体性质是_____ (填字母)。
(2)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,是一元弱酸,NaH2PO2属于____ (正盐、酸式盐、碱式盐),写出NaH2PO2的电离方程式____ 。
(3)已知:氧化性Cl2>Fe3+>I2,请写出过量Cl2通入到FeI2溶液中的化学方程式____ 。
(1)下列描述的分别是胶体的性质或现象,按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔现象 D.胶体的稳定性
①用激光鉴别胶体和溶液,利用的胶体性质是
②工厂采用高压静电除尘,利用的胶体性质是
(2)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,是一元弱酸,NaH2PO2属于
(3)已知:氧化性Cl2>Fe3+>I2,请写出过量Cl2通入到FeI2溶液中的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)往Fe(OH)3胶体中逐滴加入过量的3mol/L硫酸产生的现象是_________ 。
(2)现在有下列10种物质:① H2O ②空气 ③Mg ④ NH3 ⑤ 稀H2SO4⑥ Ca(OH)2 ⑦CuSO4 ·5 H2O ⑧碘酒⑨无水乙醇⑩NaHCO3其中,⑤在水溶液中的电离方程式为______ ,属于电解质的是__________ (填序号,下同);属于非电解质的是__________ ;属于既不是电解质也不是非电解质的是__________ 。
(2)现在有下列10种物质:① H2O ②空气 ③Mg ④ NH3 ⑤ 稀H2SO4⑥ Ca(OH)2 ⑦CuSO4 ·5 H2O ⑧碘酒⑨无水乙醇⑩NaHCO3其中,⑤在水溶液中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】利用分类法可系统、全面认识物质的性质
现有下列十种物质:①液态HCl ② ③NaCl溶液 ④
③NaCl溶液 ④ ⑤蔗糖晶体 ⑥
⑤蔗糖晶体 ⑥ ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩
⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩
(1)上述物质中属于电解质的是___________ ;属于非电解质的是___________ 能导电的是___________ (填序号)。
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为: ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)②在水中的电离方程式为___________ 。
(4)向⑦的溶液中逐渐滴加①的溶液,看到的现象是___________
(5)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打( ),能治疗胃酸过多,请写出其反应的离子方程式
),能治疗胃酸过多,请写出其反应的离子方程式___________ ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含 的胃药(如胃舒平),它与胃酸反应的离子方程式
的胃药(如胃舒平),它与胃酸反应的离子方程式___________ 。
现有下列十种物质:①液态HCl ②
 ③NaCl溶液 ④
③NaCl溶液 ④ ⑤蔗糖晶体 ⑥
⑤蔗糖晶体 ⑥ ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩
⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨空气 ⑩
(1)上述物质中属于电解质的是
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:
 ,该反应的化学方程式为
,该反应的化学方程式为(3)②在水中的电离方程式为
(4)向⑦的溶液中逐渐滴加①的溶液,看到的现象是
(5)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(
 ),能治疗胃酸过多,请写出其反应的离子方程式
),能治疗胃酸过多,请写出其反应的离子方程式 的胃药(如胃舒平),它与胃酸反应的离子方程式
的胃药(如胃舒平),它与胃酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酸钠 是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下;
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下;
________ ________
________ ________=________
________=________ ________
________ ________
________ ________
________ ________
________
(1)补充并配平该化学方程式______ (若系数为1,请标注“1”)。
(2)从物质分类角度来看, 是
是________ (填字母)。
a.酸 b.酸式盐 c.碱 d.非电解质
e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是________ 。
(4)下列方法不能用来区分固体 和NaCl的是________(填字母)。
和NaCl的是________(填字母)。
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列________(填字母)反应中
表现出的性质与下列________(填字母)反应中 表现出的性质相同。
表现出的性质相同。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学方程式,并用单线桥表示其电子转移的方向和数目:________ 。
 是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下;
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下;________
 ________
________ ________=________
________=________ ________
________ ________
________ ________
________ ________
________
(1)补充并配平该化学方程式
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质
e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是(4)下列方法不能用来区分固体
 和NaCl的是________(填字母)。
和NaCl的是________(填字母)。| A.分别溶于水 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列________(填字母)反应中
表现出的性质与下列________(填字母)反应中 表现出的性质相同。
表现出的性质相同。A. |
B. |
C.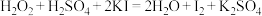 |
D.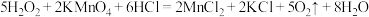 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔融的K2SO4 ⑨纯水。请回答下列问题(用序号):
以上物质中能导电的是___________ 属于电解质的是___________ 属于非电解质的是___________
(2)配平下列氧化还原反应的化学方程式___________ 、___________
KClO3+_______HCl(浓) = ______KCl+_____ClO2↑+_____Cl2↑+_______H2O
MnO +_______H2O2+________H+ = ________Mn2++______O2↑+______H2O
+_______H2O2+________H+ = ________Mn2++______O2↑+______H2O
(3)NaHSO4和Ba(OH)2两溶液混合,反应后成中性时的离子方程式为___________
(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔融的K2SO4 ⑨纯水。请回答下列问题(用序号):
以上物质中能导电的是
(2)配平下列氧化还原反应的化学方程式
KClO3+_______HCl(浓) = ______KCl+_____ClO2↑+_____Cl2↑+_______H2O
MnO
 +_______H2O2+________H+ = ________Mn2++______O2↑+______H2O
+_______H2O2+________H+ = ________Mn2++______O2↑+______H2O(3)NaHSO4和Ba(OH)2两溶液混合,反应后成中性时的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:①氮气 ②液态CO2 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔融的KNO3 ⑨NaOH溶液,请回答下列问题(填序号):
(1)以上物质能导电的是_______ 。
(2)以上物质中属于电解质的是_______ 。
(1)以上物质能导电的是
(2)以上物质中属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有如下物质:①铜;②NaOH溶液;③ 固体;④
固体;④ ;⑤酒精;⑥蒸馏水;⑦
;⑤酒精;⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体
(1)以上物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是_______ 。
(3)将②与⑦进行混合,该过程中发生的离子反应方程式是_______ 。
(4)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为_______ 。
 固体;④
固体;④ ;⑤酒精;⑥蒸馏水;⑦
;⑤酒精;⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体(1)以上物质中,属于电解质的是
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是
(3)将②与⑦进行混合,该过程中发生的离子反应方程式是
(4)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有下列10种物质:①液态HCl,②NH4Cl,③蔗糖,④Cl2,⑤NaOH溶液,⑥熔融碳酸钠,⑦碳酸氢钠固体,⑧淀粉,⑨CaO,⑩H2O。回答下列问题:
(1)上述物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,在上述状态下能够导电的是_______ 。
(2)写出⑤和⑦反应的离子方程式:_______ 。
(3)在酒精灯火焰上灼烧,火焰呈黄色的,为_______ 。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:_______ 。
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是_______ ,化学方程式为_______ 。
(1)上述物质中,属于电解质的是
(2)写出⑤和⑦反应的离子方程式:
(3)在酒精灯火焰上灼烧,火焰呈黄色的,为
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有以下几种物质(或微粒):
① 丝 ②
丝 ② ③
③ ④液态
④液态 ⑤稀
⑤稀 ⑥熔融
⑥熔融 ⑦
⑦ 溶液 ⑧饱和
溶液 ⑧饱和 溶液 ⑨消毒酒精
溶液 ⑨消毒酒精
回答下列问题:
(1)②和③之间互为__________ 。
(2)以上物质中属于能导电的电解质是__________ 。(填代号)
(3)⑤中溶质的电离方程式为__________ 。
(4)利用⑧制备 胶体的操作方法是
胶体的操作方法是__________ 。(用文字描述)
(5)向⑤中逐渐加入 固体,其溶液的导电性变化情况是
固体,其溶液的导电性变化情况是__________ 。
(6)根据酸能电离出 的数目可将酸分为一元酸(如
的数目可将酸分为一元酸(如 )、二元酸(如
)、二元酸(如 )、三元酸(如
)、三元酸(如 )。二元酸能与碱反应生成一种正盐(如
)。二元酸能与碱反应生成一种正盐(如 )和一种酸式盐(如
)和一种酸式盐(如 ),三元酸能与碱反应生成一种正盐(如
),三元酸能与碱反应生成一种正盐(如 )和两种酸式盐(如
)和两种酸式盐(如 、
、 )。
)。
① 属于二元酸,写出它与
属于二元酸,写出它与 反应生成酸式盐的化学方程式
反应生成酸式盐的化学方程式__________ ;
② 与
与 溶液反应生成的酸式盐只有一种,则
溶液反应生成的酸式盐只有一种,则 是
是__________ 元酸;若反应生成正盐,则该正盐的化学式为__________ 。
①
 丝 ②
丝 ② ③
③ ④液态
④液态 ⑤稀
⑤稀 ⑥熔融
⑥熔融 ⑦
⑦ 溶液 ⑧饱和
溶液 ⑧饱和 溶液 ⑨消毒酒精
溶液 ⑨消毒酒精回答下列问题:
(1)②和③之间互为
(2)以上物质中属于能导电的电解质是
(3)⑤中溶质的电离方程式为
(4)利用⑧制备
 胶体的操作方法是
胶体的操作方法是(5)向⑤中逐渐加入
 固体,其溶液的导电性变化情况是
固体,其溶液的导电性变化情况是(6)根据酸能电离出
 的数目可将酸分为一元酸(如
的数目可将酸分为一元酸(如 )、二元酸(如
)、二元酸(如 )、三元酸(如
)、三元酸(如 )。二元酸能与碱反应生成一种正盐(如
)。二元酸能与碱反应生成一种正盐(如 )和一种酸式盐(如
)和一种酸式盐(如 ),三元酸能与碱反应生成一种正盐(如
),三元酸能与碱反应生成一种正盐(如 )和两种酸式盐(如
)和两种酸式盐(如 、
、 )。
)。①
 属于二元酸,写出它与
属于二元酸,写出它与 反应生成酸式盐的化学方程式
反应生成酸式盐的化学方程式②
 与
与 溶液反应生成的酸式盐只有一种,则
溶液反应生成的酸式盐只有一种,则 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)写出 的电离方程式
的电离方程式___________ 。
(2) 中氧元素的化合价
中氧元素的化合价___________ 。
(3)氢化钠(NaH)可作为野外生氢剂,其化学反应原理为 。此反应中的氧化剂为
。此反应中的氧化剂为___________ (填化学式),若生成1mol ,则转移电子的物质的量为
,则转移电子的物质的量为___________ mol。
(1)写出
 的电离方程式
的电离方程式(2)
 中氧元素的化合价
中氧元素的化合价(3)氢化钠(NaH)可作为野外生氢剂,其化学反应原理为
 。此反应中的氧化剂为
。此反应中的氧化剂为 ,则转移电子的物质的量为
,则转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知溶液导电能力取决于自由移动离子的浓度和所带电荷数,离子浓度越大,所带电荷数越多,溶液导电能力越强。现有浓度均为1mol/L的以下电解质溶液:①K2CO3②AgNO3③NaHSO4④KOH⑤H2SO4⑥HCl⑦NaHCO3⑧Ba(OH)2⑨Al2(SO4)3⑩NaCl请回答相关问题。
(1)这些溶液中导电能力最强的是_______ (填溶质化学式),其电离方程式为_______ 。写出一种导电原理与电解质溶液不同的物质名称 _________ 。
(2)以上溶液两两混合后溶液的导电能力有多种变化趋势,请写出符合要求的组合(不考虑温度变化,填序号,如①和②)。导电能力变化符合图1的组合是_________ (任写一组);导电能力变化符合图2的组合是__________ ,混合过程中发生反应的离子方程式是_________ ;①的溶液和_______ (任写一种)的溶液混合导电能力变化符合图3且两溶液体积相等时导电能力最弱,溶液导电能力最弱时溶质的物质的量浓度为 ____________ 。
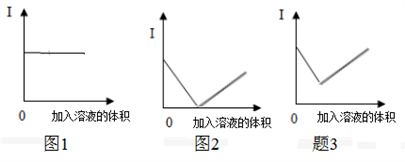
(1)这些溶液中导电能力最强的是
(2)以上溶液两两混合后溶液的导电能力有多种变化趋势,请写出符合要求的组合(不考虑温度变化,填序号,如①和②)。导电能力变化符合图1的组合是

您最近一年使用:0次



