(1)将1mol·L-1FeCl3饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为红褐色,得到的是_______ ;Fe(OH)3胶体与Fe(OH)3沉淀的本质区别在于_______ 。
(2)将(1)中得到的分散系装入U形管内,用石墨棒作电极,接通直流电源,通电一段时间后发现与电源负极相连的电极附近颜色_______ ,这个过程称为_______ 。
(3)掌握仪器的名称、组装及使用方法是中学化学实验的基础。下图为一套实验装置。
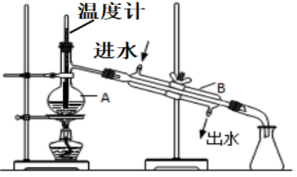
①写出仪器的名称:A._______ ,B._______ 。
②实验时A中除加入液体外,还需加入少量_______ ,其作用是_______ 。
③改正图中两处明显的错误:_______ ; _______
(2)将(1)中得到的分散系装入U形管内,用石墨棒作电极,接通直流电源,通电一段时间后发现与电源负极相连的电极附近颜色
(3)掌握仪器的名称、组装及使用方法是中学化学实验的基础。下图为一套实验装置。

①写出仪器的名称:A.
②实验时A中除加入液体外,还需加入少量
③改正图中两处明显的错误:
更新时间:2021-01-05 18:12:36
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有甲、乙、丙三名同学分别进行 Fe(OH)3胶体的制备实验。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是___________ ,反应的离子方程式为___________ 。
(2)证明有Fe(OH)3胶体生成的方法是___________ 。
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是___________ 。
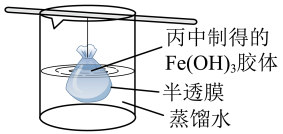
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___________ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的方法是
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是___________ ,分散剂是___________ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是___________ 。
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是___________ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是___________ 。
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是___________(填序号)
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是___________(填序号)
| A.两者颜色相同 | B.两者稳定性相同 |
| C.两者的分子直径均大于100nm | D.滴加稀盐酸后,两者现象完全相同 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是_______。
(2)Fe(OH)3胶体的制备:向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确_______ 。
(3)写出制备Fe(OH)3胶体的化学方程式:_______ 。
(4)怎样检验制备的物质是否为胶体?_______ 。
(5)取少量制得的胶体加入试管中,加入H2SO4溶液,现象是_______ 。
(6)氢氧化铁胶体稳定存在的主要原因是_______。
(7)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是_______。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是_______。
| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
(3)写出制备Fe(OH)3胶体的化学方程式:
(4)怎样检验制备的物质是否为胶体?
(5)取少量制得的胶体加入试管中,加入H2SO4溶液,现象是
(6)氢氧化铁胶体稳定存在的主要原因是_______。
| A.胶粒直径小于1 nm | B.胶粒带正电荷 |
| C.胶粒做布朗运动 | D.胶粒能透过滤纸 |
| A.Fe(OH)3胶体粒子的直径在1~100 nm之间 |
| B.Fe(OH)3胶体具有丁达尔效应 |
| C.Fe(OH)3胶体是均一的分散系 |
| D.Fe(OH)3胶体的分散质能透过滤纸 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空:
I、现有7种物质:①Na、②FeCl3溶液、③H2SO4、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl固体、⑧NaHSO4固体、⑨Ba(OH)2溶液。
(1)能导电的电解质有___________ (填序号)。
(2)属于盐的物质有___________ (填序号)。
(3)FeCl3溶液Fe(OH)3胶体的本质区别:___________ 。
(4)NaHSO4在水溶液中的电离方程式是___________ 。
(5)在两份相同体积相同浓度的Ba(OH)2溶液中,分别逐滴滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示:

其中Ba(OH)2和H2SO4反应的曲线为___________ 。(填①或②);b→d反应的离子方程式为___________ 。
II、用有关物质的量的相关知识进行计算:
(6)若1gN2中含有x个N原子,则阿伏加德罗常数为___________ 。
(7)一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入lmol氖气,右边充入CO和CO2的混合气体共18g时,隔板处于如图位置(左、右两侧温度相同)。则左、右两侧气体的原子个数比为___________ 。

I、现有7种物质:①Na、②FeCl3溶液、③H2SO4、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl固体、⑧NaHSO4固体、⑨Ba(OH)2溶液。
(1)能导电的电解质有
(2)属于盐的物质有
(3)FeCl3溶液Fe(OH)3胶体的本质区别:
(4)NaHSO4在水溶液中的电离方程式是
(5)在两份相同体积相同浓度的Ba(OH)2溶液中,分别逐滴滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示:

其中Ba(OH)2和H2SO4反应的曲线为
II、用有关物质的量的相关知识进行计算:
(6)若1gN2中含有x个N原子,则阿伏加德罗常数为
(7)一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入lmol氖气,右边充入CO和CO2的混合气体共18g时,隔板处于如图位置(左、右两侧温度相同)。则左、右两侧气体的原子个数比为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:_______ (填序号,下同)。以上物质属于电解质的是:_______ 。以上物质属于非电解质的是:_______ 。
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是_______ 。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:_______ ;继续滴加稀硫酸至过量可观察到的现象是_______ ,写出上述反应的化学方程式_______ 。
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
I.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO
②HCl、H2O、H2SO4、HNO3
③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):①________ ;②________ ;③________ 。
(2)若这三种物质相互作用可生成一种新物质碳酸氢钠,请写出该反应的化学反应方程式______________ 。
II.现有以下物质:
①NaCl晶体②液态HCl ③CaCO3固体④熔融KCl ⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH溶液
(1)以上物质中能导电的是____________ 。(填序号)
(2)以上物质中属于非电解质的是____________ 。(填序号
III.有一种橘红色的硫化锑(Sb2S3)胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,这叫________ 现象,证明Sb2S3胶粒带________ 电荷。
I.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO
②HCl、H2O、H2SO4、HNO3
③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):①
(2)若这三种物质相互作用可生成一种新物质碳酸氢钠,请写出该反应的化学反应方程式
II.现有以下物质:
①NaCl晶体②液态HCl ③CaCO3固体④熔融KCl ⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH溶液
(1)以上物质中能导电的是
(2)以上物质中属于非电解质的是
III.有一种橘红色的硫化锑(Sb2S3)胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,这叫
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答下列问题:
(1)写出NaCl的电离方程式_______ ;
(2)除去Na2CO3粉末中混有的少量NaHCO3的方法是_______ ;
(3)Cl2在化学反应中很容易_______ 电子(填“得”或“失”);
(4)向FeCl3溶液中滴加NaOH溶液时,可观察到的现象是_______ 。
(1)写出NaCl的电离方程式
(2)除去Na2CO3粉末中混有的少量NaHCO3的方法是
(3)Cl2在化学反应中很容易
(4)向FeCl3溶液中滴加NaOH溶液时,可观察到的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
Fe A
A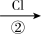 B
B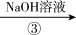 C
C
(1)反应①、②、③中属于氧化还原反应的是____ (填序号)。
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是____ 。
(3)C的化学式为____ 。
(4)写出反应②的离子方程式:________________ 。
Fe
 A
A B
B C
C(1)反应①、②、③中属于氧化还原反应的是
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是
(3)C的化学式为
(4)写出反应②的离子方程式:
您最近一年使用:0次

 A
A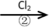 B
B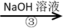 C
C

