在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)⇌A(g)+B(g), 经 一段时间后, 甲、乙两容器反应都达到平衡。下列说法中正确的是
| A.平均反应速度:乙>甲 | B.平衡时nc(甲)>nc(乙) |
| C.平衡时C的转化率:乙>甲 | D.平衡时A的物质的量甲>乙 |
2007高二·安徽·竞赛 查看更多[1]
更新时间:2021-08-07 16:22:37
|
【知识点】 化学平衡
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】对于反应N2O4(g)⇌2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法中,正确的是


| A.A、C两点对应状态的正反应速率大小关系为vA<vC |
| B.A、B、C、D、E各点对应状态中,v(正)<v(逆)的是B |
| C.维持p1不变,E→A所需时间为t1;维持p2不变,D→C所需时间为t2,则t1=t2 |
| D.欲使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的方法是从pl迅速加压至p2,再由p2无限缓慢降压至p1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)反应过程中测得的部分数据见下表(表中最t2>t1):
下列说法正确的是
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A.反应在t1min内的平均速率为υ(H2)=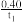 mol-1·L-1 ·min-1 mol-1·L-1 ·min-1 |
| B.保持其它条件不变,起始时向容器中充入0.60molCO和1.20molH2O,达到平衡时n(CO2)=0.40mol |
| C.保持其它条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 |
| D.温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐3】向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入2molH2、1molCO(甲)及1molH2、0.5molCO(乙)。发生的反应为2H2(g)+CO(g)⇌CH3OH(g) ∆H=-128.1kJ·mol-1。甲经4min,乙经5min达到平衡。测得平衡时乙容器中c(H2)=0.5mol·L-1。下列说法中正确的是
| A.体系总压强p:p(甲)<2p(乙) |
| B.乙中,前5min内的反应速率v(CO)=0.05mol·L-1·min-1 |
| C.放出的热量Q:Q(甲)=2Q(乙) |
| D.平衡时,甲容器中c(H2)=1.0mol·L-1 |
您最近一年使用:0次



