研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应: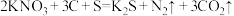 。其中作氧化剂的是
。其中作氧化剂的是_____ (填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为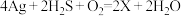 ,则
,则 的化学式是
的化学式是_____ ,其中 在该反应中
在该反应中_____ (填标号)。
A. 作氧化剂 B. 作还原剂
C. 既是氧化剂又是还原剂 D. 既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:
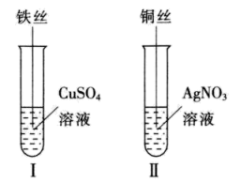
①Ⅱ中铜丝上观察到的现象是___________ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(4)取少量 粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:
粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:
①在烧杯中加入 蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈
蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈___________ 色,停止加热,用激光笔照射烧杯中的液体,可以观察到液体中___________ ,用这个实验可以区别___________ 和___________ 。
②向烧杯中液体逐滴加入过量的盐酸,写出发生反应的离子方程式:___________ 。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应:
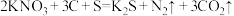 。其中作氧化剂的是
。其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为
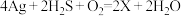 ,则
,则 的化学式是
的化学式是 在该反应中
在该反应中A. 作氧化剂 B. 作还原剂
C. 既是氧化剂又是还原剂 D. 既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)取少量
 粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:
粉末溶于适量盐酸,得到黄色溶液,用此溶液进行以下实验:①在烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈
蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液5~6滴,继续煮沸至液体呈②向烧杯中液体逐滴加入过量的盐酸,写出发生反应的离子方程式:
更新时间:2021-10-17 21:37:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:取 蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,然后向烧杯中逐滴滴加饱和
蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,然后向烧杯中逐滴滴加饱和 溶液。
溶液。
(1)生成 胶体的化学方程式为
胶体的化学方程式为___________ ,制备过程中,下列操作错误的是___________ (填标号)。
a.用 溶液代替蒸馏水
溶液代替蒸馏水
b.待水沸腾后滴加 滴饱和
滴饱和 溶液
溶液
c.当溶液呈红褐色时停止加热
d.用过滤的方法分离氢氧化铁胶体和生成的盐酸
(2)新制 胶体的胶团结构如图所示。
胶体的胶团结构如图所示。

① 胶体粒子带
胶体粒子带___________ (填“正”或“负”)电荷,胶体粒子的直径为___________ (填标号)。
A. B.
B. C.
C. D.
D.
②用一束光照射 胶体,在与光束垂直的方向进行观察,可以看到一条光亮的“通路”,这是胶体粒子对光线
胶体,在与光束垂直的方向进行观察,可以看到一条光亮的“通路”,这是胶体粒子对光线___________ (填“透射”、“反射”、“散射”或“折射”)造成的。
(3)某同学向 胶体中逐滴滴加稀盐酸,加入的离子中和了胶体粒子所带的电荷,使胶体粒子聚集成较大颗粒,从而形成红褐色沉淀,继续加稀盐酸,沉淀又溶解。
胶体中逐滴滴加稀盐酸,加入的离子中和了胶体粒子所带的电荷,使胶体粒子聚集成较大颗粒,从而形成红褐色沉淀,继续加稀盐酸,沉淀又溶解。
①红褐色沉淀为___________ (填化学式),其直接与水混合会形成悬浊液,悬浊液与胶体的本质区别为___________ 。
②沉淀溶解时反应的离子方程式是___________ 。
 蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,然后向烧杯中逐滴滴加饱和
蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,然后向烧杯中逐滴滴加饱和 溶液。
溶液。(1)生成
 胶体的化学方程式为
胶体的化学方程式为a.用
 溶液代替蒸馏水
溶液代替蒸馏水b.待水沸腾后滴加
 滴饱和
滴饱和 溶液
溶液c.当溶液呈红褐色时停止加热
d.用过滤的方法分离氢氧化铁胶体和生成的盐酸
(2)新制
 胶体的胶团结构如图所示。
胶体的胶团结构如图所示。
①
 胶体粒子带
胶体粒子带A.
 B.
B. C.
C. D.
D.
②用一束光照射
 胶体,在与光束垂直的方向进行观察,可以看到一条光亮的“通路”,这是胶体粒子对光线
胶体,在与光束垂直的方向进行观察,可以看到一条光亮的“通路”,这是胶体粒子对光线(3)某同学向
 胶体中逐滴滴加稀盐酸,加入的离子中和了胶体粒子所带的电荷,使胶体粒子聚集成较大颗粒,从而形成红褐色沉淀,继续加稀盐酸,沉淀又溶解。
胶体中逐滴滴加稀盐酸,加入的离子中和了胶体粒子所带的电荷,使胶体粒子聚集成较大颗粒,从而形成红褐色沉淀,继续加稀盐酸,沉淀又溶解。①红褐色沉淀为
②沉淀溶解时反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有甲、乙、丙三名同学分别进行制备 胶体的实验。
胶体的实验。
I.甲同学向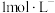 氯化铁溶液中加入少量的NaOH溶液;
氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和 溶液;
溶液;
III.丙同学向25mL沸水中逐滴加入 饱和溶液;煮沸至液体呈红褐色,停止加热。
饱和溶液;煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_______ 。写出此过程中的化学方程式_______ 。
(2)证明制得的红褐色液体属于胶体,最简单实验操作是_______ 。
(3) 胶体是不是电解质:
胶体是不是电解质:_______ (填“是”或“不是”)。
(4)丁同学利用所制得的 胶体进行下列实验:
胶体进行下列实验:
①向所得 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为_______ ;继续滴加,沉淀减少甚至最终消失,写出化学方程式_______ 。
②欲除去 胶体中患混有的NaCl,所用仪器物品是
胶体中患混有的NaCl,所用仪器物品是_______ 操作名称是_______ 。
 胶体的实验。
胶体的实验。I.甲同学向
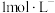 氯化铁溶液中加入少量的NaOH溶液;
氯化铁溶液中加入少量的NaOH溶液;II.乙同学直接加热饱和
 溶液;
溶液;III.丙同学向25mL沸水中逐滴加入
 饱和溶液;煮沸至液体呈红褐色,停止加热。
饱和溶液;煮沸至液体呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是
(2)证明制得的红褐色液体属于胶体,最简单实验操作是
(3)
 胶体是不是电解质:
胶体是不是电解质:(4)丁同学利用所制得的
 胶体进行下列实验:
胶体进行下列实验:①向所得
 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为②欲除去
 胶体中患混有的NaCl,所用仪器物品是
胶体中患混有的NaCl,所用仪器物品是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知下列九种物质:①H2O,②Al,③CO2,④盐酸,⑤硫酸钡,⑥NaOH⑦饱和FeCl3溶液,⑧氨水,⑨乙醇。根据上述提供的物质,回答下列问题:
(1)属于电解质的是_______________________ (填序号),属于非电解质__________ (填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为_________________________________________________________________________ 。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________ (填序号),反应的离子方程式为____________________________________________________________________________ 。
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:______________________________ ; ____________________________________________________________ 。
(1)属于电解质的是
(2)上述物质间发生的某反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为
(3)实验室制备少量Fe(OH)3胶体所用的物质有
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】作为绿色氧化剂和消毒剂, 在工业生产及日常生活中应用广泛。
在工业生产及日常生活中应用广泛。
I.过氧化氢的储存
(1)下图为 分解率与pH的变化关系,储存10.9%的
分解率与pH的变化关系,储存10.9%的 溶液的最佳pH范围为
溶液的最佳pH范围为___________ (填字母序号)。
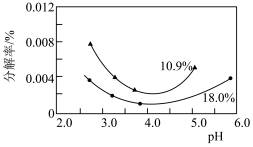
a.pH<2.5b.2.5<pH<3.5c.3.5<pH<4.5d.pH>4.5
Ⅱ.过氧化氢的制备
用催化氢气制备 是一种工艺简单、能耗低的方法,反应原理如图所示。
是一种工艺简单、能耗低的方法,反应原理如图所示。

(2)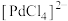 中元素Pd的化合价为
中元素Pd的化合价为___________ 。
(3)总反应的化学方程式为___________ 。
Ⅲ.探究过氧化氢的性质
实验1:将螺旋状铜丝插入30%的 溶液中,3小时后取出铜丝,观察到铜丝表面有棕色物质生成。
溶液中,3小时后取出铜丝,观察到铜丝表面有棕色物质生成。
实验2:将螺旋状铜丝插入30%的 溶液中,加入适量稀硫酸,观察到铜丝溶解,溶液变成蓝色,有少量无色气体产生。
溶液中,加入适量稀硫酸,观察到铜丝溶解,溶液变成蓝色,有少量无色气体产生。
(4)经X-射线光电子能谱仪测定,实验1中铜丝表面棕色物质的成分为CuO和 ,溶液中微粒的种类保持不变。写出生成
,溶液中微粒的种类保持不变。写出生成 的化学方程式并用单线桥法标明电子转移的方向和数目
的化学方程式并用单线桥法标明电子转移的方向和数目___________ 。
(5)实验2中铜丝溶解的离子方程式为___________ ;产生的气体为___________ 。
(6)用足量NaOH溶液处理实验2新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,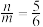 。X的化学式为
。X的化学式为___________ 。
 在工业生产及日常生活中应用广泛。
在工业生产及日常生活中应用广泛。I.过氧化氢的储存
(1)下图为
 分解率与pH的变化关系,储存10.9%的
分解率与pH的变化关系,储存10.9%的 溶液的最佳pH范围为
溶液的最佳pH范围为
a.pH<2.5b.2.5<pH<3.5c.3.5<pH<4.5d.pH>4.5
Ⅱ.过氧化氢的制备
用催化氢气制备
 是一种工艺简单、能耗低的方法,反应原理如图所示。
是一种工艺简单、能耗低的方法,反应原理如图所示。
(2)
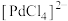 中元素Pd的化合价为
中元素Pd的化合价为(3)总反应的化学方程式为
Ⅲ.探究过氧化氢的性质
实验1:将螺旋状铜丝插入30%的
 溶液中,3小时后取出铜丝,观察到铜丝表面有棕色物质生成。
溶液中,3小时后取出铜丝,观察到铜丝表面有棕色物质生成。实验2:将螺旋状铜丝插入30%的
 溶液中,加入适量稀硫酸,观察到铜丝溶解,溶液变成蓝色,有少量无色气体产生。
溶液中,加入适量稀硫酸,观察到铜丝溶解,溶液变成蓝色,有少量无色气体产生。(4)经X-射线光电子能谱仪测定,实验1中铜丝表面棕色物质的成分为CuO和
 ,溶液中微粒的种类保持不变。写出生成
,溶液中微粒的种类保持不变。写出生成 的化学方程式并用单线桥法标明电子转移的方向和数目
的化学方程式并用单线桥法标明电子转移的方向和数目(5)实验2中铜丝溶解的离子方程式为
(6)用足量NaOH溶液处理实验2新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥的X在惰性氛围下加热,m g X完全分解为n g黑色氧化物Y,
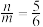 。X的化学式为
。X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)现有下列物质:①K2SO4晶体;②液态SO3;③冰醋酸(即纯醋酸);④汞;⑤小苏打;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠。其中:能导电的是______________ (填序号,下同);属于非电解质的是_________ 属于强电解质的是_____________ ;弱电解质的电离方程式:_________
(2)已知0.1 mol/L的NaHSO4溶液中H+的浓度为0.1mol/L, 若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1:1混合,离子方程式为________ ,此时溶液呈____ 性。
(3)若向Ba(OH)2溶液中缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的_________ (填序号)曲线表示。

(2)已知0.1 mol/L的NaHSO4溶液中H+的浓度为0.1mol/L, 若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1:1混合,离子方程式为
(3)若向Ba(OH)2溶液中缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】亚硫酰氯(SOCl2)在农药、医药、染料等生产中有重要应用,是一种无色或淡黄色液体,易挥发,遇水极易反应生成两种酸性气体。回答下列问题:
(1)根据价电子对互斥理论,亚硫酰氯空间构型为_______ ,其构成元素电负性由大到小的顺序为_______ 。
(2)实验室可通过将二氧化硫和氯气通入一氯化硫(S2Cl2)中反应制取亚硫酰氯。
①一氯化硫的电子式为_______ ;
②该反应中还原剂与氧化剂的物质的量之比为_______ ;
③向Ba(OH)2溶液中滴加少量亚硫酰氯,有白色沉淀生成,发生反应的离子方程式为_______ 。
(3)MgCl2·6H2O、AlCl3·6H2O、FeCl2·4H2O等结晶水合氯化物在空气中受热脱水易发生水解反应,常用亚硫酰氯作脱水剂以制取无水氯化物。
①在加热条件下,亚硫酰氯与MgCl2·6H2O反应的化学方程式为_______ 。
②MgCl2·6H2O在空气中受热脱水过程中,热重分析测得剩余固体质量占初始固体质量的百分含量随温度变化的曲线如图所示。
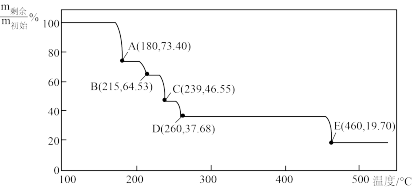
试判断A点固体的化学式为_______ ;460℃时发生反应的化学方程式为_______ 。
(1)根据价电子对互斥理论,亚硫酰氯空间构型为
(2)实验室可通过将二氧化硫和氯气通入一氯化硫(S2Cl2)中反应制取亚硫酰氯。
①一氯化硫的电子式为
②该反应中还原剂与氧化剂的物质的量之比为
③向Ba(OH)2溶液中滴加少量亚硫酰氯,有白色沉淀生成,发生反应的离子方程式为
(3)MgCl2·6H2O、AlCl3·6H2O、FeCl2·4H2O等结晶水合氯化物在空气中受热脱水易发生水解反应,常用亚硫酰氯作脱水剂以制取无水氯化物。
①在加热条件下,亚硫酰氯与MgCl2·6H2O反应的化学方程式为
②MgCl2·6H2O在空气中受热脱水过程中,热重分析测得剩余固体质量占初始固体质量的百分含量随温度变化的曲线如图所示。

试判断A点固体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法表示上述反应的电子转移情况。_______ 。
(2)根据上述反应,填写表格:
(3)参加反应的HNO3和作为氧化剂的HNO3的个数比为_______ 。
(4)若有64 g Cu被氧化,则生成的NO的质量是_______ 。
(5)Ag与稀硝酸也发生类似反应,写出反应的离子方程式:_______ 。
(1)用双线桥法表示上述反应的电子转移情况。
(2)根据上述反应,填写表格:
| 氧化剂 | 还原剂 | 氧化产物 | 还原产物 |
(3)参加反应的HNO3和作为氧化剂的HNO3的个数比为
(4)若有64 g Cu被氧化,则生成的NO的质量是
(5)Ag与稀硝酸也发生类似反应,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:
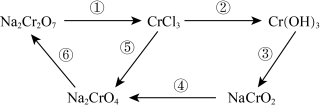
(1)Na2Cr2O7中Cr元素的化合价是_______ ,该物质属于_______ (填序号)。
① 酸 ② 碱 ③ 盐 ④ 氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是_______ (填序号)。
(3)反应①为:Na2Cr2O7 + HCl = NaCl + CrCl3 + Cl2↑+ H2O (未配平)。其中还原剂为_______ ,还原产物为 _______ 。Na2Cr2O7与Cl2的反应系数比为_______ 。
(4)完成反应④的配平,并用单线桥 标出电子转移的方向和数目_______ 。(系数若为1也请写出。)
反应④为:_______ClO + _______CrO
+ _______CrO + _
+ _  = _______Cl-+ _______CrO
= _______Cl-+ _______CrO + _______H2O
+ _______H2O

(1)Na2Cr2O7中Cr元素的化合价是
① 酸 ② 碱 ③ 盐 ④ 氧化物
(2)在上述转化中,Cr元素化合价不变的步骤是
(3)反应①为:Na2Cr2O7 + HCl = NaCl + CrCl3 + Cl2↑+ H2O (未配平)。其中还原剂为
(4)完成反应④的配平,并用
反应④为:_______ClO
 + _______CrO
+ _______CrO + _
+ _  = _______Cl-+ _______CrO
= _______Cl-+ _______CrO + _______H2O
+ _______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】宏观辨识与微观探析是化学学科核心素养之一、根据所学知识,回答下列问题:
(1)拟卤离子主要有 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
①已知还原性;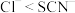 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:___________ 。
② 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为___________ 。氰化提金工艺在黄金生产领域仍占主导地位,但会产生大量含氰( )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含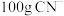 ),需要消耗
),需要消耗___________ g (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:___________ 。
(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成 。写出该反应的离子方程式:
。写出该反应的离子方程式:___________ ;在该反应中还原剂是___________ (填化学式)。氧化23g乙醇时转移电子的物质的量为___________ 。
(3) 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:___________ 。
(1)拟卤离子主要有
 、
、 、
、 ,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。
,性质与卤离子相似,它们相应的中性分子性质与卤素单质也相似。①已知还原性;
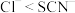 ,写出酸性条件下加热时,
,写出酸性条件下加热时, 和KSCN(aq)反应的离子方程式:
和KSCN(aq)反应的离子方程式:②
 与水反应生成的含氧酸的结构式为
与水反应生成的含氧酸的结构式为 )废水,含氰废水中加入足量的
)废水,含氰废水中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为 。理论上处理含氰废水(含
。理论上处理含氰废水(含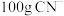 ),需要消耗
),需要消耗 (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:
(保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,请分析原因:(2)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成
 。写出该反应的离子方程式:
。写出该反应的离子方程式:(3)
 和
和 都属于离子型化合物,前者跟水反应生成
都属于离子型化合物,前者跟水反应生成 和
和 ,写出
,写出 跟水反应的化学方程式:
跟水反应的化学方程式:
您最近一年使用:0次



