已知溶液的导电性强弱由溶液中离子的浓度大小及离子所带电荷数决定。离子浓度越大,电荷数越多,则溶液导电性越强。某兴趣小组同学做了以下实验:
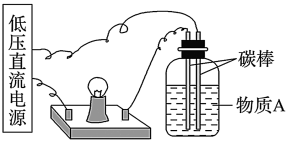
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质 可以是
可以是_______ (填序号)。
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性实验装置(如图1所示)中,若向某一电解质溶液中逐滴加另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮(如图2)的是_______ (填字母)。
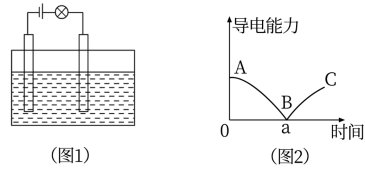
(3)试推测“硫酸中逐滴加入氢氧化钠溶液”,灯泡亮度的变化:_______ ,变化的原因_______ (用离子方程式解释)。
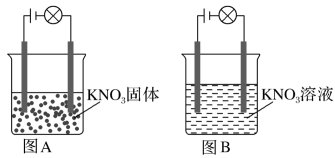
(4)某一化学兴趣小组的同学在家中进行实验,按照图A连接好线路,发现灯泡不亮;按照图B连接好线路,发现灯泡亮了。由此得出的以下结论中,正确的是_______

(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质
 可以是
可以是①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性实验装置(如图1所示)中,若向某一电解质溶液中逐滴加另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮(如图2)的是_______ (填字母)。

| A.盐酸中逐滴加入食盐溶液 |
| B.硫酸中逐滴加入氢氧化钠溶液 |
| C.石灰乳中滴加稀盐酸 |
| D.硫酸中逐滴加入氢氧化钡溶液 |
(4)某一化学兴趣小组的同学在家中进行实验,按照图A连接好线路,发现灯泡不亮;按照图B连接好线路,发现灯泡亮了。由此得出的以下结论中,正确的是_______

| A.硝酸钾固体不是电解质 |
| B.硝酸钾溶液是电解质 |
| C.硝酸钾在水溶液中电离出了可以自由移动的离子 |
| D.在硝酸钾溶液中,水电离出了大量的离子 |
2021高三·全国·专题练习 查看更多[2]
(已下线)专题24 弱电解质的电离(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)1.2.1 电解质及其电离(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)
更新时间:2021-12-05 09:14:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】以下为中学化学中常见的几种物质:(1)Cu (2)熔融NaCl (3)NaHSO4 (4)CO2 (5)H2SO4 (6)酒精 (7)KHCO3溶液 (8)BaSO4 (9)NaOH请按下列分类标准回答问题
(1)属于电解质的是___________
(2)属于酸的是___________
(3)属于难溶性盐的是___________
(4)属于非电解质的是___________
(5)能导电的是___________
(1)属于电解质的是
(2)属于酸的是
(3)属于难溶性盐的是
(4)属于非电解质的是
(5)能导电的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:_______ (填序号,下同)。以上物质属于电解质的是:_______ 。以上物质属于非电解质的是:_______ 。
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是_______ 。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:_______ ;继续滴加稀硫酸至过量可观察到的现象是_______ ,写出上述反应的化学方程式_______ 。
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有下列 10 种物质:
①Al②NaNO3③C2H5OH④CO2⑤H2SO4⑥NaOH⑦Fe(OH)3胶体⑧Na2O2⑨氨水⑩KAl(SO4)2
(1)上述 10 种物质中属于非电解质的是___________ (填编号)。
(2)上述 10 种物质中有两种物质之间可发生离子反应:H++OH- = H2O,该离子反应对应的化学方程为___________ 。
(3)⑩在水中的电离方程式为___________ 。
(4)①②⑥之间可发生如下反应,用单线桥标出该反应电子转移方向和数目___________ :10Al+6NaNO3+4NaOH =10NaAlO2+3N2↑+2H2O
(5)⑧可用作呼吸面具和潜艇的供氧剂,写出⑧与水反应的离子方程式___________ ,当生成气体在标准状况下的体积为 5.6 L 时,转移的电子数目为___________ 。
(6)常温下,⑤的浓溶液能用铁容器盛装,体现⑤的浓溶液的性质是___________ 。
①Al②NaNO3③C2H5OH④CO2⑤H2SO4⑥NaOH⑦Fe(OH)3胶体⑧Na2O2⑨氨水⑩KAl(SO4)2
(1)上述 10 种物质中属于非电解质的是
(2)上述 10 种物质中有两种物质之间可发生离子反应:H++OH- = H2O,该离子反应对应的化学方程为
(3)⑩在水中的电离方程式为
(4)①②⑥之间可发生如下反应,用单线桥标出该反应电子转移方向和数目
(5)⑧可用作呼吸面具和潜艇的供氧剂,写出⑧与水反应的离子方程式
(6)常温下,⑤的浓溶液能用铁容器盛装,体现⑤的浓溶液的性质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】阅读下列科普短文并填空:燃料电池是一种活性电池,具有能量转化率高、对环境友好等特点。例如,氢氧燃料电池在工作时,从负极连续通入①H2,从正极连续通入②O2,二者在电池内部(含有③H2SO4溶液或④KOH溶液)发生反应生成⑤H2O,同时产生电能。除了H2,⑥CH4、⑦C2H5OH等也可以作为燃料电池的燃料。目前已研制成功⑧Al—⑨空气燃料电池,它可以代替⑩汽油为汽车提供动力,也可以用做照明电源。
(1)在上述短文标有序号的物质中,属于混合物的是____ (填序号,下同);属于氧化物的是____ ;属于非电解质的是____ 。
(2)从物质的类别来看,H2、O2、Al都属于___ 。
(3)请写出③与④反应的离子方程式____ 。
(1)在上述短文标有序号的物质中,属于混合物的是
(2)从物质的类别来看,H2、O2、Al都属于
(3)请写出③与④反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下列物质属于电解质的是_________ ,非电解质是:________ ;(请填序号):
①稀硫酸 ②石墨 ③盐酸 ④HCl气体 ⑤CO2 ⑥熔融NaOH ⑦NaCl溶液 ⑧蔗糖 ⑨硫酸铜晶体 ⑩酒精
①稀硫酸 ②石墨 ③盐酸 ④HCl气体 ⑤CO2 ⑥熔融NaOH ⑦NaCl溶液 ⑧蔗糖 ⑨硫酸铜晶体 ⑩酒精
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】酸、碱、盐在水溶液中能导电是因为它们在溶液中发生了______ ,产生能够自由移动的离子。酸是指电离时生成的阳离子全部都是_____ 的化合物;碱是指电离时生成的阴离子全部都是___ 的化合物;盐是指电离生成____________________ 的化合物。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列物质在水溶液中的电离方程式。
(1)氢氧化钙_______ 。
(2)氯化铁_______ 。
(3)碳酸氢钠_______ 。
(4)硫酸_______ 。
(1)氢氧化钙
(2)氯化铁
(3)碳酸氢钠
(4)硫酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据要求写出方程式。
① NaCl溶液与AgNO3溶液反应____________________________ (写出离子方程式)
② K2SO4____________________________________________ (写出电离方程式)
③ NaHCO3_____________________________________________ (写出电离方程式)
① NaCl溶液与AgNO3溶液反应
② K2SO4
③ NaHCO3
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下面三个方法都可以用来制氯气:
①4HCl(浓) + MnO2 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
②KClO3 + 6HCl(浓)=3Cl2↑ + KCl + 3H2O
③KMnO4 + HCl(浓)——KCl + MnCl2 + Cl2↑ + H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②中,氧化产物与还原产物的质量比为_______ 。
(2)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_______ 。
(3)请将反应③配平:_______
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2+_______Cl2↑+_______H2O
(4)工业废水中的Cr2O 有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O
有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O 转化为Cr3+,其中Fe2+会被转化为Fe3+,反应的离子方程式
转化为Cr3+,其中Fe2+会被转化为Fe3+,反应的离子方程式_______ 。
①4HCl(浓) + MnO2
 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O②KClO3 + 6HCl(浓)=3Cl2↑ + KCl + 3H2O
③KMnO4 + HCl(浓)——KCl + MnCl2 + Cl2↑ + H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②中,氧化产物与还原产物的质量比为
(2)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(3)请将反应③配平:
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2+_______Cl2↑+_______H2O
(4)工业废水中的Cr2O
 有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O
有毒,常在酸性条件下用Fe2+做处理剂,将Cr2O 转化为Cr3+,其中Fe2+会被转化为Fe3+,反应的离子方程式
转化为Cr3+,其中Fe2+会被转化为Fe3+,反应的离子方程式
您最近一年使用:0次

 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O =BaSO4↓
=BaSO4↓

