下列物质:①Al② ③
③ ④
④ ⑤
⑤ ⑥酒精⑦
⑥酒精⑦ 溶液⑧
溶液⑧ ⑨熔融NaCl,请回答下面问题。
⑨熔融NaCl,请回答下面问题。
(1)属于电解质且能导电的是(填序号)___________ 。
(2)写出②溶于水的电离方程式:___________ 。
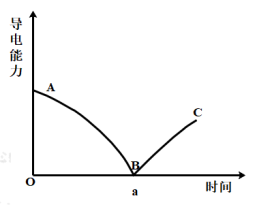
(3)向一定体积的②溶液中逐滴加入⑧的溶液,并测得混合溶液的导电能力随时间变化的曲线如图所示。写出AB段发生反应的离子方程式___________ ;图中___________ 处(填“A”或“B”或“C”)表示 溶液恰好被沉淀完全。
溶液恰好被沉淀完全。
(4)①与②溶液能反应产生 写出反应离子方程式
写出反应离子方程式________ 。Al还能和上述_____ 物质的溶液反应产生 (填序号)。
(填序号)。
 ③
③ ④
④ ⑤
⑤ ⑥酒精⑦
⑥酒精⑦ 溶液⑧
溶液⑧ ⑨熔融NaCl,请回答下面问题。
⑨熔融NaCl,请回答下面问题。(1)属于电解质且能导电的是(填序号)
(2)写出②溶于水的电离方程式:
(3)向一定体积的②溶液中逐滴加入⑧的溶液,并测得混合溶液的导电能力随时间变化的曲线如图所示。写出AB段发生反应的离子方程式
 溶液恰好被沉淀完全。
溶液恰好被沉淀完全。
(4)①与②溶液能反应产生
 写出反应离子方程式
写出反应离子方程式 (填序号)。
(填序号)。
21-22高一上·江西上饶·期末 查看更多[3]
江西省上饶市2021-2022学年高一上学期期末质量检测化学试题(已下线)第一章《物质及其变化》能力提升单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)河北省邢台市第二中学2022-2023学年高三上学期第一次月考化学试题
更新时间:2022-01-16 09:08:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用分类思想研究一类物质的通性和特殊性是学习化学的一种重要方法。以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。已知:Cl2+H2O=HCl+HClO;2Na+2H2O=2NaOH+H2↑;3NO2+H2O=2HNO3+NO。请根据你所学的知识,按要求填空:
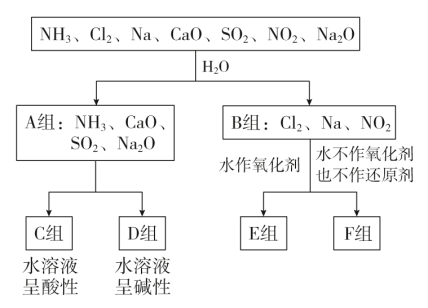
(1)C组中有哪些物质_______ ;F组物质中除了Cl2外还有_______ (填物质名称,下同)。
(2)A组中属于电解质的是_______ ,B组中既不是电解质也不是非电解质的是_______ (填物质名称,下同)。
(3)有反应①2H2O+Cl2+SO2=H2SO4+2HCl,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,针对上述两个反应回答下列问题:
①36g的水的物质的量是_______ , 的摩尔质量是
的摩尔质量是_______ 。
②反应②中浓盐酸表现出的性质是_______ (填字母)。
a.还原性 b.酸性 c.氧化性

(1)C组中有哪些物质
(2)A组中属于电解质的是
(3)有反应①2H2O+Cl2+SO2=H2SO4+2HCl,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,针对上述两个反应回答下列问题:
①36g的水的物质的量是
 的摩尔质量是
的摩尔质量是②反应②中浓盐酸表现出的性质是
a.还原性 b.酸性 c.氧化性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列物质:①稀硫酸②小苏打③氨水④二氧化碳⑤FeCl3固体⑥稀NaOH溶液⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2))有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______ 。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______ 。
(4)能导电的物质序号为_______________ 。
(5)实验室用⑤制备胶体的化学方程式为__________________________________ 。
(1)上述物质中属于电解质的物质序号为
(2))有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为
(4)能导电的物质序号为
(5)实验室用⑤制备胶体的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)以下为中学化学中常见的几种物质:①二氧化碳②熔融KC1③NaHSO4固体④铜⑤稀硫酸⑥蔗糖⑦澄清石灰水,其中属于电解质的有_____________ ,属于非电解质的有__________________ (填编号)。
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe (OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是_____________ (用化学式表示,后同),_____________ 元素被氧化,还原产物为_____________ ;
②当反应中有1molNaFeO4生成,转移的电子有_____________ mol;
③用单线桥法标出反应中电子转移的方向和数目。________
(3)配平该反应方程式:
______ K2Cr2O7+______ HCl═ ______ KCl+______ CrCl3+______ Cl2↑+______ H2O,
(4)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:_________________ 。
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe (OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是
②当反应中有1molNaFeO4生成,转移的电子有
③用单线桥法标出反应中电子转移的方向和数目。
(3)配平该反应方程式:
(4)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:
是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:

(1)写出“氧化炉”中氨催化氧化的化学方程式:___________ 。
(2)为避免 尾气污染环境,常用
尾气污染环境,常用 溶液吸收。
溶液吸收。
已知:①
②
现有一定条件下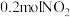 和
和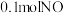 的混合气体恰好被
的混合气体恰好被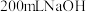 溶液完全吸收,则
溶液完全吸收,则 溶液的物质的量浓度为
溶液的物质的量浓度为___________  。
。
(3)已知氨氮废水中氮元素多以 和
和 的形式存在,加入
的形式存在,加入 可将废水中的
可将废水中的 转化为无污染气体,该反应的化学方程式为
转化为无污染气体,该反应的化学方程式为___________ 。
(4)用铜与浓硝酸反应时,观察到如下实验现象:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。某同学猜测反应后溶液呈绿色的原因是 在溶液中达到饱和,
在溶液中达到饱和, 的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后,溶液变为蓝色,可能的原因是
的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后,溶液变为蓝色,可能的原因是___________ 。(用离子方程式表示)
(5)某化学小组在实验室用63%的浓 (其密度为
(其密度为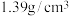 ,配制
,配制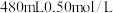 稀
稀 ,回答下列问题:
,回答下列问题:
①配制溶液需要用量筒量取63%的浓 的体积为
的体积为___________  。
。
②该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、量筒、___________ 。
③下列操作会使所配溶液浓度小于 的是:
的是:___________ 。(填对应的序号)
a.容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水
b.在操作中没有用蒸馏水洗涤烧杯和玻璃棒
c.定容时视线俯视刻度线
d.定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线
e.将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液
f.用量筒量取浓硝酸时视线仰视刻度线
 是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:
是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:
(1)写出“氧化炉”中氨催化氧化的化学方程式:
(2)为避免
 尾气污染环境,常用
尾气污染环境,常用 溶液吸收。
溶液吸收。已知:①

②

现有一定条件下
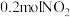 和
和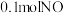 的混合气体恰好被
的混合气体恰好被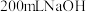 溶液完全吸收,则
溶液完全吸收,则 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(3)已知氨氮废水中氮元素多以
 和
和 的形式存在,加入
的形式存在,加入 可将废水中的
可将废水中的 转化为无污染气体,该反应的化学方程式为
转化为无污染气体,该反应的化学方程式为(4)用铜与浓硝酸反应时,观察到如下实验现象:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。某同学猜测反应后溶液呈绿色的原因是
 在溶液中达到饱和,
在溶液中达到饱和, 的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后,溶液变为蓝色,可能的原因是
的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后,溶液变为蓝色,可能的原因是(5)某化学小组在实验室用63%的浓
 (其密度为
(其密度为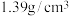 ,配制
,配制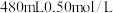 稀
稀 ,回答下列问题:
,回答下列问题:①配制溶液需要用量筒量取63%的浓
 的体积为
的体积为 。
。②该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、量筒、
③下列操作会使所配溶液浓度小于
 的是:
的是:a.容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水
b.在操作中没有用蒸馏水洗涤烧杯和玻璃棒
c.定容时视线俯视刻度线
d.定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线
e.将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液
f.用量筒量取浓硝酸时视线仰视刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列10种物质: ①硫酸 ②CO2 ③Ba(OH)2固体 ④NH4Al(SO4)2固体 ⑤葡萄糖 ⑥Al ⑦氢氧化铁胶体 ⑧CH3COOH ⑨熔融氯化钾 ⑩氯水
请回答下列问题:
(1)上述物质中属于电解质的是______ (填序号),属于非电解质的是___________ (填序号),能导电的是___________ (填序号)。
(2)将①的稀溶液加入⑦中,实验现象为___________ 。
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:_____ 。
(4)久置的氯水酸性增强的原因:(化学方程式表示)___________ 。
请回答下列问题:
(1)上述物质中属于电解质的是
(2)将①的稀溶液加入⑦中,实验现象为
(3)向④的溶液中加入过量③的稀溶液,发生的离子反应方程式为:
(4)久置的氯水酸性增强的原因:(化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据要求写出下列反应的离子方程式(标明化学方程式的除外)
(1)Na2S溶液和AgNO3溶液混合:_____________ 。
(2)硫磺与足量浓NaOH溶液共热,其中一种产物为Na2SO3:_____________ 。
(3)灭火器中NaHCO3与Al2(SO4)3溶液混合:_____________ 。
(4)工业流程中除去溶液中Fe3+时,也可采用以下方法:将pH值调整到1.6~1.8左右,并将溶液加热至85~95℃时,加入适量Na2SO4,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,反应的离子方程式为______________ 。
(5)含0.300molH3PO4的水溶液滴加到含0.500mol Ca(OH)2的悬浊液中,反应恰好完全,生成1种难溶盐和16.2gH2O。反应的化学方程式为______________ 。
(6)向一定比例的CuSO4、NaCl溶液中加入一定量的Na2SO3溶液可制得CuCl白色沉淀,并有刺激性气味气体产生:_____________ 。
(1)Na2S溶液和AgNO3溶液混合:
(2)硫磺与足量浓NaOH溶液共热,其中一种产物为Na2SO3:
(3)灭火器中NaHCO3与Al2(SO4)3溶液混合:
(4)工业流程中除去溶液中Fe3+时,也可采用以下方法:将pH值调整到1.6~1.8左右,并将溶液加热至85~95℃时,加入适量Na2SO4,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,反应的离子方程式为
(5)含0.300molH3PO4的水溶液滴加到含0.500mol Ca(OH)2的悬浊液中,反应恰好完全,生成1种难溶盐和16.2gH2O。反应的化学方程式为
(6)向一定比例的CuSO4、NaCl溶液中加入一定量的Na2SO3溶液可制得CuCl白色沉淀,并有刺激性气味气体产生:
您最近一年使用:0次



