“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_______ (填序号,下同);属于盐类的是_______ ;相互间能发生反应的是_______ 。
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的_______ (填物质名称),该反应的离子方程式是1ClO-+1CO2+1H2O=_______+_______。_______
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的
更新时间:2022/04/11 12:57:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有以下5个反应(反应条件略):
a.Na2O+CO2=Na2CO3
b.CH4+2O2=CO2+2H2O
c.2KClO3=2KCl+3O2↑
d.2Na+2H2O=2NaOH+H2↑
e.CaCO3+2HCl=CaCl2+H2O+CO2↑
(1)属于化合反应的有________ (填编号,下同),属于分解反应的有________ ,属于置换反应的有________ ,属于复分解反应的有________ 。
(2)上述5个反应中,盐有__________ 种,其中难溶于水的是________ (填化学式)。
a.Na2O+CO2=Na2CO3
b.CH4+2O2=CO2+2H2O
c.2KClO3=2KCl+3O2↑
d.2Na+2H2O=2NaOH+H2↑
e.CaCO3+2HCl=CaCl2+H2O+CO2↑
(1)属于化合反应的有
(2)上述5个反应中,盐有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氢氧化钙,俗称熟石灰或消石灰,是一种白色粉末状固体。氢氧化钙是重要的建筑材料。农药中的波尔多液正是利用石灰乳(溶于水的氢氧化钙)和硫酸铜水溶液按照一定的比例配制而成的。冬天,树木过冬防虫,树木根部以上涂80 cm的石灰浆。
工业上常用下列方法制备氢氧化钙。具体过程为:将石灰石煅烧成氧化钙后,经精选与水按1∶(3~3.5)的比例混合,生成氢氧化钙料液经净化分离除渣,再经离心脱水,干燥,即为氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
(2)写出生成波尔多液的化学反应方程式,并注明反应类型:__________ 。
(3)写出工业制备氢氧化钙的化学方程式,并注明物质类别的转化关系。示例如下:
A(氧化物)+B(氧化物)→C(盐)___________ 。
(4)请写出与题目不相同的制备氢氧化钙的方法,并说明工业生产方法的优点:___________ 。
工业上常用下列方法制备氢氧化钙。具体过程为:将石灰石煅烧成氧化钙后,经精选与水按1∶(3~3.5)的比例混合,生成氢氧化钙料液经净化分离除渣,再经离心脱水,干燥,即为氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
| 类别 | 混合物 | 碱 | 氧化物 |
| 名称 | |||
| 化学式 | 无 |
(3)写出工业制备氢氧化钙的化学方程式,并注明物质类别的转化关系。示例如下:
A(氧化物)+B(氧化物)→C(盐)
(4)请写出与题目不相同的制备氢氧化钙的方法,并说明工业生产方法的优点:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】对下列物质分类,并完善表格内容
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
| 物质 | 分类依据 | 物质类型 | 实例 |
| 酸 | 根据酸根离子是否含有氧元素 | 含氧酸 | |
| 无氧酸 | |||
根据一定条件下能电离出 的数目 的数目 | 一元酸 | ||
| 二元酸 | |||
| 三元酸 | |||
| 根据电离程度 | 强酸 | ||
| 弱酸 | |||
| 根据沸点高低 | 高沸点酸 | ||
| 低沸点酸 | |||
| 盐 | 根据生成盐时酸、碱中和反应进行的程度 | 正盐 | |
| 酸式盐 | |||
| 碱式盐 | |||
| 根据生成盐的酸或碱的强弱 | 强酸强碱盐 | ||
| 强酸弱碱盐 | |||
| 弱酸强碱盐 | |||
| 根据溶解性 | 易溶性盐 | ||
| 难溶性盐 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了 。氯水中存在的离子有
。氯水中存在的离子有___________ ; 的结构式为
的结构式为___________ ; 在溶液中电离本质是
在溶液中电离本质是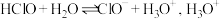 的电子式是
的电子式是___________ 。
(2) 氮的氧化物
氮的氧化物 中,含
中,含 物质的量为
物质的量为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)已知反应: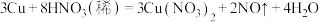 。若有
。若有 被氧化,则被还原的
被氧化,则被还原的 的物质的量是
的物质的量是___________  。
。
(4) 是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备
是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备 的一种方法为在平底烧瓶中加入
的一种方法为在平底烧瓶中加入 固体、足量草酸
固体、足量草酸 、稀硫酸,
、稀硫酸, 水浴加热。已知草酸被氧化为
水浴加热。已知草酸被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(5)消毒效率是指消毒剂的有效氯。有效氯 有效系数
有效系数 含氯量,其中有效系数
含氯量,其中有效系数 夺取电子数,含氯量
夺取电子数,含氯量 的消毒效率为
的消毒效率为___________ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了
 。氯水中存在的离子有
。氯水中存在的离子有 的结构式为
的结构式为 在溶液中电离本质是
在溶液中电离本质是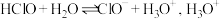 的电子式是
的电子式是(2)
 氮的氧化物
氮的氧化物 中,含
中,含 物质的量为
物质的量为 ,则
,则 的摩尔质量为
的摩尔质量为(3)已知反应:
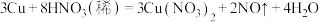 。若有
。若有 被氧化,则被还原的
被氧化,则被还原的 的物质的量是
的物质的量是 。
。(4)
 是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备
是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备 的一种方法为在平底烧瓶中加入
的一种方法为在平底烧瓶中加入 固体、足量草酸
固体、足量草酸 、稀硫酸,
、稀硫酸, 水浴加热。已知草酸被氧化为
水浴加热。已知草酸被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为(5)消毒效率是指消毒剂的有效氯。有效氯
 有效系数
有效系数 含氯量,其中有效系数
含氯量,其中有效系数 夺取电子数,含氯量
夺取电子数,含氯量 的消毒效率为
的消毒效率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.有下列物质:①氢氧化钡溶液②KHSO4③稀硫酸④干冰⑤石墨⑥蔗糖晶体⑦熔融氯化钠。请用序号填空:
(1)上述状态下可导电的是___________ ,向氢氧化钡溶液中通入少量二氧化碳气体溶液的导电性将___________ (增强、减弱或不变)。
(2)属于非电解质的是___________ 。
II.实验小组为探究次氯酸消毒剂的分解规律,进行了下列实验。
①制备和净化氯气:使用二氧化锰等几种原料制备并净化氯气。
②制备氯水:将氯气通入水中,得到氯水。
③除去尾气:用烧碱溶液吸收多余的氯气。
④探究次氯酸的分解规律:用数字传感器测量光照条件下装有氯水的容器中氧气浓度的变化、氯水的pH变化以及氯离子浓度的变化装置如图1所示。测量的数据如图2所示。
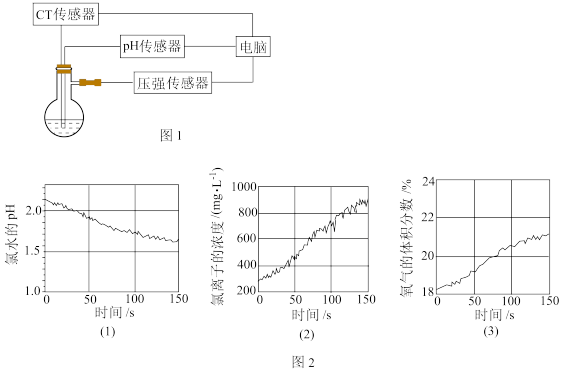
(3)实验室用二氧化锰制备氯气时发生反应的化学方程式为___________ ;该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)依据数字传感器所测量的图2中(1)和(2)数据,光照时氯水的pH变化及氯离子浓度变化的原因是___________ (用离子方程式表示)。
(1)上述状态下可导电的是
(2)属于非电解质的是
II.实验小组为探究次氯酸消毒剂的分解规律,进行了下列实验。
①制备和净化氯气:使用二氧化锰等几种原料制备并净化氯气。
②制备氯水:将氯气通入水中,得到氯水。
③除去尾气:用烧碱溶液吸收多余的氯气。
④探究次氯酸的分解规律:用数字传感器测量光照条件下装有氯水的容器中氧气浓度的变化、氯水的pH变化以及氯离子浓度的变化装置如图1所示。测量的数据如图2所示。

(3)实验室用二氧化锰制备氯气时发生反应的化学方程式为
(4)依据数字传感器所测量的图2中(1)和(2)数据,光照时氯水的pH变化及氯离子浓度变化的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学与我们的生活、生产、环境、资源利用等息息相关。回答下列问题:
(1)氯化铁可用于净水,写出其溶于水的电离方程式:________ ;在氯化铁溶液中加入铁粉,发生反应的离子方程式是___________ ;在氯化铁的水溶液中逐滴加入氢氧化钠溶液,可观察到的现象是__________ 。
(2)漂白粉常用作棉、麻、纸张的漂白剂,还可用作游泳池及环境消毒剂。漂白粉的有效成分为_________ ,写出漂白粉在空气中失效的有关化学方程式:_________ 、________ 。
(3)pH小于5.6的天然降水称为酸雨,引起酸雨的主要物质是SO2和_________ 。燃煤脱硫可有效减少酸雨的形成,燃煤脱硫除用石灰法外,也可以向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为MgSO4,写出该反应的化学方程式:___________ 。
(1)氯化铁可用于净水,写出其溶于水的电离方程式:
(2)漂白粉常用作棉、麻、纸张的漂白剂,还可用作游泳池及环境消毒剂。漂白粉的有效成分为
(3)pH小于5.6的天然降水称为酸雨,引起酸雨的主要物质是SO2和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】含有农药、染料、酚、氰化物,以及引起色度、臭味的废水,常用化学氧化法进行处理,所用的氧化剂有氯类(如液氯、次氯酸钙、次氯酸钠等)和氧类(如空气、臭氧、过氧化氢、高锰酸钾等)。一个典型实例是用氯氧化法处理含有剧毒的氰化物(含CN-)的废水。在碱性条件下(pH=8.5~11),氯气可将氰化物中CN-氧化为只有它毒性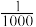 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。
(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:_________________ 。
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:______________________________________________ 。
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为__________________________________________ 。
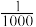 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为
您最近一年使用:0次



