铁是人类较早使用的金属之一,如图为铁及其化合物的“价—类”二维图。
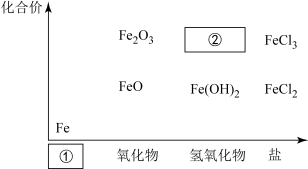
(1)填写二维图缺失的类别①_______ 和化学式②_______ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2 ②Fe ③NaOH ④AgNO3。从物质类别上看,FeCl3属于_______ ,可能与_______ 发生反应(填序号);从化合价角度看,Fe3+具有_______ 性,可能与_______ 发生反应(填序号)。
(3)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是_______ nm。
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
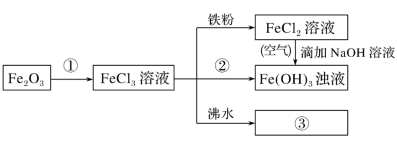
(5)Fe2O3与物质①反应的化学方程式为_______ 。
(6)FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是_______ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2 ②Fe ③NaOH ④AgNO3。从物质类别上看,FeCl3属于
(3)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:

(5)Fe2O3与物质①反应的化学方程式为
(6)FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
更新时间:2022-09-03 07:05:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组在实验室中以烧杯为容器,用饱和 溶液制备
溶液制备 胶体,并对其性质做了如下探究:
胶体,并对其性质做了如下探究:
【实验制备】
(1)将饱和 溶液加到沸水中,加热至整个体系呈
溶液加到沸水中,加热至整个体系呈_______ 色为止,即制得 胶体。
胶体。
(2)制备过程中,发生化学反应的方程式为___________ 。
(3)小米同学在制备时,加热时间过久,结果未能得到胶体。那么小米同学得到的物质应该是:___________ (填化学式),该物质属于___________ (请从下面选择)
A.酸 B.碱 C.盐
【性质探究】
(4)小庄同学想证明 胶体已经制备成功,她可以利用
胶体已经制备成功,她可以利用___________ (最简单的方法,请写出方法的名称)进行鉴别。
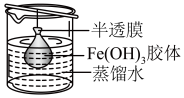
(5)小静同学利用___________ (填方法名称)方法对 胶体提纯。
胶体提纯。
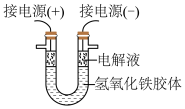
(6)小邱同学将提纯后的 胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源
胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源___________ 极相连的那个电极附近的颜色变深,说明___________ (请写出分析理由),化学上把这种现象称为___________ 。
 溶液制备
溶液制备 胶体,并对其性质做了如下探究:
胶体,并对其性质做了如下探究:【实验制备】
(1)将饱和
 溶液加到沸水中,加热至整个体系呈
溶液加到沸水中,加热至整个体系呈 胶体。
胶体。(2)制备过程中,发生化学反应的方程式为
(3)小米同学在制备时,加热时间过久,结果未能得到胶体。那么小米同学得到的物质应该是:
A.酸 B.碱 C.盐
【性质探究】
(4)小庄同学想证明
 胶体已经制备成功,她可以利用
胶体已经制备成功,她可以利用(5)小静同学利用
 胶体提纯。
胶体提纯。
(6)小邱同学将提纯后的
 胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源
胶体置于U型管中(如图),通入直流电一段时间后,观察到与电源
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】通过分散系的学习,我们认识了胶体,下面就胶体的制备以及相关性质做了相应探究。根据所学回答下列问题:
(1)取少量Fe2O3粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为__________________ ,反应后得到的溶液(记为A)。
(2)取少量A置于试管中,滴入几滴NaOH溶液,可观察到红褐色沉淀生成(记为B),反应的离子方程式为___________ ,此反应属于___________ (填基本反应类型)。
(3)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入___________ (填“饱和A”或“B”),继续煮沸至溶液呈___________ 色,停止加热,即制得Fe(OH)3胶体(记为C)。
(4)另取一只小烧杯也加入25mL蒸馏水,接着向烧杯中加入少量CuSO4溶液,振荡均匀后的液体(记为D),将C与D一起放置于暗处,分别用激光笔照射,可以看到___________ (填现象)。
(1)取少量Fe2O3粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
(2)取少量A置于试管中,滴入几滴NaOH溶液,可观察到红褐色沉淀生成(记为B),反应的离子方程式为
(3)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入
(4)另取一只小烧杯也加入25mL蒸馏水,接着向烧杯中加入少量CuSO4溶液,振荡均匀后的液体(记为D),将C与D一起放置于暗处,分别用激光笔照射,可以看到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验小组探究 胶体的制备方法及其性质。
胶体的制备方法及其性质。
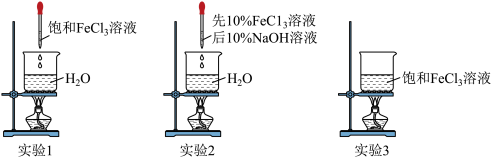
Ⅰ.制备 胶体
胶体
(1)实验1,生成 胶体和
胶体和_______ (填化学式)。
(2)实验2与实验1对比,优点是_______ (写出1条即可)。
(3)综合上述实验:制备 胶体提供
胶体提供 的物质可以是
的物质可以是 或
或_______ ,控制反应条件即可制得。
Ⅱ. 胶体的性质
胶体的性质
(4)下列关于 胶体和
胶体和 悬浊液的描述,正确的是_______
悬浊液的描述,正确的是_______
(5)将 胶体置于U型管中,通直流电一段时间,观察到
胶体置于U型管中,通直流电一段时间,观察到_______ 极附近颜色变深,说明_______ 。
资料:
Ⅰ.pH>10时, 胶体溶解。
胶体溶解。
Ⅱ.固体 易升华。
易升华。
实验4取5mL实验3得到的液体于蒸发皿中,继续加热,待蒸发皿中液体变为黏稠状,罩上漏斗,可观察到漏斗内出现棕褐色的烟,且有棕褐色固体附着在漏斗的内壁上。继续加热,蒸发皿中最终得到红棕色固体 。
。
(6)根据资料,推测漏斗内棕褐色的烟中主要含有_______ (填化学式)。
研究表明: 胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。
胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。
(7)不同pH时,测得溶液中 胶体对砷酸的吸附效率如图。
胶体对砷酸的吸附效率如图。
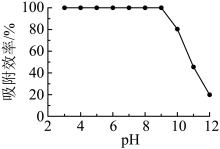
pH为3~9时, 胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是
胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是_______ 。
(8)去除水中高浓度砷酸的原理是 胶体与砷酸反应生成砷酸铁(
胶体与砷酸反应生成砷酸铁( )沉淀,化学方程式是
)沉淀,化学方程式是_______ 。
 胶体的制备方法及其性质。
胶体的制备方法及其性质。
Ⅰ.制备
 胶体
胶体| 实验 | 实验操作 | 丁达尔效应 |
| 1 | 向40mL沸腾的蒸馏水中滴入5滴饱和 溶液(浓度约为30%) 溶液(浓度约为30%) | 迅速出现 |
| 2 | 向40mL蒸馏水中滴入5滴10% 溶液,然后滴入1滴10%NaOH溶液,边滴边搅拌 溶液,然后滴入1滴10%NaOH溶液,边滴边搅拌 | 迅速出现 |
| 3 | 加热40mL饱和 溶液 溶液 | 一段时间后出现 |
 胶体和
胶体和(2)实验2与实验1对比,优点是
(3)综合上述实验:制备
 胶体提供
胶体提供 的物质可以是
的物质可以是 或
或Ⅱ.
 胶体的性质
胶体的性质(4)下列关于
 胶体和
胶体和 悬浊液的描述,正确的是_______
悬浊液的描述,正确的是_______| A.两者颜色相同 | B.两者稳定性相同 |
| C.两者的分散质直径均大于100nm | D.滴加稀盐酸后,两者现象完全相同 |
 胶体置于U型管中,通直流电一段时间,观察到
胶体置于U型管中,通直流电一段时间,观察到资料:
Ⅰ.pH>10时,
 胶体溶解。
胶体溶解。Ⅱ.固体
 易升华。
易升华。实验4取5mL实验3得到的液体于蒸发皿中,继续加热,待蒸发皿中液体变为黏稠状,罩上漏斗,可观察到漏斗内出现棕褐色的烟,且有棕褐色固体附着在漏斗的内壁上。继续加热,蒸发皿中最终得到红棕色固体
 。
。(6)根据资料,推测漏斗内棕褐色的烟中主要含有
研究表明:
 胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。
胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。(7)不同pH时,测得溶液中
 胶体对砷酸的吸附效率如图。
胶体对砷酸的吸附效率如图。
pH为3~9时,
 胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是
胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是(8)去除水中高浓度砷酸的原理是
 胶体与砷酸反应生成砷酸铁(
胶体与砷酸反应生成砷酸铁( )沉淀,化学方程式是
)沉淀,化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】【任务一】探究墨粉中铁的氧化物。墨粉是由树脂和炭黑、电荷剂、磁粉(铁氧化物)等组成。
(1)向一定量墨粉中加入适量的稀硫酸充分振荡后,向试管中缓缓压入棉花团至试管底部,棉花团所起的作用是___________ 。
(2)取(1)中水层部分清液,把清液分装两试管,一试管中加入适量 溶液,出现
溶液,出现_________ ,证明有Fe3+,另一试管中加入铁氰化钾溶液,立即出现______ ,证明有Fe2+。
【任务二】设计实验方案,测定墨粉中铁元素的质量分数。取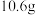 墨粉经过一系列操作,配制成
墨粉经过一系列操作,配制成 溶液(溶液中铁元素全部转化为Fe3+),取出
溶液(溶液中铁元素全部转化为Fe3+),取出 溶液,用
溶液,用 的
的 溶液滴定。
溶液滴定。
(1)滴定过程中,选择的指示剂是______ 。
a.淀粉溶液 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(2)若滴定过程中消耗 溶液
溶液 ,则墨粉中铁的质量分数为
,则墨粉中铁的质量分数为______ (百分数保留两位整数)。
【任务三】了解 的工业制备。复印机使用的墨粉的主要成分是
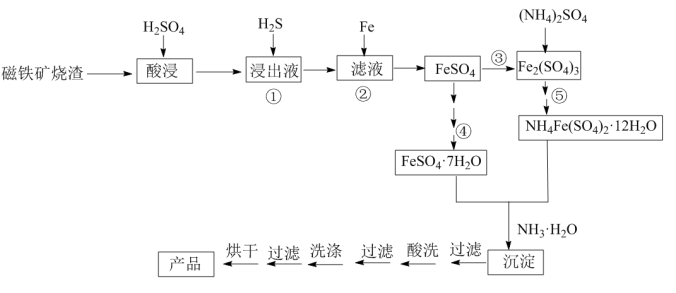
的工业制备。复印机使用的墨粉的主要成分是 ,如图是利用硫铁矿烧渣制备高纯
,如图是利用硫铁矿烧渣制备高纯 的工艺流程。
的工艺流程。
已知:
①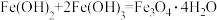 ;
;
② 在水中可溶,在乙醇中难溶;
在水中可溶,在乙醇中难溶;
③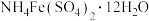 在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线如图所示:
在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线如图所示:
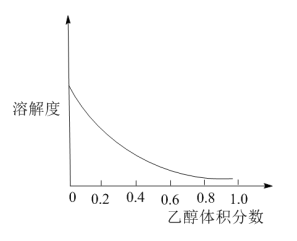
回答下列问题:
(1)①浸出液中含有的金属阳离子为______________ ,操作②中加入铁屑的目的是_________ 。
(2)步骤③用 作氧化剂的优点是
作氧化剂的优点是_______ 。
(3)经步骤⑤后,一般需要对所得晶体进行洗涤和干燥处理。请说出选择乙醇和水的混合液作为洗涤液的理由___________ 。
(1)向一定量墨粉中加入适量的稀硫酸充分振荡后,向试管中缓缓压入棉花团至试管底部,棉花团所起的作用是
(2)取(1)中水层部分清液,把清液分装两试管,一试管中加入适量
 溶液,出现
溶液,出现【任务二】设计实验方案,测定墨粉中铁元素的质量分数。取
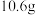 墨粉经过一系列操作,配制成
墨粉经过一系列操作,配制成 溶液(溶液中铁元素全部转化为Fe3+),取出
溶液(溶液中铁元素全部转化为Fe3+),取出 溶液,用
溶液,用 的
的 溶液滴定。
溶液滴定。(1)滴定过程中,选择的指示剂是
a.淀粉溶液 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(2)若滴定过程中消耗
 溶液
溶液 ,则墨粉中铁的质量分数为
,则墨粉中铁的质量分数为【任务三】了解
 的工业制备。复印机使用的墨粉的主要成分是
的工业制备。复印机使用的墨粉的主要成分是 ,如图是利用硫铁矿烧渣制备高纯
,如图是利用硫铁矿烧渣制备高纯 的工艺流程。
的工艺流程。
已知:
①
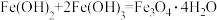 ;
;②
 在水中可溶,在乙醇中难溶;
在水中可溶,在乙醇中难溶;③
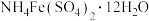 在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线如图所示:
在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线如图所示:
回答下列问题:
(1)①浸出液中含有的金属阳离子为
(2)步骤③用
 作氧化剂的优点是
作氧化剂的优点是(3)经步骤⑤后,一般需要对所得晶体进行洗涤和干燥处理。请说出选择乙醇和水的混合液作为洗涤液的理由
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E是中学常见的五种物质,其转化关系如图所示。反应I、II均在水溶液中进行,其中某些物质可能已略去。已知D是双原子分子形成的单质,C、E是化合物。

(1)若A是气态单质,其水溶液具有漂白性,D在常温下为固态。E是一种可溶性强碱,其焰色反应为黄色。则
①A、C的化学键类型分别为_______ ,_______ ;
②写出C的一种用途_______ ;
③写出A+B→C+D反应的化学方程式_______ 。
(2)若A是金属单质,D是无色气体,E是A的盐溶液。则
①D的化学式是_______
②A和E发生反应的离子方程式为_______ 。

(1)若A是气态单质,其水溶液具有漂白性,D在常温下为固态。E是一种可溶性强碱,其焰色反应为黄色。则
①A、C的化学键类型分别为
②写出C的一种用途
③写出A+B→C+D反应的化学方程式
(2)若A是金属单质,D是无色气体,E是A的盐溶液。则
①D的化学式是
②A和E发生反应的离子方程式为
您最近一年使用:0次
【推荐3】某研究小组同学对市售某种补铁口服液的成分进行探究。根据名称认为该糖浆中含有Fe2+,设计方案进行验证。

I.设计方案如下:
(1)方案i的预期现象是产生白色沉淀,逐渐变为灰绿色,最终变为红褐色。产生白色沉淀的离子方程式是_________ ,最终变为红褐色的化学方程式是________ 。
(2)方案ii的预期现象是_________ 。
(3)方案iii的预期现象是________ ,反应中氯水参与反应的的离子方程式是____ 。
II.进行实验操作,得到的实际现象如下:
(4)为探究实验中出现异常现象的原因,该小组同学查看说明书,得知有关补铁口服液成分的如下:
结合资料对异常现象产生的原因进行猜想:______________ ;为验证其猜想,在方案iii的基础上继续加入过量的氯水,得到了预期的现象。
(5) 实验反思:方案ii中预期现象与实验现象相同,并不能证明补铁口服液中一定含有Fe2+,理由是______ 。
(6)小组同学进一步提出研究问题:仍选用之前用过的试剂,设计实验验证某久置的补铁口服液(计为Y)已部分变质。以下是小组同学的实验方案:
实验V的操作及现象是_____________ 。

I.设计方案如下:
 | 方案 | 试剂X | 预期现象 |
| 方案i | 1mL 1 mol/L NaOH溶液 | a | |
| 方案ii | 1mL 1 mol/L 酸性KMnO4溶液 | b | |
| 方案iii | 依次加入5滴KSCN溶液、1mL氯水 | c |
(2)方案ii的预期现象是
(3)方案iii的预期现象是
II.进行实验操作,得到的实际现象如下:
| 方案 | 实际现象 | 是否与预期现象相同 |
| 方案i | 产生灰绿色浑浊,长时间不变红褐色 | 不同 |
| 方案ii | 相同 | |
| 方案iii | 自始至终无明显现象 | 不同 |
| 本品每毫升含主要成分葡萄糖酸亚铁30毫克, 辅料为:蔗糖、香精、枸檬酸、羟苯乙酯。 |
(5) 实验反思:方案ii中预期现象与实验现象相同,并不能证明补铁口服液中一定含有Fe2+,理由是
(6)小组同学进一步提出研究问题:仍选用之前用过的试剂,设计实验验证某久置的补铁口服液(计为Y)已部分变质。以下是小组同学的实验方案:
| 实验序号 | 操作 | 现象 |
| ⅳ | 取2 mL溶液Y,加入1滴KSCN,再加入1 mL水 | 溶液显红色 |
| V |
您最近一年使用:0次



