如图为一“铁链”图案,小明在图案上分别写了 、
、 、
、 、NaCl、
、NaCl、 五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:

(1)请将分类依据代号填入相应的空格内:
____________ 两种物质都不是电解质;
____________ 两种物质都是钠的化合物;
____________ 两种物质都是氧化物;
____________ 两种物质都是盐。
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为____________ 。
②证明有红褐色胶体生成的方法是____________ 。
(3)按要求写出方程式:
①制备该红褐色胶体的化学方程式______________ ;
②硫酸氢钾溶于水的电离方程式是__________ ;
 、
、 、
、 、NaCl、
、NaCl、 五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
(1)请将分类依据代号填入相应的空格内:
(2)实验室常用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为
②证明有红褐色胶体生成的方法是
(3)按要求写出方程式:
①制备该红褐色胶体的化学方程式
②硫酸氢钾溶于水的电离方程式是
更新时间:2022-10-27 17:05:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】物质集合M中含有常见物质Na2O2、NaHCO3、Al、SO2、Fe、NH3、Na、Cl2,这些物质按照以下方法进行分类后如图所示,其中A组为单质,B组为化合物,请按照要求回答问题。
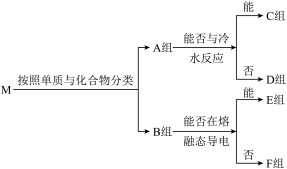
(1)该分类方法为_______ ,
(2)B组物质中属于非电解质的为_______ ,其中能作制冷剂的物质的电子式为_______ 。
(3)C组物质中有的能与水剧烈反应,该反应中氧化剂和还原剂物质的量之比为_______ 。
(4)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:_______ 。
(5)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:_______ 。
(6)在密闭容器中,将E组中的混合物加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为_______ ;

(1)该分类方法为
(2)B组物质中属于非电解质的为
(3)C组物质中有的能与水剧烈反应,该反应中氧化剂和还原剂物质的量之比为
(4)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:
(5)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:
(6)在密闭容器中,将E组中的混合物加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请对下列化合物:①NaCl、②HCl、③CaCl2、④CuO、⑤H2O、⑥Fe2O3进行分类:
(1)依据通常状况下物质的____ 为标准分类,属于固体的是_____ (填序号,下同),属于液体的是_____ 。
(2)依据以物质的____ 为标准分类,属于酸的是____ (填序号,下同),属于盐的是____ ,属于氧化物的是_____ 。
(1)依据通常状况下物质的
(2)依据以物质的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 如图所示,依据一定的标准,对下列五种物质进行分类。回答下列问题:

(1)“分类标准1”是按所含物质的种类差异进行分类,则“类别1”涉及的物质属于_______ ,“分类标准2”是按电离产生的离子差异进行分类,则“类别2”涉及的物质属于_______ 。
(2) 易溶于水,写出
易溶于水,写出 在水中发生电离的方程式:
在水中发生电离的方程式:_______ ,部分 与水作用可形成氢氧化铝胶体,氢氧化铝胶体具有净水作用,这利用了该胶体的
与水作用可形成氢氧化铝胶体,氢氧化铝胶体具有净水作用,这利用了该胶体的_______ 性。检验 溶于水后的分散系中存在氢氧化铝胶体的简便方法是
溶于水后的分散系中存在氢氧化铝胶体的简便方法是_______ 。
(3)利用图中两种物质在加热条件下反应可产生氨气,写出反应的化学方程式:_______ 。
(4)将含有杂质离子的氢氧化铁胶体置于装置中,氢氧化铁胶体中的一些离子杂质可透过半透膜进入烧杯中,从而提纯氢氧化铁胶体,该分离原理与下图中的_______ (填字母)类似。

(5)已知空气的平均摩尔质量为 。则常温、常压下,
。则常温、常压下, 的密度是空气密度的
的密度是空气密度的_______ 倍(保留1位小数)。

(1)“分类标准1”是按所含物质的种类差异进行分类,则“类别1”涉及的物质属于
(2)
 易溶于水,写出
易溶于水,写出 在水中发生电离的方程式:
在水中发生电离的方程式: 与水作用可形成氢氧化铝胶体,氢氧化铝胶体具有净水作用,这利用了该胶体的
与水作用可形成氢氧化铝胶体,氢氧化铝胶体具有净水作用,这利用了该胶体的 溶于水后的分散系中存在氢氧化铝胶体的简便方法是
溶于水后的分散系中存在氢氧化铝胶体的简便方法是(3)利用图中两种物质在加热条件下反应可产生氨气,写出反应的化学方程式:
(4)将含有杂质离子的氢氧化铁胶体置于装置中,氢氧化铁胶体中的一些离子杂质可透过半透膜进入烧杯中,从而提纯氢氧化铁胶体,该分离原理与下图中的

(5)已知空气的平均摩尔质量为
 。则常温、常压下,
。则常温、常压下, 的密度是空气密度的
的密度是空气密度的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】胶体金即金溶胶,其具有光吸收性、呈色性和胶体性等特点。免疫胶体金技术作为胶体金标记物,可实现对抗原抗体的测定。用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。
其操作步骤如下:
a.取20%白磷的乙醚溶液0.5mL,加蒸馏水60mL。
b.先滴加1%氯化金水溶液0.75mL,再滴加一定浓度的K2CO3溶液0.6mL,振荡变成棕红色。
c.加热煮沸至溶液变成透明红色。
d.分离提纯,除去无机溶质。
所得分散系中,金颗粒直径在5—10nm之间。
请回答下列问题:
(1)从分散系粒子大小角度,该分散系属于___________ ,其分散质是___________ 。
(2)“分离提纯”步骤中,分离方法在化学中叫______ (填“蒸发”、“过滤”、“蒸馏”、“渗析”、“萃取”、“分液”、“升华”),证明 进入无机溶质的操作方法为:
进入无机溶质的操作方法为:___________ 。
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
a.若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是______ 。
A.冷水 B.沸水 C. NaOH溶液 D. NaCl溶液
b.制备Fe(OH)3胶体对应的离子方程式为:______
c.向FeCl3溶液分别滴入NaOH溶液对应的离子方程式为:______
向Fe(OH)3胶体中逐滴加稀盐酸,结果出现了一系列变化。先出现红褐色沉淀,原因是______ 。随后沉淀溶解,此反应的离子方程式是______ 。
其操作步骤如下:
a.取20%白磷的乙醚溶液0.5mL,加蒸馏水60mL。
b.先滴加1%氯化金水溶液0.75mL,再滴加一定浓度的K2CO3溶液0.6mL,振荡变成棕红色。
c.加热煮沸至溶液变成透明红色。
d.分离提纯,除去无机溶质。
所得分散系中,金颗粒直径在5—10nm之间。
请回答下列问题:
(1)从分散系粒子大小角度,该分散系属于
(2)“分离提纯”步骤中,分离方法在化学中叫
 进入无机溶质的操作方法为:
进入无机溶质的操作方法为:(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
a.若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C. NaOH溶液 D. NaCl溶液
b.制备Fe(OH)3胶体对应的离子方程式为:
c.向FeCl3溶液分别滴入NaOH溶液对应的离子方程式为:
向Fe(OH)3胶体中逐滴加稀盐酸,结果出现了一系列变化。先出现红褐色沉淀,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为了能观察到丁达尔效应,一中鼹鼠科学社的同学在实验室制备Fe(OH)3胶体。
(1)胶体与其他分散系的本质区别是:___ 。
(2)制备时,将______ 逐滴滴加至______ 中,待液体呈______ 后,停止加热;反应方程式为______ 。
(3)有一种橘红色的硫化锑(Sb2S3)胶体,装入U型管,插入电极后通直流电,发现阳极附近橘红色加深,这叫______ 现象,证明Sb2S3胶粒带______ 电荷。
(1)胶体与其他分散系的本质区别是:
(2)制备时,将
(3)有一种橘红色的硫化锑(Sb2S3)胶体,装入U型管,插入电极后通直流电,发现阳极附近橘红色加深,这叫
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.(1)实验室常用石灰石与盐酸反应制取CO2,请写出该反应的离子方程式__________ 。
(2)实验室常用锌粒与稀硫酸制取氢气,请写出该反应的离子方程式__________ 。
Ⅱ.(1)实验室常将饱和三氯化铁溶液滴入沸水中继续加热至红褐色制备氢氧化铁胶体,请写出制备氢氧化铁胶体的化学方程式___________ 。
(2)将Fe(OH)3 胶体装入U形管内,用石墨做电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐加深,这表明Fe(OH)3胶体微粒带_________ (填“正”或“负”)电荷。
(3)取少量Fe(OH)3 胶体于试管中,逐滴加入硫酸至过量,可看到的现象是____________ 。
(4)3.4gOH-中有_________ mol OH-,其含有的电子数是_______ 个(阿伏伽德罗常数用NA表示)。在同温同压下CH4和N2组成的混合气体对H2的相对密度为10,则混合气体中CH4与N2的体积比为_____ 。
(2)实验室常用锌粒与稀硫酸制取氢气,请写出该反应的离子方程式
Ⅱ.(1)实验室常将饱和三氯化铁溶液滴入沸水中继续加热至红褐色制备氢氧化铁胶体,请写出制备氢氧化铁胶体的化学方程式
(2)将Fe(OH)3 胶体装入U形管内,用石墨做电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐加深,这表明Fe(OH)3胶体微粒带
(3)取少量Fe(OH)3 胶体于试管中,逐滴加入硫酸至过量,可看到的现象是
(4)3.4gOH-中有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知下列九种物质:①H2O,②Al,③CO2,④盐酸,⑤硫酸钡,⑥NaOH⑦饱和FeCl3溶液,⑧氨水,⑨乙醇。根据上述提供的物质,回答下列问题:
(1)属于电解质的是_______________________ (填序号),属于非电解质__________ (填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为_________________________________________________________________________ 。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________ (填序号),反应的离子方程式为____________________________________________________________________________ 。
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:______________________________ ; ____________________________________________________________ 。
(1)属于电解质的是
(2)上述物质间发生的某反应的离子方程式为H++OH−===H2O,则该反应的化学方程式为
(3)实验室制备少量Fe(OH)3胶体所用的物质有
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计以下实验。

(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是_______ ,该反应中氧化剂是_______ 。
(2)如下图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色_______ 。
②写出上述过程中有关反应的化学方程式A→B_______ 。
③ 变化中可看到的现象是
变化中可看到的现象是_______ 。
④将A的饱和溶液滴入沸水中并不断加热,可制得_______ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为_______ 效应。

(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是
(2)如下图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色
②写出上述过程中有关反应的化学方程式A→B
③
 变化中可看到的现象是
变化中可看到的现象是④将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的 FeCl3 溶液继续煮沸, 至液体呈透明的红褐色。
(1)反应原理为___________ ,判断胶体的制备是否成功,可利用的物理方法是___________ 。
(2)甲同学向沸水中滴加饱和氯化铁溶液后,长时间加热,会看到___________ 。
(3)乙同学按要求制备了 Fe(OH)3 胶体,又向 Fe(OH)3 胶体中逐滴加入了稀 H2SO4,结果出现了一系列变化:
①先出现红褐色沉淀,原因是___________ 。
②随后沉淀溶解,此反应的离子方程式是___________ 。
(4)丙同学将氢氧化铁胶体进行电泳实验发现___________ (填“阴极”、“阳极”)颜色加深,说明氢氧化铁胶粒带___________ (填“正电”或“负电”)。
(1)反应原理为
(2)甲同学向沸水中滴加饱和氯化铁溶液后,长时间加热,会看到
(3)乙同学按要求制备了 Fe(OH)3 胶体,又向 Fe(OH)3 胶体中逐滴加入了稀 H2SO4,结果出现了一系列变化:
①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
(4)丙同学将氢氧化铁胶体进行电泳实验发现
您最近一年使用:0次



