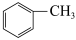
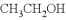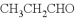写出下列有机反应的化学方程式。
(1)乙二酸与乙二醇酯化反应生成高聚酯:_______ 。
(2)HOOCCH2CHO与足量新制Cu(OH)2溶液的反应:_______ 。
(3)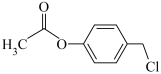 在足量NaOH溶液中的水解反应:
在足量NaOH溶液中的水解反应:_______ 。
(1)乙二酸与乙二醇酯化反应生成高聚酯:
(2)HOOCCH2CHO与足量新制Cu(OH)2溶液的反应:
(3)
 在足量NaOH溶液中的水解反应:
在足量NaOH溶液中的水解反应:
更新时间:2023-03-09 10:35:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在下列物质中选择合适的物质的序号 填空:①苯②乙醇③乙酸④乙酸乙酯。
(1)在加热有铜作催化剂的条件下,被氧化后的产物能发生银镜反应的是____ ;该催化氧化反应的化学方程式为______________________ 。
(2)在浓硫酸和加热条件下,能发生酯化反应的是_______________________ ;
(3)既能发生加成反应又能发生取代反应的是____ ;
(4)在无机酸或碱作用下,能发生水解反应的是____ ;写出其在碱性条件下水解的化学方程式_______________________________ 。
(1)在加热有铜作催化剂的条件下,被氧化后的产物能发生银镜反应的是
(2)在浓硫酸和加热条件下,能发生酯化反应的是
(3)既能发生加成反应又能发生取代反应的是
(4)在无机酸或碱作用下,能发生水解反应的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】丙烯是石油化工的重要原料,一定条件下可发生下列转化:
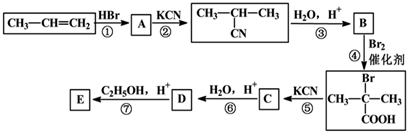
已知: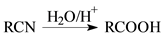
(1)A的结构简式为:____________ ;
(2)反应④的类型为:_________________ 反应;反应⑦进行所需的条件是:_________ 。
(3)D与足量乙醇反应生成E的化学方程式为:__________________ 。
(4)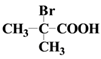 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为_________________ 。
(5)B的同分异构体有多种.写出其中一种既能发生银镜反应,又能发生酯化反应,并且核磁共振氢谱峰值为6:1:1的同分异构体的结构简式:_____________________ 。
(6)请写出以丙烯为原料制备聚2-羟基丙酸的合成路线,无机试剂任选。______________
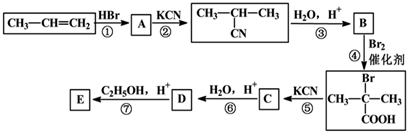
已知:
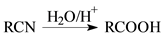
(1)A的结构简式为:
(2)反应④的类型为:
(3)D与足量乙醇反应生成E的化学方程式为:
(4)
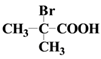 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为(5)B的同分异构体有多种.写出其中一种既能发生银镜反应,又能发生酯化反应,并且核磁共振氢谱峰值为6:1:1的同分异构体的结构简式:
(6)请写出以丙烯为原料制备聚2-羟基丙酸的合成路线,无机试剂任选。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)写出下列有机物的官能团名称:
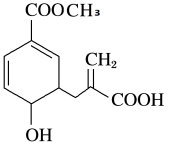
_________________________
(2)书写以下化学方程式
①乙烯与溴水的加成反应__________________________________________________
②氯乙烯的加聚反应______________________________________________________
③ 在碱性条件下的水解反应
在碱性条件下的水解反应_________________________________

(2)书写以下化学方程式
①乙烯与溴水的加成反应
②氯乙烯的加聚反应
③
 在碱性条件下的水解反应
在碱性条件下的水解反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知乳酸的结构简式为:

(1)则90g乳酸与足量金属钠反应产生的气体在标准状况下的体积是_____________ L,方程式为______________________________________________________
(2)乳酸发生消去反应的条件__________ ;生成有机物的结构简式_____________ 。
(3)已知两分子乳酸可在一定条件下反应生成环状的酯,写出该酯的结构简式:_____________________ 。

(1)则90g乳酸与足量金属钠反应产生的气体在标准状况下的体积是
(2)乳酸发生消去反应的条件
(3)已知两分子乳酸可在一定条件下反应生成环状的酯,写出该酯的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】由γ-羟基丁酸(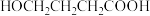 )生成γ-丁内酯(
)生成γ-丁内酯( )的反应为:
)的反应为:

(1)上述反应的反应类型是_______ ,写出γ-羟基丁酸中官能团的名称_______
(2)在25℃时,溶液中γ-羟基丁酸的初始浓度为0.200mol/L,随着反应的进行,测得γ-丁内酯浓度随时间的变化如表所示。
①该反应达到平衡后,升高温度,平衡_______ 移动(填“正向”“不”或“逆向”)。
②在50min时,γ-羟基丁酸的转化率为_______
③为提高平衡时γ-羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是_______
④25℃时,该反应的平衡常数K_______ (结果保留两位小数),在25℃时,当γ-丁内酯与γ-羟基丁酸的物质的量浓度之比保持不变时,反应_______ 达到平横(填“一定”或“不一定”)
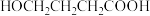 )生成γ-丁内酯(
)生成γ-丁内酯( )的反应为:
)的反应为:

(1)上述反应的反应类型是
(2)在25℃时,溶液中γ-羟基丁酸的初始浓度为0.200mol/L,随着反应的进行,测得γ-丁内酯浓度随时间的变化如表所示。
| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
| c(mol/L) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
②在50min时,γ-羟基丁酸的转化率为
③为提高平衡时γ-羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是
④25℃时,该反应的平衡常数K
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】有时候,化学如同魔法一般,让人捉摸不透……
(1)直至2022年7月24日11时,我国的“问天”实验舱已经进入了发射倒计时。“问天”实验舱是中国空间站“天宫”的组成部分,舱段规模20吨级,主要面向空间生命科学研究,而他的发动机——大推力氢氧发动机YF-77也十分引人注目。已知氢氧发动机内部可以简化为燃料电池,写出此电池的总反应方程式:_______ 并写出使用液氧液氢做燃料的一个优势:_______ 。
(2)写出HOOCCOOH和HOCH2CH2OH反应生成六元环化合物的反应方程式:_______ 。
(3)已知Fe(OH)2在常温无氧条件下会发生分解,转化为Fe3O4,且该反应为涉及到两种元素变价,写出其反应方程式:_______ 。
(4)写出氢氧化铁溶解在氢碘酸溶液中的离子方程式:_______ 。
(1)直至2022年7月24日11时,我国的“问天”实验舱已经进入了发射倒计时。“问天”实验舱是中国空间站“天宫”的组成部分,舱段规模20吨级,主要面向空间生命科学研究,而他的发动机——大推力氢氧发动机YF-77也十分引人注目。已知氢氧发动机内部可以简化为燃料电池,写出此电池的总反应方程式:
(2)写出HOOCCOOH和HOCH2CH2OH反应生成六元环化合物的反应方程式:
(3)已知Fe(OH)2在常温无氧条件下会发生分解,转化为Fe3O4,且该反应为涉及到两种元素变价,写出其反应方程式:
(4)写出氢氧化铁溶解在氢碘酸溶液中的离子方程式:
您最近一年使用:0次
【推荐1】下列实验方案合理的是_______ (填选项)。
A.配制银氨溶液:在一定量的AgNO3溶液中,逐滴滴加氨水至最初生成的沉淀恰好溶解为止
B.在检验醛基配制Cu(OH)2悬浊液时,在一定量CuSO4溶液中,加入少量NaOH溶液
C.验证RX为碘代烷,把RX与烧碱水溶液混合加热,将溶液冷却后再加入硝酸银溶液
D.无水乙醇和浓硫酸共热至170℃,将制得的气体通入酸性高锰酸钾溶液中,可检验制得的气体是否为乙烯
E.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
F.除去混合苯中的少量苯酚,加入过量溴水,过滤
G.实验室制取乙烯时,必须将温度计的水银球插入反应液中,测定反应液的温度
A.配制银氨溶液:在一定量的AgNO3溶液中,逐滴滴加氨水至最初生成的沉淀恰好溶解为止
B.在检验醛基配制Cu(OH)2悬浊液时,在一定量CuSO4溶液中,加入少量NaOH溶液
C.验证RX为碘代烷,把RX与烧碱水溶液混合加热,将溶液冷却后再加入硝酸银溶液
D.无水乙醇和浓硫酸共热至170℃,将制得的气体通入酸性高锰酸钾溶液中,可检验制得的气体是否为乙烯
E.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
F.除去混合苯中的少量苯酚,加入过量溴水,过滤
G.实验室制取乙烯时,必须将温度计的水银球插入反应液中,测定反应液的温度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(I)有下列物质①己烯②苯③己烷④异丙醇⑤乙醇⑥乙醛⑦乙酸⑧苯酚⑨聚乙烯⑩甲酸乙酯,其中:
(1)能使酸性高锰酸钾溶液褪色的是______ ;
(2)常温下能和溴水反应的是______ ;
(3)能和金属钠反应放出氢气的是______ ;
(4)能和FeCl3溶液反应产生紫色物质的是______ ;
(5)在一定条件下能与新制Cu(OH)2反应的是______ ;
(6)在一定条件下能与NaOH溶液反应的是______ ;
(7)能与NaHCO3溶液反应的是______ ;
(II)完成下列填空。
①乙二醇与HOOCCH2CH2COOH发生缩聚,得到的聚酯结构简式为______ 。
②CH3CHO与新制的氢氧化铜反应的化学方程式______ 。
③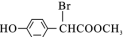 与NaOH水溶液共热反应的化学方程式
与NaOH水溶液共热反应的化学方程式______ 。
④(CH3)2CHOH在铜催化的条件下反应方程式______ 。
(III)以下实验操作方法以及结论不正确的有______ 。
①通过与金属钠反应放出氢气的速率判断酸性强弱:乙酸>乙醇>苯酚
②检验淀粉是否水解完全的方法是:在水解液中先加入过量的氢氧化钠溶液,然后滴加碘水,未变蓝,说明已水解完全
③将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是否为还原性糖
④用足量的NaOH溶液与矿物油和地沟油加热,可鉴别出地沟油
⑤用燃烧的方法鉴别乙醇、四氯化碳、苯
⑥将铜丝在酒精灯外焰上加热变黑后移至内焰,铜丝恢复原来的红色
(1)能使酸性高锰酸钾溶液褪色的是
(2)常温下能和溴水反应的是
(3)能和金属钠反应放出氢气的是
(4)能和FeCl3溶液反应产生紫色物质的是
(5)在一定条件下能与新制Cu(OH)2反应的是
(6)在一定条件下能与NaOH溶液反应的是
(7)能与NaHCO3溶液反应的是
(II)完成下列填空。
①乙二醇与HOOCCH2CH2COOH发生缩聚,得到的聚酯结构简式为
②CH3CHO与新制的氢氧化铜反应的化学方程式
③
 与NaOH水溶液共热反应的化学方程式
与NaOH水溶液共热反应的化学方程式④(CH3)2CHOH在铜催化的条件下反应方程式
(III)以下实验操作方法以及结论不正确的有
①通过与金属钠反应放出氢气的速率判断酸性强弱:乙酸>乙醇>苯酚
②检验淀粉是否水解完全的方法是:在水解液中先加入过量的氢氧化钠溶液,然后滴加碘水,未变蓝,说明已水解完全
③将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是否为还原性糖
④用足量的NaOH溶液与矿物油和地沟油加热,可鉴别出地沟油
⑤用燃烧的方法鉴别乙醇、四氯化碳、苯
⑥将铜丝在酒精灯外焰上加热变黑后移至内焰,铜丝恢复原来的红色
您最近一年使用:0次