下列操作不能达到实验目的的是
| 选项 | 目的 | 操作 |
| A | 测定氯水的pH | 用玻璃棒蘸取饱和氯水点在置于玻璃片的pH试纸上,稍后与标准比色卡对照 |
| B | 检验某溶液中只含 不含 不含 | 先向该溶液中滴加KSCN溶液,再滴加少量氯水 |
| C | 制取氢氧化铁胶体 | 向40 mL沸水中滴加5~6滴饱和 溶液,继续煮沸直到形成红褐色液体停止加热 溶液,继续煮沸直到形成红褐色液体停止加热 |
| D | 验证 的还原性强于 的还原性强于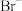 | 向 溶液中加入少量氯水,再加 溶液中加入少量氯水,再加 ,振荡 ,振荡 |
| A.A | B.B | C.C | D.D |
22-23高一上·辽宁抚顺·期末 查看更多[2]
更新时间:2023-04-26 13:23:43
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作可以达到实验目的的是
实验目的 | 实验操作 | |
A | 制备 | 将 |
B | 比较Al和Fe的金属性强弱 | 将Al、Fe、NaOH溶液组成原电池 |
C | 除去 | 通入盛有饱和 |
D | 除去Cu粉中混有的CuO | 加入稀硝酸,过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】历经十年传承积淀,形成精湛的东阿阿胶传统工艺,包括洗皮、泡皮、晾皮、刮毛、铡皮、化皮、打沫、除渣、浓缩、挂旗、凝胶、切胶等工序。下列工序与化学实验中的原理不具有对应关系的是
| 选项 | A | B | C | D |
| 工序 |
|
|
|
|
| 化学实验 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列各项说法正确 的是( )
①“卤水点豆腐”、“黄河入海口处的沙洲形成”都与胶体的聚沉有关
②向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
③沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
④明矾能作净水剂是因为铝离子与水作用生成氢氧化铝胶体具有吸附悬浮杂质的作用
⑤在制备Fe(OH)3胶体实验中,用一束激光照射,若有一条光亮的通路,则证明有Fe(OH)3胶体生成
⑥向Fe(OH)3胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解为黄色溶液
⑦若将Fe(OH)3胶体提纯,可以采用的方法是过滤
①“卤水点豆腐”、“黄河入海口处的沙洲形成”都与胶体的聚沉有关
②向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
③沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
④明矾能作净水剂是因为铝离子与水作用生成氢氧化铝胶体具有吸附悬浮杂质的作用
⑤在制备Fe(OH)3胶体实验中,用一束激光照射,若有一条光亮的通路,则证明有Fe(OH)3胶体生成
⑥向Fe(OH)3胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解为黄色溶液
⑦若将Fe(OH)3胶体提纯,可以采用的方法是过滤
| A.①③④⑥⑦ | B.②③⑥④⑤⑥ | C.①②④⑤⑥ | D.③④⑤⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的项有
①根据酸中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
②“卤水点豆腐”“黄河入海口处三角洲的形成”都与胶体的性质有关
③向Fe(OH)3胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解形成黄色溶液
④SO2气体溶于水能导电,所以SO2是电解质
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
⑥金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
⑦测定新制氯水的pH时,先用玻璃棒蘸取液体滴在pH试纸上,再与标准比色卡对照
①根据酸中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
②“卤水点豆腐”“黄河入海口处三角洲的形成”都与胶体的性质有关
③向Fe(OH)3胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解形成黄色溶液
④SO2气体溶于水能导电,所以SO2是电解质
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
⑥金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
⑦测定新制氯水的pH时,先用玻璃棒蘸取液体滴在pH试纸上,再与标准比色卡对照
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HA和HB两种酸分别与足量的铁粉反应,用排水法收集气体 | HA放出的氢气多且反应速率快 | 酸的强弱:HA<HB |
| B | 向2mL0.1mol/LAgNO3溶液中滴2滴0.1mol/LNaCl溶液,再滴2滴0.1mol/LKI溶液 | 先生成白色沉淀,后生成黄色沉淀 | 溶度积(Ksp);AgCl>AgI |
| C | 向新制氯水中滴加紫色石蕊试液 | 溶液变为红色且保持不变 | 新制氯水具有酸性 |
| D | 常温下,用pH计分别测定饱和NaX溶液和饱和NaY溶液的pH | pH:NaX>NaY | 常温下酸性:HX<HY |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】下列实验操作或结论正确的是
| A.在某溶液中加入AgNO3溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶液中一定有Cl- |
B.向某溶液中加过量BaCl2,若产生白色沉淀,则证明有 |
C.某溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,说明原溶液中一定存在 |
| D.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中可能含有Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热,冷却后,取少量溶液,加入AgNO3溶液 | 若有沉淀产生,则CH3CH2Br发生水解 |
| B | 比较Br2和I2的氧化性强弱 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 | 若下层液体呈紫红色,则Br2的氧化性强于I2 |
| C | 检验Fe(NO3)2晶体是否氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 若溶液变红,则Fe(NO3)2晶体已氧化变质 |
| D | 比较HNO2和CH3COOH电离出H+的能力 | 用pH试纸分别测CH3COONa溶液和NaNO2溶液的pH | 若CH3COONa溶液的pH比NaNO2溶液的pH大,则HNO2电离出H+的能力比CH3COOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列指定反应的离子方程式书写不正确 的是
| A.用醋酸(CH3COOH)除去水壶水垢(CaCO3):CaCO3+2H+=Ca2++CO2↑+H2O |
| B.向漂白粉溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| C.钠在水中的反应:2Na+2H2O=2Na++2OH-+H2↑ |
| D.氯气通入氯化亚铁溶液中:2Fe2++Cl2=2Fe3++2Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列含Fe元素的物质反应的离子方程式书写正确的是
A.铁与盐酸反应: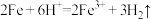 |
B.钠与氯化铁溶液反应: |
C.氧化铁与稀硫酸反应: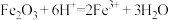 |
D.氯化亚铁溶液与氯气反应: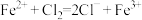 |
您最近一年使用:0次

 胶体
胶体 中混有的HCl气体
中混有的HCl气体 溶液的洗气瓶
溶液的洗气瓶




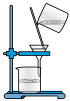
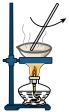
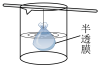
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O 等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是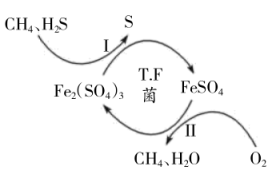
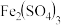 溶液
溶液 接氧化
接氧化 可用于治疗缺铁性贫血
可用于治疗缺铁性贫血

