50mL0.50 mol·L-1的盐酸与50mL0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应。实验数据如下表:
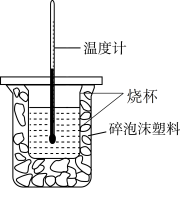
近似认为0.50 mol·L-1NaOH溶液和0.50 mol·L-1HCl溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。
请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是___________ 。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值___________ (填“偏大” “偏小”或“无影响”)。则中和热ΔH=___________ (取小数点后一位)。
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |

近似认为0.50 mol·L-1NaOH溶液和0.50 mol·L-1HCl溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。
请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)大烧杯上如不盖硬纸板,则求得的中和热数值
更新时间:2023/06/08 17:05:05
|
【知识点】 中和热的测定与误差分析解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】用图中装置测定中和反应热的测定步骤如下:
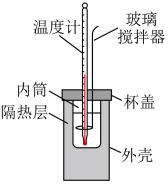
I.测量反应的温度。
①用量筒量取50mL 0.50 盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度。用水把温度计上的酸冲洗干净,擦干备用。
盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度。用水把温度计上的酸冲洗干净,擦干备用。
②用另一个量筒量取50mL 0.55 NaOH溶液,用温度计测量并记录NaOH溶液的温度。
NaOH溶液,用温度计测量并记录NaOH溶液的温度。
II.测量反应后体系的温度。
打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内筒,立即盖上杯盖,插入温度计,用搅拌器匀速搅拌;密切关注温度变化,将最高温度记为反应后体系的温度( )。
)。
III.重复测定2次,数据记录见下表。
注:稀盐酸和稀碱密度近似为1 ,混合液的比热容:4.18J(g·℃)。
,混合液的比热容:4.18J(g·℃)。
完成以下问题:
(1)上述操作中将NaOH溶液迅速倒入最热计的内筒,并立即盖上杯盖的目的是___________ 。
(2)测量过程中,测量盐酸后未清洗温度计即用来测量NaOH溶液温度,其他过程无误,测得反应热的绝对值_____ (填“偏大”“不变”或“偏小”,下同);反应后NaOH剩余,测得反应热的数值_____ 。
(3)计算此反应热的数值Q=______ kJ,写出中和热(生成1mol  )的热化学方程式
)的热化学方程式______ 。

I.测量反应的温度。
①用量筒量取50mL 0.50
 盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度。用水把温度计上的酸冲洗干净,擦干备用。
盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度。用水把温度计上的酸冲洗干净,擦干备用。②用另一个量筒量取50mL 0.55
 NaOH溶液,用温度计测量并记录NaOH溶液的温度。
NaOH溶液,用温度计测量并记录NaOH溶液的温度。II.测量反应后体系的温度。
打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内筒,立即盖上杯盖,插入温度计,用搅拌器匀速搅拌;密切关注温度变化,将最高温度记为反应后体系的温度(
 )。
)。III.重复测定2次,数据记录见下表。
| 实验次数 | 反应物温度/℃ | 反应前体系温度 | 反应后体系温度 | 温度差 | |
| 盐酸 | NaOH溶液 |  /℃ /℃ |  /℃ /℃ |  /℃ /℃ | |
| 1 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 |
| 2 | 24.8 | 25.0 | 24.9 | 28.1 | 3.2 |
| 3 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 |
 ,混合液的比热容:4.18J(g·℃)。
,混合液的比热容:4.18J(g·℃)。完成以下问题:
(1)上述操作中将NaOH溶液迅速倒入最热计的内筒,并立即盖上杯盖的目的是
(2)测量过程中,测量盐酸后未清洗温度计即用来测量NaOH溶液温度,其他过程无误,测得反应热的绝对值
(3)计算此反应热的数值Q=
 )的热化学方程式
)的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
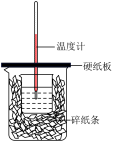
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_______ ,除此之外,装置中的一个明显错误是_______ 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_______ ,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求中和热_______ (填“相等”或“不相等”),简述理由:_______ 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),根据计算结果,写出该中和反应的热化学方程式_______ 。

(1)从上图实验装置看,其中尚缺少的一种玻璃用品是
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求中和热
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
| 3 | 25.1 | 25.1 | 25.1 | 27.1 | 2.0 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃仪器是______________ 。
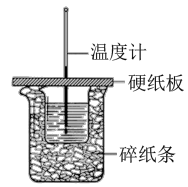
(2)烧杯间填满碎纸条的作用是________________________ 。
(3)若大烧杯上不盖硬纸板,求得的中和热ΔH___ (填“偏大”“偏小”或“无影响”)。
(4)实验用50 mL 0.50 mol·L-1盐酸与 50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应,若改用 60 mL 0.50 mol·L-1盐酸与 60 mL 0.55 mol·L-1 NaOH溶液进行反应,两个实验相比,所放出的热量__________ (填“相等”或“不相等”),所求中和热__________ (填“相等”或“不相等”)
(5)现取 50 mL 0.50 mol·L-1 NaOH溶液和 30 mL 0.50 mol·L-1硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
②近似认为 0.50 mol·L-1 NaOH溶液和 0.50 mol·L-1硫酸溶液的密度都是 1.0 g·mL-1,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则生成 1 mol H2O(l)时的反应热ΔH=_______ (取小数点后一位)。
(1)从实验装置上看,图中缺少的一种玻璃仪器是

(2)烧杯间填满碎纸条的作用是
(3)若大烧杯上不盖硬纸板,求得的中和热ΔH
(4)实验用50 mL 0.50 mol·L-1盐酸与 50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应,若改用 60 mL 0.50 mol·L-1盐酸与 60 mL 0.55 mol·L-1 NaOH溶液进行反应,两个实验相比,所放出的热量
(5)现取 50 mL 0.50 mol·L-1 NaOH溶液和 30 mL 0.50 mol·L-1硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
| 温度 次数 | 起始温度t1/℃ | 终止温 度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
您最近一年使用:0次



