现有下列10种物质:①冰水混合物;②有色玻璃;③ ;④
;④ ;⑤熔融
;⑤熔融 ;⑥
;⑥ 溶液;⑦蛋白质胶体;⑧
溶液;⑦蛋白质胶体;⑧ 溶液;⑨乙醇;⑩固体
溶液;⑨乙醇;⑩固体 。
。
(1)属于分散系的是___________ ,属于强电解质且能导电的是___________ ,属于非电解质的是___________ 。
(2)⑥和⑦本质区别是___________ 。
(3)已知⑧是二元弱酸,请写出其与 溶液反应生成酸式盐的化学式
溶液反应生成酸式盐的化学式___________ 。
(4)将⑩溶于水,写出电离方程式___________ 。下列物质加入⑩的水溶液中可能有气泡产生的是___________ 。
A.金属单质 B.碱性氧化物 C.碱 D.某些盐
(5)含有相同物质的量溶质的⑥和⑩的水溶液混合,应后溶液呈___________ 性(选A表示“酸”、B表示“中”或C表示“碱”),发生反应的离子方程式为___________ 。
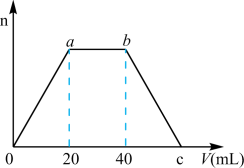
(6)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是___________  ;混合溶液中
;混合溶液中 和
和 的物质的量之比为
的物质的量之比为___________ ;写出 段发生的离子方程式。
段发生的离子方程式。___________ 。
 ;④
;④ ;⑤熔融
;⑤熔融 ;⑥
;⑥ 溶液;⑦蛋白质胶体;⑧
溶液;⑦蛋白质胶体;⑧ 溶液;⑨乙醇;⑩固体
溶液;⑨乙醇;⑩固体 。
。(1)属于分散系的是
(2)⑥和⑦本质区别是
(3)已知⑧是二元弱酸,请写出其与
 溶液反应生成酸式盐的化学式
溶液反应生成酸式盐的化学式(4)将⑩溶于水,写出电离方程式
A.金属单质 B.碱性氧化物 C.碱 D.某些盐
(5)含有相同物质的量溶质的⑥和⑩的水溶液混合,应后溶液呈
(6)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是
 ;混合溶液中
;混合溶液中 和
和 的物质的量之比为
的物质的量之比为 段发生的离子方程式。
段发生的离子方程式。
更新时间:2023-10-15 09:45:45
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Mg的结构特性类似于铝,可作飞机、导弹的合金材料。海水提取镁的流程如下:
i.制备石灰乳:将含有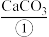 的大理石通过高温加热,随后形成
的大理石通过高温加热,随后形成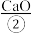 和
和 。
。 加入水中会形成石灰乳[含有部分未溶解的
加入水中会形成石灰乳[含有部分未溶解的 ]。
]。
ii.沉淀:将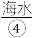 引入沉淀池中,海水中的
引入沉淀池中,海水中的 和石灰乳会发生化学反应生皮
和石灰乳会发生化学反应生皮 。
。
iii.酸化:让 与
与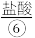 发生反应。
发生反应。
iv.蒸发结晶:将氯化镁溶液蒸发浓缩、冷却结晶得到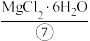 。
。
v.脱水:在 的气流中将
的气流中将 脱水制成
脱水制成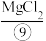 。
。
vi.电解:电解熔融 得到
得到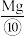 和
和 。
。
回答下列问题:
(1)常温下,上述标有序号的物质中,能导电的是___________ (填序号,下同);属于酸性氧化物的是___________ 。
(2)石灰乳属于___________ (填“溶液”、“胶体”或“浊液”),沉淀时发生反应的离子方程式为___________ 。
(3)酸化时的化学方程式为___________ ;蒸发结晶需要用到的仪器为___________ (填标号)。

(4)高温下铝粉和氧化铁可以发生置换反应,该反应的化学方程式为___________ ;甲同学提出用铝粉与MgSO4溶液反应来制备镁单质,乙同学认为甲同学的方法不合理,乙同学的理由可能是___________ 。
i.制备石灰乳:将含有
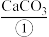 的大理石通过高温加热,随后形成
的大理石通过高温加热,随后形成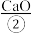 和
和 。
。 加入水中会形成石灰乳[含有部分未溶解的
加入水中会形成石灰乳[含有部分未溶解的 ]。
]。ii.沉淀:将
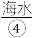 引入沉淀池中,海水中的
引入沉淀池中,海水中的 和石灰乳会发生化学反应生皮
和石灰乳会发生化学反应生皮 。
。iii.酸化:让
 与
与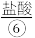 发生反应。
发生反应。iv.蒸发结晶:将氯化镁溶液蒸发浓缩、冷却结晶得到
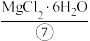 。
。v.脱水:在
 的气流中将
的气流中将 脱水制成
脱水制成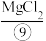 。
。vi.电解:电解熔融
 得到
得到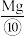 和
和 。
。回答下列问题:
(1)常温下,上述标有序号的物质中,能导电的是
(2)石灰乳属于
(3)酸化时的化学方程式为

(4)高温下铝粉和氧化铁可以发生置换反应,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识填写下列空白
(1)以下物质:① ②醋酸③氨水 ④熔融
②醋酸③氨水 ④熔融 ⑤蔗糖 ⑥液氮 ⑦
⑤蔗糖 ⑥液氮 ⑦ ;现状态下能导电的是
;现状态下能导电的是_______ (填序号,下同);属于非电解质的是_______ 。
(2)在标准状况下,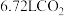 质量为
质量为_______  ,其中含有的氧原子数目约为
,其中含有的氧原子数目约为_______ 。
(3) 是一种酸性氧化物,可制取
是一种酸性氧化物,可制取 ,从括号内所给试剂(
,从括号内所给试剂( 溶液、
溶液、 溶液、
溶液、 溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:_______ 。
(4) 可经过如图所示的转化制取
可经过如图所示的转化制取 ,已知“反应Ⅱ”为复分解反应。
,已知“反应Ⅱ”为复分解反应。
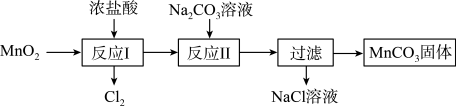
①写出“反应Ⅱ”的化学方程式:_______ 。
②过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为_______ 。
(1)以下物质:①
 ②醋酸③氨水 ④熔融
②醋酸③氨水 ④熔融 ⑤蔗糖 ⑥液氮 ⑦
⑤蔗糖 ⑥液氮 ⑦ ;现状态下能导电的是
;现状态下能导电的是(2)在标准状况下,
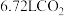 质量为
质量为 ,其中含有的氧原子数目约为
,其中含有的氧原子数目约为(3)
 是一种酸性氧化物,可制取
是一种酸性氧化物,可制取 ,从括号内所给试剂(
,从括号内所给试剂( 溶液、
溶液、 溶液、
溶液、 溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:(4)
 可经过如图所示的转化制取
可经过如图所示的转化制取 ,已知“反应Ⅱ”为复分解反应。
,已知“反应Ⅱ”为复分解反应。
①写出“反应Ⅱ”的化学方程式:
②过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:_______ 。
②有难溶性碱生成的离子反应方程式:_______ 。
(3)某兴趣小组的同学向一定体积的 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。

Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 、
、 、
、 、
、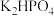 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。
(4) 属于
属于_______ 酸; 为
为_______ 盐(填序号)
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
| A.单质 | B.化合物 | C.水 | D.电解质 |
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:
②有难溶性碱生成的离子反应方程式:
(3)某兴趣小组的同学向一定体积的
 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
| A.XY段混合溶液的导电能力逐渐减弱,说明生成的白色沉淀BaSO,不是电解质 |
| B.a时刻,两溶液恰好完全反应 |
C.YZ段的导电能力不断增大,主要是由于 溶液电离出的离子导电 溶液电离出的离子导电 |
D.向一定体积的 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 |
Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
 、
、 、
、 、
、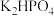 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。(4)
 属于
属于 为
为①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出
 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.在两份相同的 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
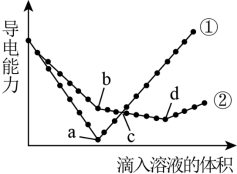
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题:
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题:
(1) 在水溶液中的电离方程式是
在水溶液中的电离方程式是___________ ; 属于“酸”、“碱”、“盐”中的
属于“酸”、“碱”、“盐”中的___________ ;图中代表滴加 溶液的变化曲线是
溶液的变化曲线是___________ (填“①”或“②”)。
(2)曲线①中a点导电能力最弱的原因是___________ (用离子方程式方程式表示);b点溶液中大量存在的离子是___________ 。
(3)c点两溶液中H+浓度:①___________ ②(填“>”、“<”或“=”,下同);d点对应的溶液显___________ (填“酸性”、“中性”、“碱性”)。
(4)曲线②中的b、d两点对应所加溶液的体积比为___________ 。
Ⅱ.硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:①准确称取17.700g样品,配制成100.00mL溶液A.②将A两等份,取一份,加入盐酸酸化的BaCl2溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65g。③另一份加适量稀硫酸酸化后,与50mL0.2mol/LKMnO 4溶液恰好完全反应。已知H2O2与KMnO4反应的化学方程式如下: 2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O
(5)通过计算确定样品的组成(写出计算过程)___________ 。
 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题:
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题:
(1)
 在水溶液中的电离方程式是
在水溶液中的电离方程式是 属于“酸”、“碱”、“盐”中的
属于“酸”、“碱”、“盐”中的 溶液的变化曲线是
溶液的变化曲线是(2)曲线①中a点导电能力最弱的原因是
(3)c点两溶液中H+浓度:①
(4)曲线②中的b、d两点对应所加溶液的体积比为
Ⅱ.硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:①准确称取17.700g样品,配制成100.00mL溶液A.②将A两等份,取一份,加入盐酸酸化的BaCl2溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65g。③另一份加适量稀硫酸酸化后,与50mL0.2mol/LKMnO 4溶液恰好完全反应。已知H2O2与KMnO4反应的化学方程式如下: 2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O
(5)通过计算确定样品的组成(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.回答下列问题
(1)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,得到氢氧化铁胶体。写出反应的化学方程式:___________ ,利用___________ 来鉴别溶液和胶体。
II.某小组在实验探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2mol/LBa(OH)2溶液中滴加0.1mol/L盐酸,测得溶液导电能力的变化如图所示,答案下列问题:

(2)上图中导电能力最弱的点为___________ 。
(3)Ba(OH)2的电离方程式为___________ 。
(4)A~B段发生反应的离子方程式是___________ 。
(5)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同___________ (填序号)。
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.NH3·H2O和HNO3
(6)Ba(OH)2溶液与CO2反应的离子方程式:___________ 。Ba(OH)2与NH4HSO4溶液以物质的量之比为1:1比例反应离子方程式:___________ 。
(1)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,得到氢氧化铁胶体。写出反应的化学方程式:
II.某小组在实验探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2mol/LBa(OH)2溶液中滴加0.1mol/L盐酸,测得溶液导电能力的变化如图所示,答案下列问题:

(2)上图中导电能力最弱的点为
(3)Ba(OH)2的电离方程式为
(4)A~B段发生反应的离子方程式是
(5)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同
A.Ba(OH)2和H2SO4 B.NaOH和H2SO4 C.NH3·H2O和HNO3
(6)Ba(OH)2溶液与CO2反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】以下都是中学化学常见的物质:①Ba(OH)2;②硫酸铝;③液态HCl;④稀硫酸;⑤二氧化碳;⑥铁;⑦碳酸钠;⑧蔗糖;⑨熔融氯化钠⑩CuSO4·5H2O,请按下列分类标准回答:
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)溶于水能电离出H+的电解质是___________ 。
(3)上述物质能导电的是___________ 。
(4)写出④溶液与⑥反应的离子方程式___________ 。
(5)写出⑤溶液与①反应的离子方程式___________ 。
(6)②在水中的电离方程式为___________ 。
(1)属于电解质的是
(2)溶于水能电离出H+的电解质是
(3)上述物质能导电的是
(4)写出④溶液与⑥反应的离子方程式
(5)写出⑤溶液与①反应的离子方程式
(6)②在水中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】填空。
(1)写出醋酸与NaOH溶液反应的离子方程式___________ 。
(2)在25℃、101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫气体,放出27kJ的热量,表示硫燃烧的热化学方程式为___________ 。
(3)已知某温度下有如下三个反应: ,
, ,
, 。则该温度下HF、HCN和
。则该温度下HF、HCN和 ,三种弱酸的电离常数由大到小的顺序是
,三种弱酸的电离常数由大到小的顺序是___________ 。
(4)在硫酸工业中,通过下列反应使 氧化为
氧化为 :
: ,在实际生产中,通入过量的空气,原因是
,在实际生产中,通入过量的空气,原因是___________ 。
(1)写出醋酸与NaOH溶液反应的离子方程式
(2)在25℃、101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫气体,放出27kJ的热量,表示硫燃烧的热化学方程式为
(3)已知某温度下有如下三个反应:
 ,
, ,
, 。则该温度下HF、HCN和
。则该温度下HF、HCN和 ,三种弱酸的电离常数由大到小的顺序是
,三种弱酸的电离常数由大到小的顺序是(4)在硫酸工业中,通过下列反应使
 氧化为
氧化为 :
: ,在实际生产中,通入过量的空气,原因是
,在实际生产中,通入过量的空气,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据已知信息回答下列各问:
I.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出H3PO2溶液与足量NaOH溶液反应的离子方程式___________ 。
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则Na2HPO4、NaH2PO2、Na2HPO3中属于酸式盐的是___________ (填化学式)。
II.NaHSO4可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是___________ 。
a.NaHSO4固体不能导电
b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质
d.NaHSO4溶液显中性
(4)NaHSO4溶液与NaHCO3溶液反应的离子方程式为___________ 。
III.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是___________ 。
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:___________ 。
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至Ba2+恰好沉淀完全,写出离子方程式:_____ 。
I.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出H3PO2溶液与足量NaOH溶液反应的离子方程式
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则Na2HPO4、NaH2PO2、Na2HPO3中属于酸式盐的是
II.NaHSO4可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是
a.NaHSO4固体不能导电
b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质
d.NaHSO4溶液显中性
(4)NaHSO4溶液与NaHCO3溶液反应的离子方程式为
III.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至Ba2+恰好沉淀完全,写出离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知下列七种物质:①H2O ②CO2 ③氢氧化钠 ④稀硫酸 ⑤淀粉溶液 ⑥氢氧化钡 ⑦饱和FeCl3溶液。根据上述提供的物质,按要求回答下列问题:
(1)属于非电解质的有___________ (填序号);
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为___________ 。
(3)实验室制备少量Fe(OH)3胶体所用的物质有___________ (填序号),反应的化学方程式为___________ 。
(4)向Fe(OH)3胶体中逐滴滴入过量的④,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生___________ ,随后沉淀溶解,得到黄色溶液,原因是___________ (用离子方程式表示)。
(1)属于非电解质的有
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(3)实验室制备少量Fe(OH)3胶体所用的物质有
(4)向Fe(OH)3胶体中逐滴滴入过量的④,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生
您最近一年使用:0次



