下列装置能达到实验目的是
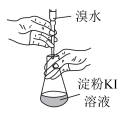 | 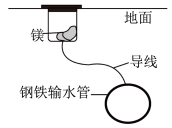 | 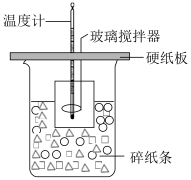 | 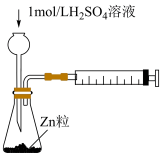 |
| 甲 | 乙 | 丙 | 丁 |
| A.甲:测定KI溶液浓度 |
| B.乙:利用牺牲阳极法来防止钢铁输水管的腐蚀 |
| C.丙:中和反应反应热的测定 |
| D.丁:测定Zn和稀硫酸反应的速率 |
更新时间:2023-11-10 16:37:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列操作会导致实验结果偏高的是
| A.中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值 |
| B.用标准NaOH溶液滴定未知盐酸溶液浓度,量取20.00mL待测盐酸溶液的滴定管未用待测盐酸溶液润洗 |
| C.用托盘天平称量10.5g某物质,砝码和药品的位置放反,所称药品的质量 |
| D.配制一定物质的量浓度稀硫酸溶液时,用量筒量取浓溶液的体积时仰视读数,所配溶液的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验装置能达到实验目的的是
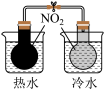 | 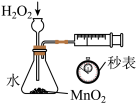 |  | 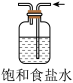 |
| A.验证温度对平衡移动的影响 | B.定量测定化学反应速率 | C.测定中和反应的反应热 | D.除去 中少量 中少量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列有关热化学方程式的叙述正确的是
| A.反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 |
| B.2H2(g)+ O2(g)= 2H2O(l) △H=-571.6kJ·mol-1,则氢气燃烧热为285.8kJ |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则稀H2SO4和稀Ca(OH)2溶液反应的中和热ΔH=-2×57.3 kJ·mol-1 |
| D.测定盐酸和NaOH溶液的中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH溶液起始温度和反应后的终止温度 |
您最近一年使用:0次
【推荐1】下列电极反应式与出现的环境相匹配的是
| 选项 | 电极反应式 | 出现的环境 |
| A | 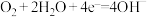 | 碱性环境下氢氧燃料电池的负极反应 |
| B |  | 弱酸性环境下钢铁的吸氧腐蚀 |
| C | 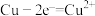 | 用铜做电极电解NaOH溶液的阳极反应 |
| D | 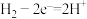 | 用惰性电极电解 溶液的阳极反应 溶液的阳极反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学与科学、技术、社会、环境密切相关。下列说法不正确的是
| A.家用铁锅用水清洗后放置在干燥处,能减弱电化学腐蚀 |
| B.加热能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 |
| C.某些抗酸药的主要成分是碳酸钠,作用是中和胃里过多的盐酸 |
| D.建国60周年燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等溶质质量分数的稀硫酸,将天平调节至平衡。然后向左盘的烧杯中加入8.4g铁,反应物之间恰好完全反应。欲使天平恢复平衡,则可向右盘的烧杯中加入( )
| A.8.4g碳酸钠 | B.8.4g氧化钙 | C.8.4g镁 | D.8.4g碳酸镁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某合金粉末11 g,加入到足量的稀硫酸中,在标准状况下产生的气体体积为11.2 L,此合金可能是( )
| A.Mg-Al合金 | B.Cu-Zn合金 | C.Zn-Fe合金 | D.Mg-Zn合金 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和镁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入2.5mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法正确的是


| A.样品中铝粉和镁粉的质量之比为2∶3 |
| B.原硝酸溶液中硝酸的物质的量为0.3mol |
C.c点时溶液中存在的主要离子有 、 、 、 、 、 、 |
| D.a点对应NaOH溶液的体积为44mL |
您最近一年使用:0次



